名校
1 . 改变某条件对反应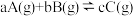 的化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量,
的化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量, 表示平衡转化率,
表示平衡转化率,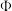 表示体积分数)。根据图象,下列判断正确的是
表示体积分数)。根据图象,下列判断正确的是
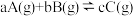 的化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量,
的化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量, 表示平衡转化率,
表示平衡转化率,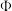 表示体积分数)。根据图象,下列判断正确的是
表示体积分数)。根据图象,下列判断正确的是
|
|
| 反应I | 反应Ⅱ |
|
|
| 反应Ⅲ | 反应Ⅳ |
A.反应I:若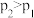 ,则此反应可以在任何温度下均自发进行 ,则此反应可以在任何温度下均自发进行 |
B.反应Ⅱ:此反应的 ,且 ,且 |
C.反应Ⅲ: 且 且 或 或 且 且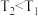 |
D.反应Ⅳ:在恒压条件下,若起始时充入反应物的物质的量相等且该反应为放热反应,则平衡时体积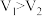 |
您最近一年使用:0次
解题方法
2 . 向2L恒容密闭容器中同时加入2
 和6
和6
 ,在催化剂作用下,发生反应:
,在催化剂作用下,发生反应:
ⅰ.

ⅱ.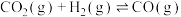

 。
。
平衡时 和
和 的选择性[CO的选择性
的选择性[CO的选择性 ]及
]及 的产率随温度的变化如图所示。下列说法错误的是
的产率随温度的变化如图所示。下列说法错误的是

 和6
和6
 ,在催化剂作用下,发生反应:
,在催化剂作用下,发生反应:ⅰ.


ⅱ.
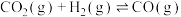

 。
。平衡时
 和
和 的选择性[CO的选择性
的选择性[CO的选择性 ]及
]及 的产率随温度的变化如图所示。下列说法错误的是
的产率随温度的变化如图所示。下列说法错误的是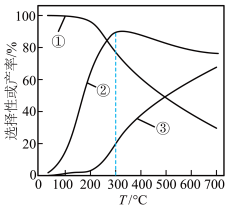
A.某温度下平衡后,向该容器中再加入1 乙醇,乙醇的平衡转化率会减小 乙醇,乙醇的平衡转化率会减小 |
| B.即使采用更高效的催化剂,反应ⅰ的正、逆反应的活化能之差也不变 |
| C.300℃之后以反应ⅰ为主 |
D.乙醇的平衡转化率为80%、 的选择性为60%时, 的选择性为60%时,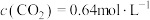 |
您最近一年使用:0次
名校
解题方法
3 . 将 置入抽空的刚性容器中,升高温度发生分解反应:
置入抽空的刚性容器中,升高温度发生分解反应: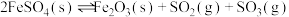 。平衡时
。平衡时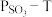 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是

 置入抽空的刚性容器中,升高温度发生分解反应:
置入抽空的刚性容器中,升高温度发生分解反应: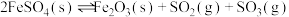 。平衡时
。平衡时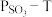 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
A.当容器中 时,说明该反应处于平衡状态 时,说明该反应处于平衡状态 |
| B.由图可知,此反应随着温度升高,反应速率增大,平衡常数减小 |
C.660K时,该反应的平衡总压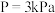 、平衡常数 、平衡常数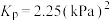 |
D.升高温度,上述容器中进一步发生反应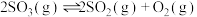 ,平衡时 ,平衡时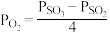 |
您最近一年使用:0次
名校
解题方法
4 . 在恒容密闭容器中通入X并发生反应:2X(g)=Y(g),T1、T2温度下X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是


| A.该反应进行到M点放出的热量大于进行到W点放出的热量 |
| B.T2温度下,在0- t1,时间内,v(Y)=a-b/t1mol·L-1min-1 |
| C.该反应的ΔH<0 |
| D.M点时向容器内充入一定量惰性气体,平衡向正反应方向移动 |
您最近一年使用:0次
2023-12-27更新
|
114次组卷
|
2卷引用:安徽省马鞍山市当涂第一中学2023-2024学年高二上学期1月期末化学试题
解题方法
5 . 一定温度下,在甲、乙、丙三个体积均为1L的恒容密闭容器中发生甲醇合成二甲醚的反应: ,起始时各物质的物质的量及平衡时各物质的物质的量如表所示。下列说法错误的是
,起始时各物质的物质的量及平衡时各物质的物质的量如表所示。下列说法错误的是
 ,起始时各物质的物质的量及平衡时各物质的物质的量如表所示。下列说法错误的是
,起始时各物质的物质的量及平衡时各物质的物质的量如表所示。下列说法错误的是| 容器 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | |
 |  |  | ||
| 甲 | 387 | 0.20 | 0.080 | 0.080 |
| 乙 | 387 | 0.40 | ||
| 丙 | 207 | 0.20 | 0.090 | 0.090 |
| A.该反应的正反应为放热反应 |
| B.甲容器中反应比丙容器中反应达到平衡状态所需时间长 |
C.平衡时,甲、乙容器中 的转化率相同 的转化率相同 |
D.若起始时向甲容器中充入 、 、 和 和 ,则反应向正反应方向进行 ,则反应向正反应方向进行 |
您最近一年使用:0次
解题方法
6 . 现有下列三个图像:

A.N2(g) + 3H2(g) 2NH3(g) △H<0 2NH3(g) △H<0 |
B.2SO3(g)  2SO2(g) +O2(g) △H>0 2SO2(g) +O2(g) △H>0 |
C.2HI(g)  H2(g) + I2(g) △H>0 H2(g) + I2(g) △H>0 |
D.4NH3(g) + 5O2(g)  4NO(g) + 6H2O(g) △H<0 4NO(g) + 6H2O(g) △H<0 |
您最近一年使用:0次
名校
解题方法
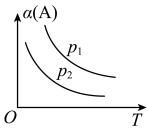
7 . 对于可逆反应mA(s)+nB(g)⇌eC(g)+fD(g),当其他条件不变时,C的体积分数[φ(C)]在不同温度(T)和不同压强(p)下随时间(t)的变化关系如图所示。下列叙述正确的是
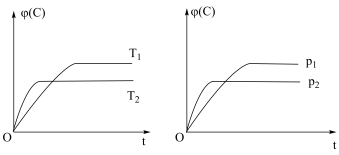

| A.达到平衡后,若使用催化剂,C的体积分数将增大 |
| B.该反应的ΔH<0 |
| C.化学方程式中,n>e+f |
| D.达到平衡后,增加A的质量有利于化学平衡向正反应方向移动 |
您最近一年使用:0次
2022-09-19更新
|
880次组卷
|
24卷引用:安徽省蚌埠市怀远禹泽、固镇县汉兴学校2023-2024学年高二上学期12月期末联考化学试题
安徽省蚌埠市怀远禹泽、固镇县汉兴学校2023-2024学年高二上学期12月期末联考化学试题黑龙江省绥化市青冈县第一中学2019-2020学年高二上学期(A)班月考化学试题山东省淄博市淄川中学2019-2020学年高二上学期期中考试化学试题西藏自治区拉萨市那曲第二高级中学2019-2020学年高二上学期期中考试化学试题湖南省岳阳市平江县第一中学2020-2021学年高二上学期10月联考化学试题甘肃省庆阳市第六中学2020-2021学年高二上学期期中考试化学(理)试题吉林省长春外国语学校2021-2022学年高二上学期第一次月考化学试题天津市武清区杨村第一中学2021-2022学年高二上学期第一次月考化学试题广西百色中学2021-2022学年高二上学期第一次月考化学试题天津市静海区四校2021-2022学年高二上学期11月阶段性检测化学试题(已下线)专题2 综合评价(2)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)黑龙江省大兴安岭实验中学(西校区)2021-2022学年高二上学期第一次月考化学试题湖南省益阳市箴言中学2021-2022学年高二上学期第三次月考化学试题三峡名校联盟2021-2022学年高二上学期联考化学试题天津市实验中学滨海学校2021-2022学年高二上学期期中质量监测化学试题河南省温县第一高级中学2022-2023学年高二上学期第二次月考化学试题黑龙江省牡丹江市第三高级中学2022-2023学年高二上学期期中考试化学试题浙江省杭州市长河高级中学2022-2023学年高二上学期期中考试化学试题章末检测卷(二)化学反应的方向、限度与速率黑龙江省齐齐哈尔市第八中学校2022-2023学年高二上学期11月期中考试化学试题浙江省台州市台州八校联盟2022-2023学年高二上学期11月期中联考化学试题山东省新泰市第一中学老校区(新泰中学)2023-2024学年高二上学期第一次质量检测化学试题天津市北辰区2023-2024学年高二上学期期中考试化学试题湖北省部分高中联考协作体2023-2024学年高二上学期期中考试化学试题
名校
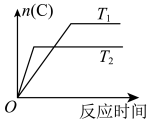
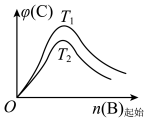
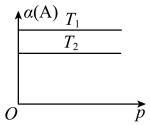
8 . 现有下列四个图像:
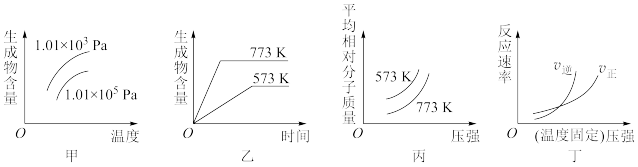
下列反应中全部符合上述图像的反应是

下列反应中全部符合上述图像的反应是
| A.N2(g)+3H2(g)⇌2NH3(g) ΔH1<0 |
| B.2SO3(g)⇌2SO2(g)+O2(g) ΔH2>0 |
| C.4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) ΔH3<0 |
| D.H2(g)+CO(g)⇌C(s)+H2O(g) ΔH4>0 |
您最近一年使用:0次
2021-12-28更新
|
638次组卷
|
45卷引用:2015-2016学年安徽省宣城郎溪中学高二上学期第三次月考化学试卷
2015-2016学年安徽省宣城郎溪中学高二上学期第三次月考化学试卷(已下线)2011届山东省潍坊市诸城一中高三12月阶段测试化学试卷(已下线)2011-2012年黑龙江双鸭山一中高二上学期期中考试化学试卷(已下线)2012-2013学年山东省威海市高二上学期期末考试化学试卷(已下线)2014-2015学年河南省汝州市高二上学期第一次月考化学试卷(已下线)2014-2015学年湖南省衡阳市第八中学高二上学期期中考试化学试卷2015-2016学年黑龙江省红兴隆第一高级中学高二上期中理科化学试卷2015-2016学年陕西省西安第七十中学高二上学期期中测试化学试卷2015-2016学年贵州省思南中学高二上二次月考化学试卷2016届陕西省蒲城尧山补习学校高三上学期第四次质检化学试卷2015-2016学年辽宁师大附中高一下学期6月月考化学试卷2016-2017学年辽宁省大连市第二十中学高二上9月月考化学试卷2016-2017学年黑龙江省铁人中学高二上开学测化学卷2017届湖北省武钢三中高三上学期11月月考化学试卷2018版化学(苏教版)高考总复习专题七题型冲关--巧解平衡及速率图像题甘肃省兰州第一中学2017-2018学年高二上学期期中考试化学(理)试题湖北省华中师范大学第一附属中学2018届高三上学期期中考试化学试题2018-2019学年鲁科版高中化学选修四:第2章检测题山东省德州市夏津一中2018-2019学年高二上学期第一次月考化学试题【全国百强校】甘肃省静宁县第一中学2018-2019学年高二上学期10月月考化学试题江西省上饶市第二中学2018-2019学年高二上学期期中考试化学试题【市级联考】湖南省娄底市2018-2019学年高二上学期期中考试化学试题江苏省泰州市第二中学2017-2018学年高二上学期期中考试化学试题云南省大理市下关一中2018-2019学年高二上学期期中考试化学试题【校级联考】湖北省宜昌市协作体2018-2019学年高二上学期期末考试化学试题江西省赣州市南康中学2019-2020学年高二上学期第一次月考化学试题山东省济南外国语学校三箭分校2019-2020学年高二上学期期中考试化学试题黑龙江省齐齐哈尔市第八中学2019-2020学年高二上学期期中考试化学试题甘肃省定西市岷县第二中学2019-2020学年高二上学期期中考试化学试题福建省建瓯市芝华中学2019-2020学年高二上学期期中考试化学(1-2班)试题江西省南昌市进贤一中2019-2020学年高二上学期期末考试化学试题甘肃省兰州市第十中学、民族中学2019-2020学年高二上学期期末考试化学试题广西钦州市2019-2020学年高二下学期期末教学质量监测化学试题河南省兰考县第三高级中学卫星试验部2020-2021学年高二上学期第一次月考化学试题辽宁省联合校2020-2021学年高二上学期第一次月考化学试题江西省南昌市第十中学2020-2021学年高二上学期第一次月考化学试题辽宁省大连市第一中学2021-2022学年高二上学期学情反馈(一)化学试题河南省洛阳市豫西名校2021-2022学年高二上学期第一次联考化学试题湖北省十堰市2016-2017学年高二上学期期末调研考试化学试题黑龙江省哈尔滨市德强高中2021-2022学年高二上学期期中考试化学试题江苏省盐城市大丰区新丰中学2021-2022学年高二上学期期中考试化学(选修)试题云南省丽江市第一高级中学2021-2022学年高二上学期元月考化学试题江苏省徐州市睢宁县第一中学2021-2022学年高二下学期第一次月考化学试题(已下线)第10讲 影响化学平衡的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)湖北省竹溪县第二高级中学2021-2022学年高二上学期12月月考化学试题
9 . 在体积均为1.0L的恒容密闭容器甲、乙中,起始投料量如表,在不同温度下发生反应:CO2(g)+C(s) 2CO(g)。CO的平衡浓度随温度的变化如图所示。下列说法正确的是
2CO(g)。CO的平衡浓度随温度的变化如图所示。下列说法正确的是

 2CO(g)。CO的平衡浓度随温度的变化如图所示。下列说法正确的是
2CO(g)。CO的平衡浓度随温度的变化如图所示。下列说法正确的是| 容器 | n(CO2)/mol | n(C)/mol | n(CO)/mol |
| 甲 | 0.1 | 0.3 | 0 |
| 乙 | 0 | 0 | 0.4 |

| A.曲线Ⅰ对应的是甲容器 |
| B.a、b两点所处状态的压强大小关系:9pa>14pb |
C.c点:CO的体积分数>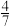 |
| D.900K时,若起始向容器乙中加入CO、CO2、C各1mol,则v(正)>v(逆) |
您最近一年使用:0次
2021-12-27更新
|
2466次组卷
|
15卷引用:安徽省安庆市第二中学2023-2024学年高二上学期期中考试化学试卷
安徽省安庆市第二中学2023-2024学年高二上学期期中考试化学试卷上海市金山区2022届高三一模化学试题(已下线)一轮巩固卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(上海卷)(已下线)专项12 化学反应速率与化学平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)江西省宜春市奉新县第一中学2021-2022学年高二下学期第一次月考化学试题上海市育才中学2022-2023学年高三上学期10月月考化学试题山东省青岛第二中学2022-2023学年高二上学期期中考试化学试题辽宁省大连市滨城高中联盟2022-2023学年高二上学期期中考试化学试题湖南省长沙市雅礼中学2022-2023学年高三上学期第五次月考化学试题湖南省攸县第二中学2022-2023学年高三第六次月考化学试题湖南省攸县第三中学2022-2023学年高三第六次月考化学试题湖南省常德市第一中学2023届高三第五次月考化学试题山东省滕州市第一中学2023-2024学年高二上学期10月月考化学试题河南省周口恒大中学2023-2024学年高二上学期9月月考化学试题(已下线)题型18 化学反应原理综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
名校
10 . 向体积为2L的恒容密闭容器中通入1.5mol CH4(g)和1.5 mol H2O(g),发生反应CH4(g)+H2O(g) CO(g)+3H2(g)。 在不同温度(Ta、Tb)下测得容器中n(CO) 随时间的变化曲线如图。下列说法正确的是
CO(g)+3H2(g)。 在不同温度(Ta、Tb)下测得容器中n(CO) 随时间的变化曲线如图。下列说法正确的是
 CO(g)+3H2(g)。 在不同温度(Ta、Tb)下测得容器中n(CO) 随时间的变化曲线如图。下列说法正确的是
CO(g)+3H2(g)。 在不同温度(Ta、Tb)下测得容器中n(CO) 随时间的变化曲线如图。下列说法正确的是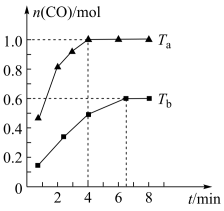
| A.Ta<Tb |
| B.该反应是放热反应 |
| C.Tb时,CH4的平衡转化率是60% |
D.Ta时,平衡后体系的压强为起始压强的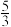 |
您最近一年使用:0次
2021-12-10更新
|
524次组卷
|
7卷引用:安徽省滁州市定远县育才学校2022-2023学年高二下学期期末化学试卷