解题方法
1 . 氢能是一种极具发展潜力的清洁能源。下列反应是目前大规模制取氢气的方法。
①
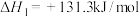
②


(1)

___________ ,此反应能够自发进行的条件是___________ (填“高温”、“低温”或“任何温度”)。
(2)在1.0L、830℃恒温恒容的密闭容器中,投入2.0molCO和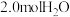 ,此时压强为
,此时压强为 ,只发生反应②,达到平衡时CO的平衡转化率为50%,写出反应②的平衡常数
,只发生反应②,达到平衡时CO的平衡转化率为50%,写出反应②的平衡常数 的
的表达式并计算出结果 
___________ (分压=物质的量分数×总压,用平衡分压代替平衡浓度计算的平衡常数即为 )。向上述密闭容器中再通入
)。向上述密闭容器中再通入 ,再次达到平衡时,CO的平衡转化率为
,再次达到平衡时,CO的平衡转化率为___________ ;实验发现,向上述体系中投入一定量的CaO可以增大 的体积分数,试说明原因
的体积分数,试说明原因___________ 。
(3)羰基硫(COS)是一种粮食熏蒸剂,结构与 类似,在一定条件可由类似上述反应②的反应制取:
类似,在一定条件可由类似上述反应②的反应制取: 。在若下个同温同体积的密闭容器中,以CO和
。在若下个同温同体积的密闭容器中,以CO和 体积比1∶1投料进行上述反应,反应相同时间,
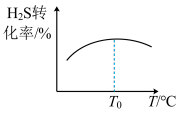
体积比1∶1投料进行上述反应,反应相同时间, 的转化率与温度(T)的关系如图所示。则
的转化率与温度(T)的关系如图所示。则
___________ (填“>”或“<”)0;转化率先增大后减小的原因是___________ 。
①

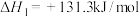
②



(1)


(2)在1.0L、830℃恒温恒容的密闭容器中,投入2.0molCO和
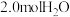 ,此时压强为
,此时压强为 ,只发生反应②,达到平衡时CO的平衡转化率为50%,写出反应②的平衡常数
,只发生反应②,达到平衡时CO的平衡转化率为50%,写出反应②的平衡常数 的
的
 )。向上述密闭容器中再通入
)。向上述密闭容器中再通入 ,再次达到平衡时,CO的平衡转化率为
,再次达到平衡时,CO的平衡转化率为 的体积分数,试说明原因
的体积分数,试说明原因(3)羰基硫(COS)是一种粮食熏蒸剂,结构与
 类似,在一定条件可由类似上述反应②的反应制取:
类似,在一定条件可由类似上述反应②的反应制取: 。在若下个同温同体积的密闭容器中,以CO和
。在若下个同温同体积的密闭容器中,以CO和 体积比1∶1投料进行上述反应,反应相同时间,
体积比1∶1投料进行上述反应,反应相同时间, 的转化率与温度(T)的关系如图所示。则
的转化率与温度(T)的关系如图所示。则

您最近一年使用:0次
2 . 正确判断反应自发进行的方向对于科学研究、生产实践具有重要意义。下列说法不正确 的是
A.反应 在任何温度条件都可自发进行 在任何温度条件都可自发进行 |
B.已知反应  。积极研究此反应合适的催化剂有助于除二氧化碳 。积极研究此反应合适的催化剂有助于除二氧化碳 |
C.已知: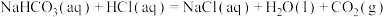 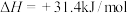 。说明在常温常压下,此反应自发进行的决定因素是熵增 。说明在常温常压下,此反应自发进行的决定因素是熵增 |
D.常温常压下可发生反应: ,说明此反应 ,说明此反应 |
您最近一年使用:0次
解题方法
3 . 下列对化学学科的认识不正确 的是
| A.工业上生产玻璃、水泥、漂白粉,均需要用石灰石为原料 |
| B.化学键断裂和形成时的能量变化是化学反应中能量变化的主要原因 |
| C.基元反应发生的先决条件是反应物的分子必须发生碰撞 |
| D.能够自发进行的反应一定是放热反应 |
您最近一年使用:0次
名校
解题方法
4 . 下列说法或表示方法中正确的是
A.101 kPa时, 燃烧热为316.25 kJ/mol,则表示氨气燃烧热的热化学方程式为: 燃烧热为316.25 kJ/mol,则表示氨气燃烧热的热化学方程式为: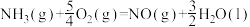 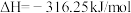 |
B.反应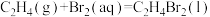 在常温下能自发进行,则该反应的 在常温下能自发进行,则该反应的 |
C.醋酸溶液和氢氧化钠溶液反应的热化学方程式为: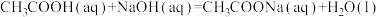  |
D.由于  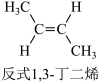  ,则顺式1,3—丁二烯比较稳定 ,则顺式1,3—丁二烯比较稳定 |
您最近一年使用:0次
2023-07-18更新
|
127次组卷
|
3卷引用:安徽省宣城市2022-2023学年高二上学期11月期中化学试题
名校
5 . 氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法正确的是
A.氢氧燃料电池的负极反应为 |
B.该氢氧燃料电池放电过程中消耗11.2L ,转移电子的数目为 ,转移电子的数目为 |
C.一定温度下,反应 能自发进行,该反应的 能自发进行,该反应的 |
D.反应 的 的 可通过下式估算: 可通过下式估算: 反应中形成新共价键的键能之和 反应中形成新共价键的键能之和 反应中断裂旧共价键的键能之和 反应中断裂旧共价键的键能之和 |
您最近一年使用:0次
6 . 下列反应在任意温度下一定能自发进行的是
A.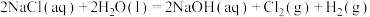 |
B. |
C.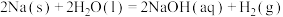 |
D.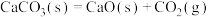 |
您最近一年使用:0次
23-24高二·全国·假期作业
名校
解题方法
7 . 下列对化学反应预测正确的是
| 选项 | 化学反应方程式 | 已知条件 | 预测 |
| A | M(s)=X(g)+Y(s) | ΔH>0 | 它是非自发反应 |
| B | W(s)+xG(g)=2Q(g) | ΔH<0,自发反应 | x可能等于1、2、3 |
| C | 4X(g)+5Y(g)=4W(g)+6G(g) | 能自发反应 | ΔH一定小于0 |
| D | 4M(s)+N(g)+2W(l)=4Q(s) | 常温下,自发进行 | ΔH>0 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-30更新
|
579次组卷
|
6卷引用:上海市嘉定区安亭高级中学2022-2023学年高二上学期期中考试化学试题
上海市嘉定区安亭高级中学2022-2023学年高二上学期期中考试化学试题(已下线)第07讲 化学反应的方向-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)河南省宜阳县第一高级中学2023-2024学年高二上学期能力达标测试化学试题(已下线)专题06 化学反应的方向及调控【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1) 宁夏回族自治区银川一中2023-2024学年高二上学期期中考试化学试题河南省郑州市宇华实验学校2023-2024学年高二下学期开学考试化学试题
名校
解题方法
8 . 含氮污染物的有效去除和资源的充分利用是重要研究课题,回答下列问题:
(1)利用工业尾气NO2与O3反应制备新型硝化剂N2O5,过程涉及以下反应:
Ⅰ.2O3(g)=3O2(g)△H1 平衡常数为K1
Ⅱ.4NO2(g)+O2(g)=2N2O5(g)△H2 平衡常数为K2
Ⅲ.2NO2(g)+O3(g)=N2O5(g)+O2(g)△H3平衡常数为K3
平衡常数K与温度T的函数关系为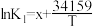 、
、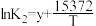 、
、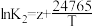 ,其中x、y、z为常数。
,其中x、y、z为常数。
①K1=________ (用含K2、K3的等式表示)。
②反应△H2________ 0 (填>或<),反应Ⅰ________ (填“高温“、“低温”或“任意温度”)下能自发进行。
③平衡常数与温度的函数关系式和②中一致,则 的取值范围是
的取值范围是________ 。(填序号)
A.<-2 B.-2~0 C.0~2 D.>2
(2)NH3与O2作用分别生成N2、NO和N2O的反应均为放热反应。工业尾气中的NH3可通过催化氧化为N2除去,将一定比例的NH3和N2的混合气体以一定的流速通过装有催化剂的反应管,NH3的转化率、N2的选择性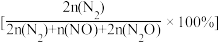 与温度的关系如图所示。
与温度的关系如图所示。
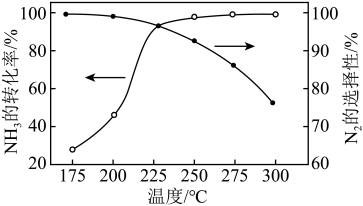
①其他条件不变,在175~300℃范围内升高温度,出口处氮氧化合物的含量____ (填“增大”或“减小“)。
②综合上述信息,需研发________ (填“高温“或“低温“)下N2选择性和催化效果更高的催化剂,能更有效除去尾气中的NH3。
(3)在催化剂条件下发生反应:2NO(g)+2CO(g)⇌N2(g)+2CO2(g)可消除NO和CO对环境的污染。为探究温度对该反应的影响,实验初始体系中气体分压p(CO)=p(NO)且p(CO2)=2p(N2),测得反应体系中CO和N2的分压随时间变化情况如表所示。
200℃时,该反应的化学平衡常数Kp=_______ (kPa)-1[Kp表示平衡常数计算表达式中用分压代替浓度计算所得的值],该反应的△H_________ 0(填“>“或“<“)。
(1)利用工业尾气NO2与O3反应制备新型硝化剂N2O5,过程涉及以下反应:
Ⅰ.2O3(g)=3O2(g)△H1 平衡常数为K1
Ⅱ.4NO2(g)+O2(g)=2N2O5(g)△H2 平衡常数为K2
Ⅲ.2NO2(g)+O3(g)=N2O5(g)+O2(g)△H3平衡常数为K3
平衡常数K与温度T的函数关系为
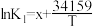 、
、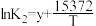 、
、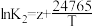 ,其中x、y、z为常数。
,其中x、y、z为常数。①K1=
②反应△H2
③平衡常数与温度的函数关系式和②中一致,则
 的取值范围是
的取值范围是A.<-2 B.-2~0 C.0~2 D.>2
(2)NH3与O2作用分别生成N2、NO和N2O的反应均为放热反应。工业尾气中的NH3可通过催化氧化为N2除去,将一定比例的NH3和N2的混合气体以一定的流速通过装有催化剂的反应管,NH3的转化率、N2的选择性
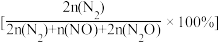 与温度的关系如图所示。
与温度的关系如图所示。
①其他条件不变,在175~300℃范围内升高温度,出口处氮氧化合物的含量
②综合上述信息,需研发
(3)在催化剂条件下发生反应:2NO(g)+2CO(g)⇌N2(g)+2CO2(g)可消除NO和CO对环境的污染。为探究温度对该反应的影响,实验初始体系中气体分压p(CO)=p(NO)且p(CO2)=2p(N2),测得反应体系中CO和N2的分压随时间变化情况如表所示。
| 时间/min | 0 | 30 | 60 | 120 | 180 | |
| 200℃ | CO的分压/kPa | 4 | 8.8 | 13 | 20 | 20 |
| N2的分压/kPa | 48 | 45.6 | 43.5 | 40 | 40 | |
| 300℃ | CO的分压/kPa | 100 | 69.0 | 48 | 48 | 48 |
| N2的分压/kPa | 10 | 25.5 | 36 | 36 | 36 | |
您最近一年使用:0次
9 . 恒温恒容密闭容器中,一定条件发生下列反应,有关说法不正确的是
| A.反应2H2S(g)+SO2(g)=3S(s)+2H2O(1)能自发进行,说明该反应的△H<0 |
| B.反应2HS(g)+3O2(g)=2SO2(g)+2H2O(g)的△H<0,说明反应物的键能总和小于生成物的键能总和 |
| C.反应CaCO3(s)=CaO(s)+CO2(g)达平衡后,向该容器中充入少量CO2,反应再次达平衡时,c(CO2)增大 |
D.反应2SO3(g) 2SO2(g)+O2(g)达平衡后,向该容器中加入正催化剂,活化分子百分数增大,反应速率加快 2SO2(g)+O2(g)达平衡后,向该容器中加入正催化剂,活化分子百分数增大,反应速率加快 |
您最近一年使用:0次
10 . 聚氯乙烯(PVC)制成的呼吸面罩在抗击新冠疫情中发挥了重要作用。工业上常用乙烯氧氯化法制氯乙烯单体:4CH2=CH2(g)+2Cl2(g)+O2(g) 4CH2=CHCl(g)+2H2O(g) △H。下列说法正确的是
4CH2=CHCl(g)+2H2O(g) △H。下列说法正确的是
 4CH2=CHCl(g)+2H2O(g) △H。下列说法正确的是
4CH2=CHCl(g)+2H2O(g) △H。下列说法正确的是| A.CH2=CH2是极性分子,分子中碳原子的杂化方式为sp2杂化 |
| B.CH2=CHCl分子中含有4个σ键和1个π键 |
| C.H2O分子VSEPR模型为四面体型,分子空间结构为V形 |
| D.该反应为自发反应,△H>0 |
您最近一年使用:0次



