名校
1 . 下列说法中错误的是
| A.焓降低且熵增加的反应,在任何温度下都能自发进行 |
| B.对于等物质的量的同一物质在不同状态时的熵值:气态>液态>固态 |
| C.平衡常数K值越大,则可逆反应进行越完全,反应物的转化率越大 |
| D.凡是能量达到活化能的分子发生的碰撞均为有效碰撞 |
您最近一年使用:0次
名校
2 . 对于反应4NH3(g)+5O2(g) 4NO(g) +6H2O(g) ΔH=-904 kJ·mol-1,下列有关说法不正确的是
4NO(g) +6H2O(g) ΔH=-904 kJ·mol-1,下列有关说法不正确的是
 4NO(g) +6H2O(g) ΔH=-904 kJ·mol-1,下列有关说法不正确的是
4NO(g) +6H2O(g) ΔH=-904 kJ·mol-1,下列有关说法不正确的是| A.该反应一定能自发进行 |
| B.该反应的正反应的活化能小于逆反应的活化能 |
| C.达到平衡时,增大容器的体积,v(正)增加、v(逆)减小 |
| D.断裂1mol N-H键的同时,断裂1mol O-H键,说明该反应达到平衡状态 |
您最近一年使用:0次
2023-04-30更新
|
207次组卷
|
2卷引用:江苏省连云港市东海县2022-2023学年高二上学期期中考试化学试题
名校
3 . 完成下列小题
(1)以CaO为吸收体,将生物材质(以C计)与水蒸气反应制取H2.相关主要反应如下:
I:C(s)+H2O(g)=CO(g)+H2(g) △H =+131.0kJ/mol
Ⅱ:CO(g)+H2O(g)=CO2(g)+H2(g) △H =-43kJ/mol
Ⅲ:CaO(s)+CO2(g)=CaCO3(s) △H =-178.3kJ/mol
①计算反应C(s)+2H2O(g)+CaO(s) CaCO3(s)+2H2(g)的△H =
CaCO3(s)+2H2(g)的△H =___________ kJ/mol;
②反应I能自发进行的条件是___________ (填“较低温度”“较高温度”或“任何温度”)。
(2)在一定体积的密闭容器中,进行如下化学反应: CO2(g)+H2(g)=CO(g)+H2O(g),其化学平衡常数K和温度T的关系如表所示:
回答下列问题:
①该反应的化学平衡常数表达式为K=___________ 。
②该反应的逆反应为___________ (填“吸热”或“放热”)反应。
③在1200℃时,加入1molCO2(g)和1molH2(g),充分反应,达到平衡时,CO2的转化率为___________ (保留三位有效数字)。
④在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2mol∙L-1,c(H2)为1.5mol∙L-1,c(CO)为1mol∙L-1,c(H2O)为3mol∙L-1,则此时平衡___________ (填“向左移动”“向右移动”或“不移动”)。
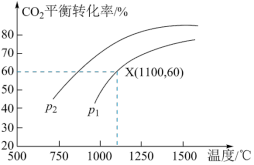
(3)可将炼铁产生的CO2与CH4反应得到气体燃料,其反应原理为:CO2(g)+CH4(g)=2CO(g)+2H2(g)。某小组向体积是1L的刚性密闭容器中充入物质的量均是1mol的CH4与CO2,反应过程中CO2的平衡转化率与温度、压强的关系如图所示。___________ p2(填“ ”或“
”或“ ”)。
”)。
②1100℃、p1kPa条件下,反应经tmin达到平衡,则平均反应速率v(CO2)=___________ mol/(L·min)。反应的平衡常数Kp=___________ (kPa)2(用含p1的代数式表示,Kp为以分压表示的平衡常数,分压 总压
总压 物质的量分数)。
物质的量分数)。
(1)以CaO为吸收体,将生物材质(以C计)与水蒸气反应制取H2.相关主要反应如下:
I:C(s)+H2O(g)=CO(g)+H2(g) △H =+131.0kJ/mol
Ⅱ:CO(g)+H2O(g)=CO2(g)+H2(g) △H =-43kJ/mol
Ⅲ:CaO(s)+CO2(g)=CaCO3(s) △H =-178.3kJ/mol
①计算反应C(s)+2H2O(g)+CaO(s)
 CaCO3(s)+2H2(g)的△H =
CaCO3(s)+2H2(g)的△H =②反应I能自发进行的条件是
(2)在一定体积的密闭容器中,进行如下化学反应: CO2(g)+H2(g)=CO(g)+H2O(g),其化学平衡常数K和温度T的关系如表所示:
| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 2 | 4 |
①该反应的化学平衡常数表达式为K=
②该反应的逆反应为
③在1200℃时,加入1molCO2(g)和1molH2(g),充分反应,达到平衡时,CO2的转化率为
④在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2mol∙L-1,c(H2)为1.5mol∙L-1,c(CO)为1mol∙L-1,c(H2O)为3mol∙L-1,则此时平衡
(3)可将炼铁产生的CO2与CH4反应得到气体燃料,其反应原理为:CO2(g)+CH4(g)=2CO(g)+2H2(g)。某小组向体积是1L的刚性密闭容器中充入物质的量均是1mol的CH4与CO2,反应过程中CO2的平衡转化率与温度、压强的关系如图所示。
 ”或“
”或“ ”)。
”)。②1100℃、p1kPa条件下,反应经tmin达到平衡,则平均反应速率v(CO2)=
 总压
总压 物质的量分数)。
物质的量分数)。
您最近一年使用:0次
22-23高二上·浙江杭州·期中
4 . 按要求完成下列问题。
(1)汽油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g),已知反应的△H>0,判断该设想能否实现________ (填“能”或“不能”),并简述原因________________ 。
(2)甲烷的烧热△H = - 890.3kJ/mol,写出甲烷的燃烧热的热化学方程式:__________________ 。
(1)汽油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g),已知反应的△H>0,判断该设想能否实现
(2)甲烷的烧热△H = - 890.3kJ/mol,写出甲烷的燃烧热的热化学方程式:
您最近一年使用:0次
22-23高二上·浙江杭州·期中
解题方法
5 . 下列说法不正确的是
| A.CaCO3(s)=CaO(s)+CO2(g) △H=+178.5kJ/mol,该反应高温才能自发 |
| B.增大压强(体积减小)或升高温度,均能增大活化分子百分数,从而加快化学反应速率 |
C.c(H+)=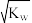 的溶液一定为中性 的溶液一定为中性 |
| D.发生化学反应的碰撞都是有效碰撞 |
您最近一年使用:0次
2023-03-28更新
|
191次组卷
|
3卷引用:【2022】【高二上】【期中考】【钱塘高级中学+杭州六县九校】
(已下线)【2022】【高二上】【期中考】【钱塘高级中学+杭州六县九校】浙江省杭州市“六县九校”联盟2022-2023学年高二上学期期中联考化学试题浙江省温州市2023-2024学年温州新力量联盟期中联考高二上学期化学试题卷
21-22高二·浙江·期中
6 . 用一种较活泼的金属把另一种金属从化合物中还原出来的方法称为金属热还原法。钠、镁、铝是常用的还原剂。一些常见的金属热还原反应如下:
下列说法不正确的是
| 序号 | 反应 | △H/kJ/mol | △S/J/(mol·K) |
| ① | 2Al(l) + 3BaO(s)=3Ba(g) +Al2O3(s) | 487 | 207.53 |
| ② | 2Al(s) + 3BaO(s)=3Ba(s)+Al2O3(s) | 4 | -15.70 |
| ③ | Mg(l) + 2RbCl(s)=2Rb(g)+MgCl2(s) | 381.77 | 223.06 |
| ④ | 4Na(l)+TiCl4(g)=Ti(s)+4NaCl(s) | -899.8 | -291 |
| A.反应①表明金属沸点:Al>Ba |
| B.对于反应:2Ba(s)+O2(g)=2BaO(s) △H1,4Al(s)+3O2(g)=2Al2O3(s) △H2,由反应②可以推出3△H1≈△H2 |
| C.反应③说明金属活动性顺序:Mg>Rb |
| D.对于反应④: |△H|>>|T△S|说明焓变对该反应的自发性起主要影响作用 |
您最近一年使用:0次
22-23高二上·浙江·期中
名校
解题方法
7 . 在容积不变的密闭容器中,一定量的SO2与O2发生反应:2SO2(g)+O2(g)⇌2SO3(g)。温度分别为t1和t2时,SO3的体积分数随时间的变化如图所示,下列关系不正确的是

| A.t1<t2 | B.△S<0 | C.△H>0 | D.K1>K2 |
您最近一年使用:0次
2023-03-28更新
|
235次组卷
|
6卷引用:【2022】【高二上】【期中考】【高中化学】60
(已下线)【2022】【高二上】【期中考】【高中化学】60(已下线)【2022】【高二化学】【期中考】-179(已下线)化学反应速率与化学平衡——课时5影响化学平衡的因素内蒙古呼伦贝尔市满洲里市第一中学2022-2023学年高二下学期第一次月考化学试题湖南省邵东市第一中学2022-2023学年高二下学期4月期中考试化学试题2.3化学反应的方向课后作业—巩固篇
名校
8 . 利用 可合成烷烃、烯烃、醇、甲酸等系列重要化工原料。回答下列有关问题:
可合成烷烃、烯烃、醇、甲酸等系列重要化工原料。回答下列有关问题:
Ⅰ.制备甲烷 。
。
已知: 的燃烧热为
的燃烧热为 ;
; 的燃烧热为
的燃烧热为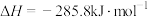 ;
;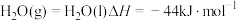 。
。
(1)
_______  ,该反应在
,该反应在_______ (填“低温”、“高温”或“任意温度”)下自发。
(2)在恒温、恒容容器中按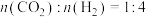 充入反应物进行该反应,下列
充入反应物进行该反应,下列不能 说明反应达到平衡状态的是_______。
(3)选择合适催化剂,在体积为VL的恒容容器中按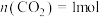 、
、 充入反应物,反应结果如下图所示。
充入反应物,反应结果如下图所示。
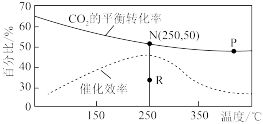
①计算平衡常数K(N)=_______ 。
②若无催化剂,N点平衡转化率是否可能降至R点_______ ,说明理由_______ 。
(4)选择合适催化剂,在相同温度下,分别在恒容容器Ⅰ和恒压容器Ⅱ中充入 和
和 ,起始容器体积相同,反应至平衡,在下图中画出两容器内反应至平衡混合气体平均摩尔质量随时间的变化曲线示意图
,起始容器体积相同,反应至平衡,在下图中画出两容器内反应至平衡混合气体平均摩尔质量随时间的变化曲线示意图_______ 。

Ⅱ.甲醇是重要的化工原料。利用合成气(主要成分为CO、 和
和 )在催化剂的作用下合成甲醇,可能发生的反应如下:
)在催化剂的作用下合成甲醇,可能发生的反应如下:
①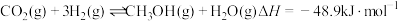
②
③
一定比例的合成气在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图所示。
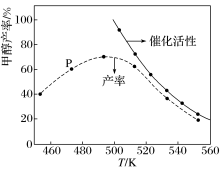
(5)温度为470K时,图中P点_______ (填“处于”或“不处于”)平衡状态,490K之后,甲醇的产率随温度的升高而减小的可能原因除了升高温度使反应①平衡逆向移动以外,还有_______ 。
(6)一定能提高甲醇产率的措施是_______ 。
A.增大压强 B.升高温度 C.加入大量催化剂
 可合成烷烃、烯烃、醇、甲酸等系列重要化工原料。回答下列有关问题:
可合成烷烃、烯烃、醇、甲酸等系列重要化工原料。回答下列有关问题:Ⅰ.制备甲烷
 。
。已知:
 的燃烧热为
的燃烧热为 ;
; 的燃烧热为
的燃烧热为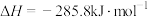 ;
;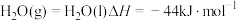 。
。(1)

 ,该反应在
,该反应在(2)在恒温、恒容容器中按
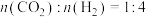 充入反应物进行该反应,下列
充入反应物进行该反应,下列A. 和 和 的转化率之比不再变化 的转化率之比不再变化 | B.混合气体的平均摩尔质量不再变化 |
| C.容器内的压强不再变化 | D.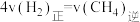 |
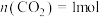 、
、 充入反应物,反应结果如下图所示。
充入反应物,反应结果如下图所示。
①计算平衡常数K(N)=
②若无催化剂,N点平衡转化率是否可能降至R点
(4)选择合适催化剂,在相同温度下,分别在恒容容器Ⅰ和恒压容器Ⅱ中充入
 和
和 ,起始容器体积相同,反应至平衡,在下图中画出两容器内反应至平衡混合气体平均摩尔质量随时间的变化曲线示意图
,起始容器体积相同,反应至平衡,在下图中画出两容器内反应至平衡混合气体平均摩尔质量随时间的变化曲线示意图
Ⅱ.甲醇是重要的化工原料。利用合成气(主要成分为CO、
 和
和 )在催化剂的作用下合成甲醇,可能发生的反应如下:
)在催化剂的作用下合成甲醇,可能发生的反应如下:①
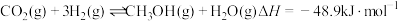
②

③

一定比例的合成气在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图所示。

(5)温度为470K时,图中P点
(6)一定能提高甲醇产率的措施是
A.增大压强 B.升高温度 C.加入大量催化剂
您最近一年使用:0次
名校
9 . 下列说法正确的是
A.一定温度下,对 平衡体系缩小体积,再次平衡时 平衡体系缩小体积,再次平衡时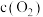 不变 不变 |
| B.加入适量的催化剂或增大压强,均可使反应物分子中活化分子的百分数增大 |
| C.燃烧热随化学方程式中各物质的化学计量数的改变而改变 |
D.水结冰的过程 , , |
您最近一年使用:0次
2023-03-06更新
|
166次组卷
|
2卷引用:山东省聊城市2022-2023学年高二上学期期末考试化学试题
名校
10 . 对于反应2NO(g)+2CO(g)⇌2CO2(g)+N2(g) ΔH=-746.5kJ⋅mol﹣1,下列说法正确的是
| A.该反应在任何条件下都能自发进行 |
B.反应的平衡常数可表示为K=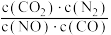 |
| C.使用高效的催化剂可以降低反应的焓变 |
D.其它条件不变,增大 的值,NO的转化率下降 的值,NO的转化率下降 |
您最近一年使用:0次
2023-03-06更新
|
417次组卷
|
8卷引用:山东省潍坊实验中学2022-2023学年高二上学期第一次单元过关检测化学试题



