名校
解题方法
1 . 已知,25℃时K2Cr2O7溶液中存在以下平衡:
①Cr2O (aq)+H2O(l)
(aq)+H2O(l) 2CrO
2CrO (aq)+2H+(aq) K1=3.27×10-15
(aq)+2H+(aq) K1=3.27×10-15
②Cr2O (aq)+H2O(l)
(aq)+H2O(l) 2HCrO
2HCrO (aq) K2=3.0×10-2
(aq) K2=3.0×10-2
③HCrO (aq)
(aq) CrO
CrO (aq)+H+(aq) K3
(aq)+H+(aq) K3
25℃时,0.1mol/LK2Cr2O7溶液中,lg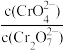 随pH的变化关系如图所示(lg3.27=0.52,10-0.78=0.17)。下列说法错误的是
随pH的变化关系如图所示(lg3.27=0.52,10-0.78=0.17)。下列说法错误的是
①Cr2O
 (aq)+H2O(l)
(aq)+H2O(l) 2CrO
2CrO (aq)+2H+(aq) K1=3.27×10-15
(aq)+2H+(aq) K1=3.27×10-15②Cr2O
 (aq)+H2O(l)
(aq)+H2O(l) 2HCrO
2HCrO (aq) K2=3.0×10-2
(aq) K2=3.0×10-2③HCrO
 (aq)
(aq) CrO
CrO (aq)+H+(aq) K3
(aq)+H+(aq) K325℃时,0.1mol/LK2Cr2O7溶液中,lg
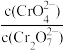 随pH的变化关系如图所示(lg3.27=0.52,10-0.78=0.17)。下列说法错误的是
随pH的变化关系如图所示(lg3.27=0.52,10-0.78=0.17)。下列说法错误的是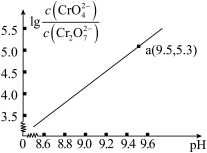
A.0.1mol/LK2Cr2O7溶液中,加入少量的HI气体,c(CrO )增大 )增大 |
| B.溶液颜色不再变化,可以判断该体系达到平衡 |
C.a点溶液中离子浓度关系:c(K+)>c(CrO )>c(Cr2O )>c(Cr2O )>c(H+) )>c(H+) |
D.反应③的化学平衡常数K3=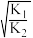 |
您最近一年使用:0次
2023-04-12更新
|
1364次组卷
|
8卷引用:湖南省2024届高三下学期高考仿真模拟卷(四)化学试题
湖南省2024届高三下学期高考仿真模拟卷(四)化学试题湘豫名校联考2022-2023学年高三上学期一轮复习诊断考试(二)化学试题(已下线)专题十二化学反应速率与平衡(已下线)专题21 电解质溶液图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)仿真卷01-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)回归教材重难点09 盘点溶液中的“四大”平衡-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)2023年高考山东卷化学真题变式题(不定项选择题)黑龙江省牡丹江市第二高级中学2023-2024学年高三下学期考前热身卷化学(三)试题
2 . 难溶盐 可溶于盐酸,常温下,用
可溶于盐酸,常温下,用 调节
调节 浊液的
浊液的 ,测得体系中
,测得体系中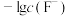 或
或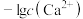 与
与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
 可溶于盐酸,常温下,用
可溶于盐酸,常温下,用 调节
调节 浊液的
浊液的 ,测得体系中
,测得体系中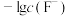 或
或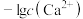 与
与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
A.M代表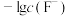 与 与 的变化曲线 的变化曲线 |
B.难溶盐 的溶度积常数 的溶度积常数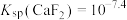 |
C.Y点的溶液中存在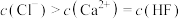 |
D.Z点的溶液中存在 |
您最近一年使用:0次
2023-02-18更新
|
2028次组卷
|
10卷引用:湖南省百校2023届高三开年摸底联考化学试题
湖南省百校2023届高三开年摸底联考化学试题浙江省杭州学军中学2022-2023学年高三下学期阶段性测试化学试题(已下线)素养卷05 电解质溶液中微粒变化图像题-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)先机卷 04 -【热题狂飙】2023年高考化学样卷(全国卷专用)广东省广州市等5地广州百师信息科技有限公司等2校2022-2023学年高三下学期开学考试化学试题山东省蒙阴第一中学等5校2023届高三开学摸底联考化学试题四川省绵阳市南山中学实验学校2022-2023学年高三下学期3月月考理科综合化学试题河南省南阳市第一中学校2023-2024学年高二上学期12月月考化学试题(已下线)选择题11-15(已下线)选择题11-12
名校
解题方法
3 . 弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。请回答下列有关平衡的问题。
Ⅰ.在一定温度下,向一个容积不变(1L)的密闭容器中,加入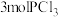 和
和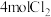 使之发生反应
使之发生反应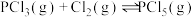 ,起始时压强为
,起始时压强为 ,平衡时容器内压强为起始时的6/7。计算并回答:
,平衡时容器内压强为起始时的6/7。计算并回答:
(1)已知:可逆反应的平衡常数可以用平衡分压代替平衡浓度(称为分压平衡常数,用 表示)计算,分压=总压×物质的量分数,则上述反应的
表示)计算,分压=总压×物质的量分数,则上述反应的
_______ (用含 的代数式表示)。
的代数式表示)。
(2)保持同一反应温度和体积,若将起始物改为amolPCl3,bmolCl2,cmol 。欲使平衡时各组分的体积分数与(1)中的一样,则a,b,c满足的关系为
。欲使平衡时各组分的体积分数与(1)中的一样,则a,b,c满足的关系为_______ 。
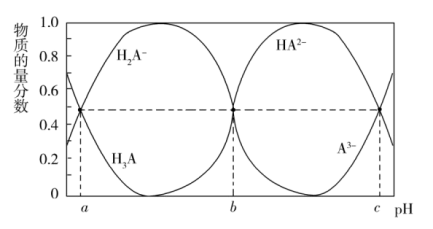
Ⅱ.某三元羧酸在表面活性剂、洗涤剂、润滑剂等方面具有重要的地位。常温时,向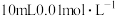 的溶液中滴入等浓度的NaOH溶液,H3A、
的溶液中滴入等浓度的NaOH溶液,H3A、 、
、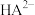 、
、 的物质的量分数与溶液的pH的关系如图所示。
的物质的量分数与溶液的pH的关系如图所示。
(3)常温时, 的
的 溶液的pH约为
溶液的pH约为_______ 。(已知 )
)
(4)常温时,反应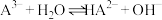 的平衡常数为K=
的平衡常数为K=_______ (用含a或b或c的代数式表示)
(5)当滴入30mLNaOH溶液时,下列溶液中微粒浓度关系正确的是_______
Ⅲ.含有 的废水毒性较大,某工厂废水中含
的废水毒性较大,某工厂废水中含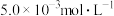 的
的 。为了使废水的排放达标,进行如下处理:
。为了使废水的排放达标,进行如下处理:
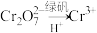 、
、
(6)该废水加硫酸酸化后,再加入绿矾( ),发生反应的离子方程式为
),发生反应的离子方程式为_______ 。
(7)若处理后的废水中残留的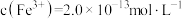 ,则残留的
,则残留的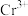 的浓度为
的浓度为_______ mol/L。(已知: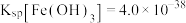 ,
,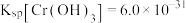 )。
)。
Ⅰ.在一定温度下,向一个容积不变(1L)的密闭容器中,加入
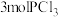 和
和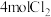 使之发生反应
使之发生反应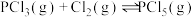 ,起始时压强为
,起始时压强为 ,平衡时容器内压强为起始时的6/7。计算并回答:
,平衡时容器内压强为起始时的6/7。计算并回答:(1)已知:可逆反应的平衡常数可以用平衡分压代替平衡浓度(称为分压平衡常数,用
 表示)计算,分压=总压×物质的量分数,则上述反应的
表示)计算,分压=总压×物质的量分数,则上述反应的
 的代数式表示)。
的代数式表示)。(2)保持同一反应温度和体积,若将起始物改为amolPCl3,bmolCl2,cmol
 。欲使平衡时各组分的体积分数与(1)中的一样,则a,b,c满足的关系为
。欲使平衡时各组分的体积分数与(1)中的一样,则a,b,c满足的关系为Ⅱ.某三元羧酸在表面活性剂、洗涤剂、润滑剂等方面具有重要的地位。常温时,向
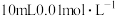 的溶液中滴入等浓度的NaOH溶液,H3A、
的溶液中滴入等浓度的NaOH溶液,H3A、 、
、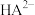 、
、 的物质的量分数与溶液的pH的关系如图所示。
的物质的量分数与溶液的pH的关系如图所示。
(3)常温时,
 的
的 溶液的pH约为
溶液的pH约为 )
)(4)常温时,反应
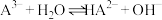 的平衡常数为K=
的平衡常数为K=(5)当滴入30mLNaOH溶液时,下列溶液中微粒浓度关系正确的是_______
A.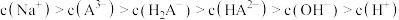 |
B.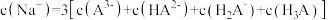 |
C.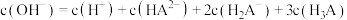 |
D.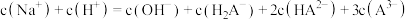 |
Ⅲ.含有
 的废水毒性较大,某工厂废水中含
的废水毒性较大,某工厂废水中含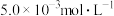 的
的 。为了使废水的排放达标,进行如下处理:
。为了使废水的排放达标,进行如下处理: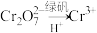 、
、
(6)该废水加硫酸酸化后,再加入绿矾(
 ),发生反应的离子方程式为
),发生反应的离子方程式为(7)若处理后的废水中残留的
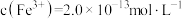 ,则残留的
,则残留的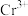 的浓度为
的浓度为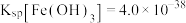 ,
,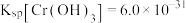 )。
)。
您最近一年使用:0次
2023-02-09更新
|
459次组卷
|
3卷引用:湖南省长沙市雅礼中学2022-2023学年高二上学期期末考试化学试题
名校
解题方法
4 . 钪及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广泛的应用。从钛白工业废酸(含钪、钛、铁、锰等离子)中提取氧化钪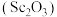 的一种流程如下:
的一种流程如下:
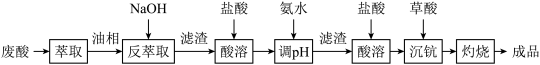
回答下列问题:
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合的实验操作是_______________________ 。
(2)常温下,先加入氨水调节 ,过滤,滤渣主要成分是
,过滤,滤渣主要成分是__________ ;再向滤液加入氨水调节 ,滤液中
,滤液中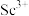 的浓度为
的浓度为__________ 。
{已知: 、
、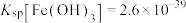 、
、 }
}
(3)用草酸“沉钪”,写出“沉钪”得到草酸钪的离子方程式:___________________________ 。
(4)草酸钪“灼烧”氧化的化学方程式为________________________________________________ 。
(5)废酸中含钪量为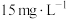 ,VL废酸最多可提取
,VL废酸最多可提取 的质量为
的质量为__________ 。
(6)镧与Sc同族位于第六周期,一种镧、锑形成的配合物结构如图所示:
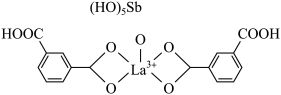
该结构中,中心离子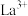 配位数为
配位数为__________ 。
(7)某铁、镧、锑的合金晶胞如图1,铁原子位于锑原子构成的正八面体的体心,晶胞的六个表面结构都如图2:
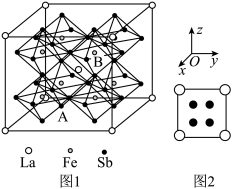
①若图中A点锑原子的坐标为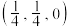 ,则B点铁原子的坐标为
,则B点铁原子的坐标为__________ 。
②若该晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Sb原子与Sb原子的最近距离为
,则Sb原子与Sb原子的最近距离为__________ cm。
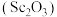 的一种流程如下:
的一种流程如下:
回答下列问题:
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合的实验操作是
(2)常温下,先加入氨水调节
 ,过滤,滤渣主要成分是
,过滤,滤渣主要成分是 ,滤液中
,滤液中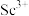 的浓度为
的浓度为{已知:
 、
、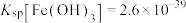 、
、 }
}(3)用草酸“沉钪”,写出“沉钪”得到草酸钪的离子方程式:
(4)草酸钪“灼烧”氧化的化学方程式为
(5)废酸中含钪量为
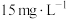 ,VL废酸最多可提取
,VL废酸最多可提取 的质量为
的质量为(6)镧与Sc同族位于第六周期,一种镧、锑形成的配合物结构如图所示:

该结构中,中心离子
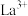 配位数为
配位数为(7)某铁、镧、锑的合金晶胞如图1,铁原子位于锑原子构成的正八面体的体心,晶胞的六个表面结构都如图2:

①若图中A点锑原子的坐标为
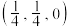 ,则B点铁原子的坐标为
,则B点铁原子的坐标为②若该晶体的密度为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Sb原子与Sb原子的最近距离为
,则Sb原子与Sb原子的最近距离为
您最近一年使用:0次
2023-02-06更新
|
598次组卷
|
3卷引用:湖南师范大学附属中学2022-2023学年高三上学期月考卷(六)化学试题
名校
解题方法
5 . 镍目前有广泛的用途,不仅可以用于不锈钢的制取中,目前也是三元锂电池中的重要元素。由红土镍矿(主要成分为NiO,还含有少量MgO2SiO2以及铁的氧化物等)可以制取黄钠铁矾[Na2Fe6(SO4)4(OH)12]和NiSO4·6H2O。
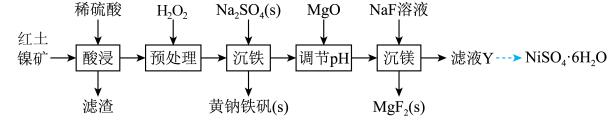
(1)Ni的价电子排布式为______ 。Ni(CO)4是用于烯烃、H2、CO制备高一级醛的重要催化剂,Ni(CO)4的空间结构类似于CH4分子,其空间结构为______ 。
(2)为加快红土镍矿的溶解,在酸浸步骤中可以采取的措施是______ (任写一条即可);“预处理”中,发生的离子方程式可能为______ 。
(3)“沉铁”中若采用Na2CO3作为除铁所需钠源,Na2CO3溶液的用量对体系pH和镍的损失影响如图1所示。当Na2CO3溶液的用量超过6g/L时,镍的损失率会增大,其可能的原因是______ 。(Fe3+、Ni2+开始沉淀的pH分别为2.2、7.5)
(4)若溶液中c(Mg2+)为0.1mol/L,溶液的体积为1L,则要使溶液中c(Mg2+)=7.4×10-7mol/L,则应加入固体NaF为______ mol[忽略体积的变化,已知Ksp(MgF2)=7.4×10-11]。“沉镁”时应保证MgO已将溶液的pH调节至5.5~6.0的原因是______ 。
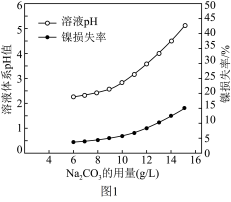
(5)硫酸钠与硫酸镍晶体溶解度曲线图如图2所示,请设计由滤液Y制备NiSO4·6H2O的实验方案:______ 。[可选用的试剂:稀硫酸,NaOH溶液、BaCl2溶液、Ca(OH)2、蒸馏水]


(1)Ni的价电子排布式为
(2)为加快红土镍矿的溶解,在酸浸步骤中可以采取的措施是
(3)“沉铁”中若采用Na2CO3作为除铁所需钠源,Na2CO3溶液的用量对体系pH和镍的损失影响如图1所示。当Na2CO3溶液的用量超过6g/L时,镍的损失率会增大,其可能的原因是
(4)若溶液中c(Mg2+)为0.1mol/L,溶液的体积为1L,则要使溶液中c(Mg2+)=7.4×10-7mol/L,则应加入固体NaF为

(5)硫酸钠与硫酸镍晶体溶解度曲线图如图2所示,请设计由滤液Y制备NiSO4·6H2O的实验方案:

您最近一年使用:0次
2023-02-05更新
|
780次组卷
|
2卷引用:湖南省长沙市长郡中学2023届高三月考(六)化学试题
2022·江苏南通·模拟预测
名校
解题方法
6 . 实验小组以某铜渣(主要成分 、
、 ,含少量
,含少量 和
和 )为原料先制备硫酸铜,再由硫酸铜制备碱式碳酸铜[
)为原料先制备硫酸铜,再由硫酸铜制备碱式碳酸铜[ ]。实验包括如下过程:
]。实验包括如下过程:
(1)浸取。
将一定量的铜渣粉碎后加入到如图-1所示的三颈烧瓶中,再通过分液漏斗分批滴入稀硝酸和稀硫酸混合溶液,滴加液体的间隔利用二连球鼓入O2,铜渣充分反应后,向溶液中加入少量 ,过滤。
,过滤。
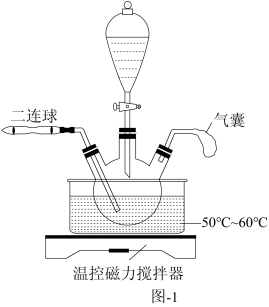
①已知浸取时无S和SO2生成,写出浸取时 所发生反应的离子方程式:
所发生反应的离子方程式:_______ 。
②滴加液体的间隔向三颈烧瓶内鼓入O2的目的是_______ 。
③当观察到_______ ,可以停止鼓入O2。
④加入 的目的是
的目的是_______ 。[已知 ]
]
(2)制取 。
。
向滤液中加入 溶液调节
溶液调节 范围为
范围为_______ ,过滤;向滤渣中加入稀硫酸至滤渣恰好完全溶解,得 溶液。{设
溶液。{设 、
、 开始沉淀时
开始沉淀时 ,沉淀完全时
,沉淀完全时 。
。 ,
, }
}
(3)制 。
。
已知 的产率{
的产率{ }随起始
}随起始 与
与 的比值和溶液pH的关系如图2所示。
的比值和溶液pH的关系如图2所示。
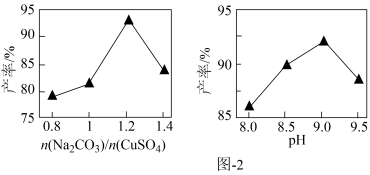
①补充完整制取 的实验方案:向烧杯中加入
的实验方案:向烧杯中加入 溶液,将烧杯置于70℃的水浴中,
溶液,将烧杯置于70℃的水浴中,_______ ,低温烘干,得到 。(实验中可选用的试剂或仪器:
。(实验中可选用的试剂或仪器: 溶液、
溶液、 溶液、
溶液、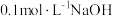 溶液、
溶液、 盐酸、pH计)
盐酸、pH计)
②实验时发现,若反应时溶液pH过大,所得 的产率偏低,但Cu元素含量偏大,原因是
的产率偏低,但Cu元素含量偏大,原因是_______ 。
 、
、 ,含少量
,含少量 和
和 )为原料先制备硫酸铜,再由硫酸铜制备碱式碳酸铜[
)为原料先制备硫酸铜,再由硫酸铜制备碱式碳酸铜[ ]。实验包括如下过程:
]。实验包括如下过程:(1)浸取。
将一定量的铜渣粉碎后加入到如图-1所示的三颈烧瓶中,再通过分液漏斗分批滴入稀硝酸和稀硫酸混合溶液,滴加液体的间隔利用二连球鼓入O2,铜渣充分反应后,向溶液中加入少量
 ,过滤。
,过滤。
①已知浸取时无S和SO2生成,写出浸取时
 所发生反应的离子方程式:
所发生反应的离子方程式:②滴加液体的间隔向三颈烧瓶内鼓入O2的目的是
③当观察到
④加入
 的目的是
的目的是 ]
](2)制取
 。
。向滤液中加入
 溶液调节
溶液调节 范围为
范围为 溶液。{设
溶液。{设 、
、 开始沉淀时
开始沉淀时 ,沉淀完全时
,沉淀完全时 。
。 ,
, }
}(3)制
 。
。已知
 的产率{
的产率{ }随起始
}随起始 与
与 的比值和溶液pH的关系如图2所示。
的比值和溶液pH的关系如图2所示。
①补充完整制取
 的实验方案:向烧杯中加入
的实验方案:向烧杯中加入 溶液,将烧杯置于70℃的水浴中,
溶液,将烧杯置于70℃的水浴中, 。(实验中可选用的试剂或仪器:
。(实验中可选用的试剂或仪器: 溶液、
溶液、 溶液、
溶液、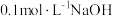 溶液、
溶液、 盐酸、pH计)
盐酸、pH计)②实验时发现,若反应时溶液pH过大,所得
 的产率偏低,但Cu元素含量偏大,原因是
的产率偏低,但Cu元素含量偏大,原因是
您最近一年使用:0次
2022-04-21更新
|
1275次组卷
|
3卷引用:湖南省常德市汉寿县第一中学2021-2022学年高三下学期4月月考化学试题
湖南省常德市汉寿县第一中学2021-2022学年高三下学期4月月考化学试题(已下线)江苏省南通市如皋市2021-2022学年高三下学期 4月适应性考试(二)化学试题江苏省响水中学2021-2022学年高二下学期第二次学情分析考试化学试题
解题方法
7 . 钪( )是地壳中含量极少的稀土元素,在照明、合金和催化剂等领域有重要应用。钛铁矿的主要成分为
)是地壳中含量极少的稀土元素,在照明、合金和催化剂等领域有重要应用。钛铁矿的主要成分为 (可表示为
(可表示为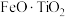 ),还含有少量
),还含有少量 等氧化物,从钛铁矿中提取
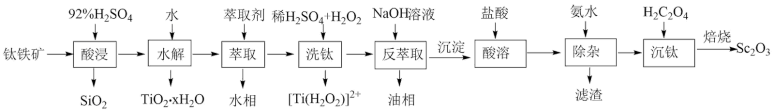
等氧化物,从钛铁矿中提取 的流程如下:
的流程如下:
已知:①当离子浓度减小至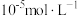 时可认为沉淀完全
时可认为沉淀完全
②室温下,溶液中离子沉淀完全的 如下表所示:
如下表所示:
③ ,
,
回答下列问题:
(1)“酸浸”后 元素转化为
元素转化为 ,其水解反应的化学方程式是
,其水解反应的化学方程式是___________ 。
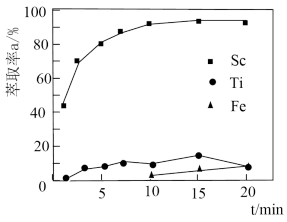
(2)“萃取”时,使用 煤油作为萃取剂,一定条件下萃取率
煤油作为萃取剂,一定条件下萃取率 受振荡时间的影响如图,萃取时选择最佳的振荡时间为
受振荡时间的影响如图,萃取时选择最佳的振荡时间为___________  。
。
(3)“洗钛”所得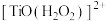 为橘黄色的稳定离子,
为橘黄色的稳定离子, 的作用是
的作用是___________ 。(写出两点)
(4)“酸溶”后滤液中存在的阳离子 浓度均小于
浓度均小于 “除杂”过程中应控制的
“除杂”过程中应控制的 范围是
范围是___________ 。
(5)“沉钪”后得到五水草酸钪,焙烧生成四种氧化物。其反应的化学方程式为___________ 。
 )是地壳中含量极少的稀土元素,在照明、合金和催化剂等领域有重要应用。钛铁矿的主要成分为
)是地壳中含量极少的稀土元素,在照明、合金和催化剂等领域有重要应用。钛铁矿的主要成分为 (可表示为
(可表示为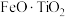 ),还含有少量
),还含有少量 等氧化物,从钛铁矿中提取
等氧化物,从钛铁矿中提取 的流程如下:
的流程如下:
已知:①当离子浓度减小至
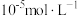 时可认为沉淀完全
时可认为沉淀完全②室温下,溶液中离子沉淀完全的
 如下表所示:
如下表所示:| 离子 |  |  |  |
沉淀完全的 | 3.2 | 9.0 | 1.05 |
 ,
,回答下列问题:
(1)“酸浸”后
 元素转化为
元素转化为 ,其水解反应的化学方程式是
,其水解反应的化学方程式是(2)“萃取”时,使用
 煤油作为萃取剂,一定条件下萃取率
煤油作为萃取剂,一定条件下萃取率 受振荡时间的影响如图,萃取时选择最佳的振荡时间为
受振荡时间的影响如图,萃取时选择最佳的振荡时间为 。
。
(3)“洗钛”所得
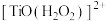 为橘黄色的稳定离子,
为橘黄色的稳定离子, 的作用是
的作用是(4)“酸溶”后滤液中存在的阳离子
 浓度均小于
浓度均小于 “除杂”过程中应控制的
“除杂”过程中应控制的 范围是
范围是(5)“沉钪”后得到五水草酸钪,焙烧生成四种氧化物。其反应的化学方程式为
您最近一年使用:0次
名校
解题方法
8 . 以钛铁矿(主要成分为FeO·TiO2,还含有MgO、CaO、SiO2等杂质)为原料合成锂离子电池的电极材料钛酸锂(Li4Ti5O12)和磷酸亚铁锂(LiFePO4)的工艺流程如下:
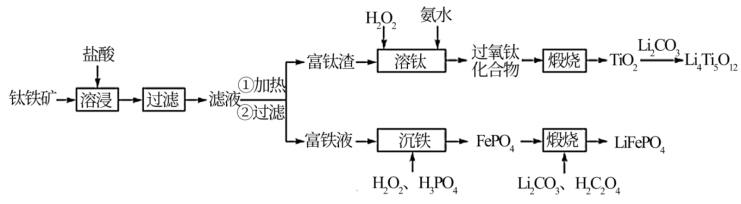
回答下列问题:
(1)“溶浸”后溶液中的金属阳离子主要包括Mg2+、TiOCl+___________ 。“滤液”经加热水解后转化为富钛渣(钛元素主要以TiO2·2H2O形式存在),写出上述转变的离子方程式:___________ 。
(2)“溶钛”过程反应温度不能太高,其原因是___________ 。
(3)“沉铁”步骤反应的化学方程式为___________ ,“沉铁”后的滤液经处理后可返回___________ 工序循环利用。
(4)“煅烧”制备LiFePO4过程中,Li2CO3和H2C2O4的理论投入量的物质的量之比为___________ 。
(5)以Li4Ti5O12和LiFePO4作电极组成电池,充电时发生反应:Li4Ti5O12+LiFePO4=Li4+xTi5O12+Li1-xFePO4(0<x<1),阳极的电极反应式为___________ 。
(6)从废旧LiFePO4电极中可回收锂元素。用硝酸充分溶浸废旧LiFePO4电极,测得浸取液中c(Li+)=4mol·L-1,加入等体积的碳酸钠溶液将Li+转化为Li2CO3沉淀 ,若沉淀中的锂元素占浸取液中锂元素总量的90%,则反应后的溶液中CO 的浓度为
的浓度为___________ mol·L-1[已知Ksp(Li2CO3)=1.6×10-3,假设反应后溶液体积为反应前两溶液之和]。

回答下列问题:
(1)“溶浸”后溶液中的金属阳离子主要包括Mg2+、TiOCl+
(2)“溶钛”过程反应温度不能太高,其原因是
(3)“沉铁”步骤反应的化学方程式为
(4)“煅烧”制备LiFePO4过程中,Li2CO3和H2C2O4的理论投入量的物质的量之比为
(5)以Li4Ti5O12和LiFePO4作电极组成电池,充电时发生反应:Li4Ti5O12+LiFePO4=Li4+xTi5O12+Li1-xFePO4(0<x<1),阳极的电极反应式为
(6)从废旧LiFePO4电极中可回收锂元素。用硝酸充分溶浸废旧LiFePO4电极,测得浸取液中c(Li+)=4mol·L-1,加入等体积的碳酸钠溶液将Li+转化为Li2CO3沉淀 ,若沉淀中的锂元素占浸取液中锂元素总量的90%,则反应后的溶液中CO
 的浓度为
的浓度为
您最近一年使用:0次
2021-08-06更新
|
1506次组卷
|
4卷引用:湖南省株洲市第八中学021-2022学年高三下学期5月月考化学试题
湖南省株洲市第八中学021-2022学年高三下学期5月月考化学试题九师联盟2021届高三下学期5月“考前练兵”联考理综化学试题宁夏回族自治区银川一中2022届高三二模理科综合化学试题(已下线)专题01 工艺流程专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)
9 . 下图1为从铜转炉烟火[主要含有ZnO,还有少量的Fe(II)、Pb、Cu、As元素]制取活性氧化锌的流程。请回答以下问题:
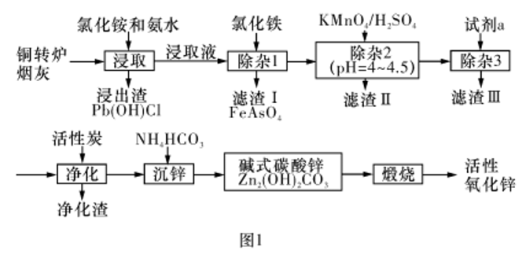
已知:①活性炭主要吸附有机质;②25℃时,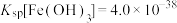 ;③氨体系环境中锌元素以
;③氨体系环境中锌元素以 形式存在;④部分金属离子开始沉淀和完全沉淀的pH:
形式存在;④部分金属离子开始沉淀和完全沉淀的pH:
(1)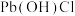 中Pb的化合价为
中Pb的化合价为____ 。
(2)题中所列铜转炉烟灰所含主要元素中有___ 种非主族元素,画出 的原子结构示意图
的原子结构示意图___ 。
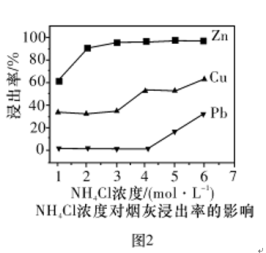
(3)浸取温度为50℃,反应时间为1h时,测定各元素的浸出率与氯化铵溶液浓度的关系如图2,则氯化铵最适宜的浓度为____  。
。
(4)加入适量 溶液的目的是除去铁元素的同时溶液中不会有明显的锰元素残留,写出除铁步骤的离子方程式:
溶液的目的是除去铁元素的同时溶液中不会有明显的锰元素残留,写出除铁步骤的离子方程式:_______ ,常温下此时体系中 残留最大浓度为
残留最大浓度为_______  。
。
(5)“滤渣Ⅲ”的主要成分为_______ (填化学式)。
(6)“沉锌”反应的离子方程式为_______ 。

已知:①活性炭主要吸附有机质;②25℃时,
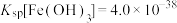 ;③氨体系环境中锌元素以
;③氨体系环境中锌元素以 形式存在;④部分金属离子开始沉淀和完全沉淀的pH:
形式存在;④部分金属离子开始沉淀和完全沉淀的pH:| 金属离子 |  |  |  |  |
| 开始沉淀pH | 1.9 | 7.0 | 4.5 | 8.1 |
| 完全沉淀pH | 3.2 | 9.0 | 6.4 | 10.1 |
(1)
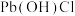 中Pb的化合价为
中Pb的化合价为(2)题中所列铜转炉烟灰所含主要元素中有
 的原子结构示意图
的原子结构示意图(3)浸取温度为50℃,反应时间为1h时,测定各元素的浸出率与氯化铵溶液浓度的关系如图2,则氯化铵最适宜的浓度为
 。
。
(4)加入适量
 溶液的目的是除去铁元素的同时溶液中不会有明显的锰元素残留,写出除铁步骤的离子方程式:
溶液的目的是除去铁元素的同时溶液中不会有明显的锰元素残留,写出除铁步骤的离子方程式: 残留最大浓度为
残留最大浓度为 。
。(5)“滤渣Ⅲ”的主要成分为
(6)“沉锌”反应的离子方程式为
您最近一年使用:0次
2021-04-10更新
|
1099次组卷
|
3卷引用:湖南省六校2021届高三4月联考化学试题
10 . 某温度下,分别向20mL浓度均为xmol/L的NaCl和Na2CrO4溶液中滴加0.1mol/LAgNO3溶液,滴加过程中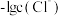 和
和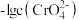 与AgNO3溶液的体积关系如图所示。下列说法不正确的是
与AgNO3溶液的体积关系如图所示。下列说法不正确的是
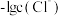 和
和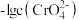 与AgNO3溶液的体积关系如图所示。下列说法不正确的是
与AgNO3溶液的体积关系如图所示。下列说法不正确的是
| A.x =0.1 | B.曲线I代表NaCl溶液 |
| C.Ksp(Ag2CrO4)约为4×10-12 | D.y=9 |
您最近一年使用:0次
2020-04-25更新
|
2168次组卷
|
8卷引用:湖南省株洲市南方中学2023届高三上学期第一次月考化学试题



