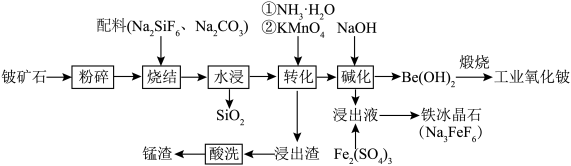
1 . 铍作为一种稀有元素,在航空航天、电子加工等领域具有重要意义。用铍矿石(含BeO及少量Ca、Mg、Mn元素)与配料生产工业氧化铍的工艺流程如下: 的还原产物为
的还原产物为 。回答下列问题:
。回答下列问题:
(1)若缺少粉碎步骤,产生的影响为_______ 。
(2)烧结时,若铍矿石中BeO恰好转化为 ,Si元素转化为
,Si元素转化为 ,则BeO发生反应的化学方程式为
,则BeO发生反应的化学方程式为_______ 。
(3)水浸后溶液中仍有未反应的 ,加入
,加入 后会转化为
后会转化为 沉淀,所得产物可除去溶液中的钙、镁元素,
沉淀,所得产物可除去溶液中的钙、镁元素, 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(4)水浸后溶液中Mn元素以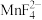 形式存在,加入稍过量
形式存在,加入稍过量 溶液煮沸50min至溶液
溶液煮沸50min至溶液______ 时说明反应结束。结合平衡移动原理解释酸洗时控制溶液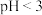 的原因:
的原因:______ 。
(5)碱化时,室温下加入NaOH,控制 ,析出颗粒状的
,析出颗粒状的 ,所得浸出液中
,所得浸出液中 ,此时溶液中
,此时溶液中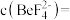
___  。已知
。已知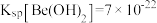 ,
,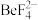 的解离常数
的解离常数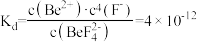
(6)碱化后浸出液中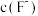 远高于排放标准,向其中加入硫酸铁生成
远高于排放标准,向其中加入硫酸铁生成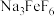 ,
, 为八面体结构,则Fe原子采取的杂化方式为
为八面体结构,则Fe原子采取的杂化方式为____ (填标号)。
A. B.
B. C.
C.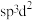
 的还原产物为
的还原产物为 。回答下列问题:
。回答下列问题:(1)若缺少粉碎步骤,产生的影响为
(2)烧结时,若铍矿石中BeO恰好转化为
 ,Si元素转化为
,Si元素转化为 ,则BeO发生反应的化学方程式为
,则BeO发生反应的化学方程式为(3)水浸后溶液中仍有未反应的
 ,加入
,加入 后会转化为
后会转化为 沉淀,所得产物可除去溶液中的钙、镁元素,
沉淀,所得产物可除去溶液中的钙、镁元素, 发生反应的离子方程式为
发生反应的离子方程式为(4)水浸后溶液中Mn元素以
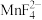 形式存在,加入稍过量
形式存在,加入稍过量 溶液煮沸50min至溶液
溶液煮沸50min至溶液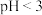 的原因:
的原因:(5)碱化时,室温下加入NaOH,控制
 ,析出颗粒状的
,析出颗粒状的 ,所得浸出液中
,所得浸出液中 ,此时溶液中
,此时溶液中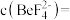
 。已知
。已知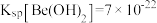 ,
,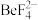 的解离常数
的解离常数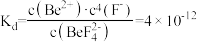
(6)碱化后浸出液中
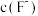 远高于排放标准,向其中加入硫酸铁生成
远高于排放标准,向其中加入硫酸铁生成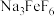 ,
, 为八面体结构,则Fe原子采取的杂化方式为
为八面体结构,则Fe原子采取的杂化方式为A.
 B.
B. C.
C.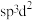
您最近一年使用:0次
2 .  可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以
可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以 形式存在,还含有
形式存在,还含有 、
、 、
、 、
、 等物质。以独居石为原料制备
等物质。以独居石为原料制备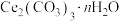 的工艺流程如下:
的工艺流程如下:
 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以
可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以 形式存在,还含有
形式存在,还含有 、
、 、
、 、
、 等物质。以独居石为原料制备
等物质。以独居石为原料制备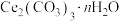 的工艺流程如下:
的工艺流程如下: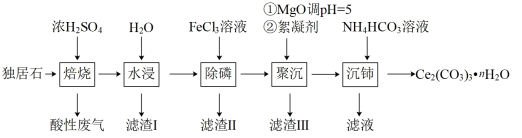
| A.焙烧过程中产生的酸性废气可用于刻蚀玻璃 |
B.滤渣Ⅲ的主要成分是 和 和 |
C.“沉铈”步骤,也可以用 沉淀得到 沉淀得到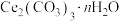 |
D.分离出 的方法为过滤,需用到的玻璃仪器:漏斗、烧杯和玻璃棒 的方法为过滤,需用到的玻璃仪器:漏斗、烧杯和玻璃棒 |
您最近一年使用:0次
解题方法
3 . 25℃时,将含有I-的溶液逐滴加入到含有Hg2+的溶液中,发生一系列可逆反应生成HgI+、HgI2(s)、 、
、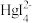 。其中,Hg2+、HgI+、
。其中,Hg2+、HgI+、 、
、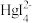 四种离子浓度的对数lgc与I-浓度的对数lgc(I-)关系如图所示(图中虚线及虚线的上方是HgI2的沉淀区)。下列说法正确的是
四种离子浓度的对数lgc与I-浓度的对数lgc(I-)关系如图所示(图中虚线及虚线的上方是HgI2的沉淀区)。下列说法正确的是
 、
、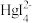 。其中,Hg2+、HgI+、
。其中,Hg2+、HgI+、 、
、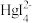 四种离子浓度的对数lgc与I-浓度的对数lgc(I-)关系如图所示(图中虚线及虚线的上方是HgI2的沉淀区)。下列说法正确的是
四种离子浓度的对数lgc与I-浓度的对数lgc(I-)关系如图所示(图中虚线及虚线的上方是HgI2的沉淀区)。下列说法正确的是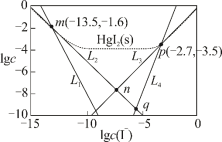
| A.Ksp(HgI2)的数量级为10-28 |
| B.n点的坐标为(-7.15,-7.95) |
C.反应 (aq) (aq) HgI2(s)+I-(aq)的平衡常数为K=10-0.8 HgI2(s)+I-(aq)的平衡常数为K=10-0.8 |
D.q点溶液中存在:c(H+)+2c(Hg2+)=c(OH-)+c(I-)+c(HgI )+c(HgI )+c(HgI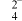 ) ) |
您最近一年使用:0次
4 . 下列描述对应方程式错误的是
A. 溶液在冷水和热水中颜色不同: 溶液在冷水和热水中颜色不同: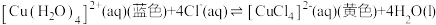  |
B.施加适量石膏降低盐碱地土壤的碱性: |
C.用FeS除去废水中的 : :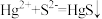 |
D.硅酸钠溶液存放过程中变浑浊: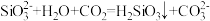 |
您最近一年使用:0次
名校
5 . 铬的化合物应用广泛,工业上以铬铁矿(含Al、Si氧化物等杂质)为主要原料制备红矾钠( )的工艺流程如下图。已知:①
)的工艺流程如下图。已知:① 中Cr的化合价为+3;②焙烧的目的是将
中Cr的化合价为+3;②焙烧的目的是将 转化为
转化为 ,并将Al、Si氧化物转化为可溶性钠盐。
,并将Al、Si氧化物转化为可溶性钠盐。
(1)与基态铬原子的最外层电子数相同且同周期的元素有_________ 种。
(2)为了提高“焙烧”效果,可采取的一种措施是____________ 。
(3)“浸取”所得的滤渣为 由此推断
由此推断 “焙烧”时发生主要反应的化学方程式为
“焙烧”时发生主要反应的化学方程式为________ 。
(4)常温下,矿物中相关元素可溶性组分物质的量浓度的对数[ ]与pH的关系如图所示。当溶液中可溶性组分浓度
]与pH的关系如图所示。当溶液中可溶性组分浓度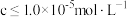 时,可认为已除尽。则“中和”时pH的理论范围为
时,可认为已除尽。则“中和”时pH的理论范围为________ ;“酸化”过程中的离子方程式为____________ 。 的酸性废水,用金属铁作阳极、石墨作阴极,一段时间后产生
的酸性废水,用金属铁作阳极、石墨作阴极,一段时间后产生 和
和 沉淀。
沉淀。
①若电解后溶液中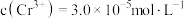 ,则
,则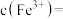
__________  {已知
{已知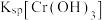
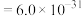 ,
,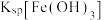 可从第(4)小题图中计算得出}。
可从第(4)小题图中计算得出}。
②电解法处理含 的酸性废水,下列有关原理的说法正确的是
的酸性废水,下列有关原理的说法正确的是_________ (填标号)。
A.阳极反应为
B.电解过程中溶液pH不会变化
C.如果石墨作阳极,电解过程不变
D.电路中每转移12mol电子,阳极有1mol 被还原
被还原
 )的工艺流程如下图。已知:①
)的工艺流程如下图。已知:① 中Cr的化合价为+3;②焙烧的目的是将
中Cr的化合价为+3;②焙烧的目的是将 转化为
转化为 ,并将Al、Si氧化物转化为可溶性钠盐。
,并将Al、Si氧化物转化为可溶性钠盐。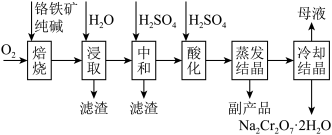
(1)与基态铬原子的最外层电子数相同且同周期的元素有
(2)为了提高“焙烧”效果,可采取的一种措施是
(3)“浸取”所得的滤渣为
 由此推断
由此推断 “焙烧”时发生主要反应的化学方程式为
“焙烧”时发生主要反应的化学方程式为(4)常温下,矿物中相关元素可溶性组分物质的量浓度的对数[
 ]与pH的关系如图所示。当溶液中可溶性组分浓度
]与pH的关系如图所示。当溶液中可溶性组分浓度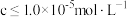 时,可认为已除尽。则“中和”时pH的理论范围为
时,可认为已除尽。则“中和”时pH的理论范围为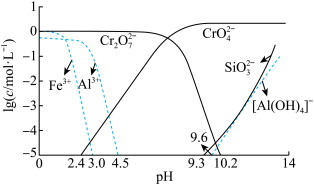
 的酸性废水,用金属铁作阳极、石墨作阴极,一段时间后产生
的酸性废水,用金属铁作阳极、石墨作阴极,一段时间后产生 和
和 沉淀。
沉淀。①若电解后溶液中
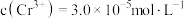 ,则
,则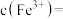
 {已知
{已知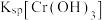
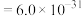 ,
,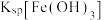 可从第(4)小题图中计算得出}。
可从第(4)小题图中计算得出}。②电解法处理含
 的酸性废水,下列有关原理的说法正确的是
的酸性废水,下列有关原理的说法正确的是A.阳极反应为

B.电解过程中溶液pH不会变化
C.如果石墨作阳极,电解过程不变
D.电路中每转移12mol电子,阳极有1mol
 被还原
被还原
您最近一年使用:0次
6 .  难溶于水,25℃时,不同
难溶于水,25℃时,不同 的溶液中含铅物种存在以下平衡:
的溶液中含铅物种存在以下平衡:
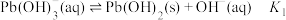 ;
;
 ;
;
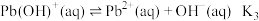 。
。
如图是溶液中各含铅物种的 图。下列说法错误的是
图。下列说法错误的是
 难溶于水,25℃时,不同
难溶于水,25℃时,不同 的溶液中含铅物种存在以下平衡:
的溶液中含铅物种存在以下平衡: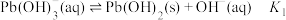 ;
; ;
;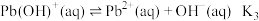 。
。如图是溶液中各含铅物种的
 图。下列说法错误的是
图。下列说法错误的是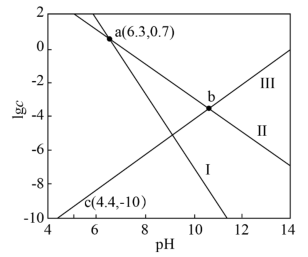
A.直线I和Ⅲ分别表示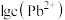 与 与 与 与 的变化关系 的变化关系 |
B. 的平衡常数K的数量级是 的平衡常数K的数量级是 |
C. 饱和溶液的 饱和溶液的 |
D.b点对应溶液的 为10.7 为10.7 |
您最近一年使用:0次
7日内更新
|
161次组卷
|
2卷引用:湖南省长沙市一中2024届高三下学期高考适应性演练(三)化学试题
7 . 在20℃时,用0.5
 溶液滴定25mL 0.25
溶液滴定25mL 0.25
 溶液,加入的
溶液,加入的 溶液体积与溶液pH变化曲线如图所示,其中
溶液体积与溶液pH变化曲线如图所示,其中 时溶液中无沉淀,之后出现白色浑浊且逐渐增多,当滴加的
时溶液中无沉淀,之后出现白色浑浊且逐渐增多,当滴加的 溶液体积为25.00mL时,溶液的pH稳定在7.20左右,整个滴定过程中未见气泡产生。下列叙述正确的是
溶液体积为25.00mL时,溶液的pH稳定在7.20左右,整个滴定过程中未见气泡产生。下列叙述正确的是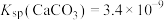 ,
,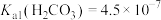 ,
,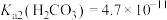 。
。

 溶液滴定25mL 0.25
溶液滴定25mL 0.25
 溶液,加入的
溶液,加入的 溶液体积与溶液pH变化曲线如图所示,其中
溶液体积与溶液pH变化曲线如图所示,其中 时溶液中无沉淀,之后出现白色浑浊且逐渐增多,当滴加的
时溶液中无沉淀,之后出现白色浑浊且逐渐增多,当滴加的 溶液体积为25.00mL时,溶液的pH稳定在7.20左右,整个滴定过程中未见气泡产生。下列叙述正确的是
溶液体积为25.00mL时,溶液的pH稳定在7.20左右,整个滴定过程中未见气泡产生。下列叙述正确的是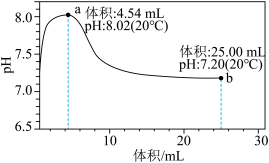
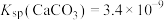 ,
,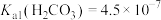 ,
,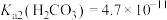 。
。A.a点的混合溶液: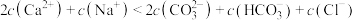 |
| B.a→b的过程中,水的电离程度不断增大 |
C.总反应的化学方程式: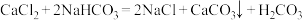 |
D.b点的混合溶液,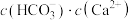 的数量级为 的数量级为 |
您最近一年使用:0次
名校
8 . 铊(Tl)广泛用于电子、军工、航天、化工、治金、通讯等方面,一种以红铊矿(主要成分是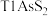 ,含少量
,含少量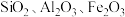 ,等杂质)为原料制备金属铊的流程如图所示。
,等杂质)为原料制备金属铊的流程如图所示。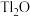 )膜,而失去金属光泽变得灰暗。
)膜,而失去金属光泽变得灰暗。
②TlCl难溶于水,而 溶于水。
溶于水。
③溶液中金属离子开始沉淀和完全沉淀的 如下表所示:
如下表所示:
回答下列问题:
(1) 中三元素的基态原子含有未成对电子数最多的元素是
中三元素的基态原子含有未成对电子数最多的元素是_______ 。(填元素符号)
(2)“焙烧1”中, 最终转化为
最终转化为 ﹔
﹔ 和
和 也转化为相应的硫酸盐。其中,
也转化为相应的硫酸盐。其中, 转化为
转化为 分如下两步完成。请写出第二步反应的化学方程式。
分如下两步完成。请写出第二步反应的化学方程式。
第一步( 与
与 反应):
反应):
第二步:_______ 。
(3)滤渣的成分 属于共价晶体,晶体中每个最小环含有
属于共价晶体,晶体中每个最小环含有_______ 个原子。
(4)“沉铊”步骤中,需要加入过量 ,其原因是
,其原因是_______ 。(用化学用语和简要的文字解释)
(5)向“沉铊”后的滤液中加入生石灰至 时才能外排,此时滤液中的
时才能外排,此时滤液中的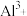 浓度为
浓度为_______  。(指数允许是小数)
。(指数允许是小数)
(6)“焙烧2”中发生的反应为 。则“置换”步骤中发生反应的离子方程式为
。则“置换”步骤中发生反应的离子方程式为_______ 。
(7)所得产品高纯铊应保存在_______ 中。
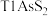 ,含少量
,含少量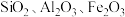 ,等杂质)为原料制备金属铊的流程如图所示。
,等杂质)为原料制备金属铊的流程如图所示。
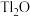 )膜,而失去金属光泽变得灰暗。
)膜,而失去金属光泽变得灰暗。②TlCl难溶于水,而
 溶于水。
溶于水。③溶液中金属离子开始沉淀和完全沉淀的
 如下表所示:
如下表所示:| 金属离子 |  |  |
开始沉淀的 | 2.2 | 3.5 |
沉淀完全( )的 )的 | 3.2 | 4.7 |
(1)
 中三元素的基态原子含有未成对电子数最多的元素是
中三元素的基态原子含有未成对电子数最多的元素是(2)“焙烧1”中,
 最终转化为
最终转化为 ﹔
﹔ 和
和 也转化为相应的硫酸盐。其中,
也转化为相应的硫酸盐。其中, 转化为
转化为 分如下两步完成。请写出第二步反应的化学方程式。
分如下两步完成。请写出第二步反应的化学方程式。第一步(
 与
与 反应):
反应):
第二步:
(3)滤渣的成分
 属于共价晶体,晶体中每个最小环含有
属于共价晶体,晶体中每个最小环含有(4)“沉铊”步骤中,需要加入过量
 ,其原因是
,其原因是(5)向“沉铊”后的滤液中加入生石灰至
 时才能外排,此时滤液中的
时才能外排,此时滤液中的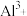 浓度为
浓度为 。(指数允许是小数)
。(指数允许是小数)(6)“焙烧2”中发生的反应为
 。则“置换”步骤中发生反应的离子方程式为
。则“置换”步骤中发生反应的离子方程式为(7)所得产品高纯铊应保存在
您最近一年使用:0次
名校
9 . 湖南稀土资源丰富,其中红土钪矿富含钪元素。钪及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广泛的应用。从红土钪矿(含钪、钛、铁、锰等元素)中提取氧化钪( )的一种流程如下:
)的一种流程如下: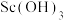 为两性氢氧化物,可与强碱反应生成
为两性氢氧化物,可与强碱反应生成 。
。
②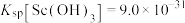 。
。
③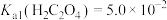 ,
,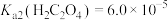 。
。
(1)为提高酸浸速率,可通过研磨、___________ 等措施(举2例)。请从原子结构的角度解释加入双氧水易将酸浸液中某种金属阳离子氧化的原因:___________ 。该步骤中选用足量的 ,理由是
,理由是___________ 。
(2)25℃时加入NaOH溶液调节 以除去
以除去 ,沉锰过程中钪也会经历沉淀的过程,
,沉锰过程中钪也会经历沉淀的过程, 完全沉淀的
完全沉淀的
___________ (已知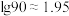 )。
)。
(3)向含 的溶液中加入草酸后可以将其沉淀,
的溶液中加入草酸后可以将其沉淀, 的草酸溶液中
的草酸溶液中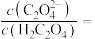
___________ 。
(4)草酸钪在空气中灼烧的化学方程式为___________ 。
(5)Y、Sc(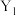 /NC,
/NC,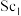 /NC)单原子催化剂可用于常温常压下的电化学催化氢气还原氮气的反应。反应历程与相对能量模拟计算结果如图所示(*表示稀土单原子催化剂)。使用
/NC)单原子催化剂可用于常温常压下的电化学催化氢气还原氮气的反应。反应历程与相对能量模拟计算结果如图所示(*表示稀土单原子催化剂)。使用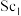 /NC单原子催化剂的反应历程中,决速步的方程式为
/NC单原子催化剂的反应历程中,决速步的方程式为___________ 。
 )的一种流程如下:
)的一种流程如下:
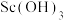 为两性氢氧化物,可与强碱反应生成
为两性氢氧化物,可与强碱反应生成 。
。②
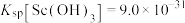 。
。③
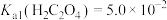 ,
,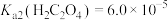 。
。(1)为提高酸浸速率,可通过研磨、
 ,理由是
,理由是(2)25℃时加入NaOH溶液调节
 以除去
以除去 ,沉锰过程中钪也会经历沉淀的过程,
,沉锰过程中钪也会经历沉淀的过程, 完全沉淀的
完全沉淀的
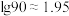 )。
)。(3)向含
 的溶液中加入草酸后可以将其沉淀,
的溶液中加入草酸后可以将其沉淀, 的草酸溶液中
的草酸溶液中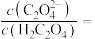
(4)草酸钪在空气中灼烧的化学方程式为
(5)Y、Sc(
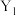 /NC,
/NC,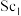 /NC)单原子催化剂可用于常温常压下的电化学催化氢气还原氮气的反应。反应历程与相对能量模拟计算结果如图所示(*表示稀土单原子催化剂)。使用
/NC)单原子催化剂可用于常温常压下的电化学催化氢气还原氮气的反应。反应历程与相对能量模拟计算结果如图所示(*表示稀土单原子催化剂)。使用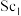 /NC单原子催化剂的反应历程中,决速步的方程式为
/NC单原子催化剂的反应历程中,决速步的方程式为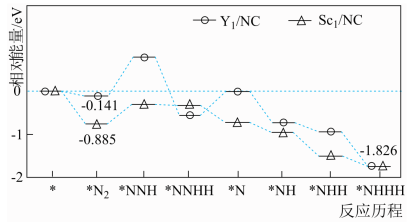
您最近一年使用:0次
名校
10 . 工业上以精炼铜的阳极泥为原料(主要成分为Se、CuSe、 等)回收Se。
等)回收Se。 和
和 ,被水吸收时发生反应。
,被水吸收时发生反应。
②Se难溶于水,沸点684.9℃,易与 反应。
反应。
③反应的 ,代表可完全转化。室温下
,代表可完全转化。室温下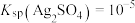 ,
,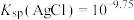 。
。
下列说法正确的是
 等)回收Se。
等)回收Se。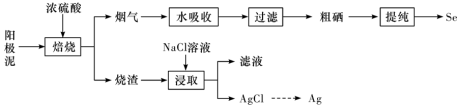
 和
和 ,被水吸收时发生反应。
,被水吸收时发生反应。②Se难溶于水,沸点684.9℃,易与
 反应。
反应。③反应的
 ,代表可完全转化。室温下
,代表可完全转化。室温下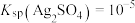 ,
,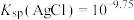 。
。下列说法正确的是
A.理论上,发生反应的 和 和 的物质的量之比为1∶2 的物质的量之比为1∶2 |
| B.在真空中可进行粗硒提纯,可降低体系中硒的沸点 |
C.“滤液”为 溶液 溶液 |
D.加入NaCl溶液浸取时发生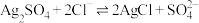 ,该反应过程不可完全转化 ,该反应过程不可完全转化 |
您最近一年使用:0次



