25℃时,将含有I-的溶液逐滴加入到含有Hg2+的溶液中,发生一系列可逆反应生成HgI+、HgI2(s)、 、
、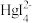 。其中,Hg2+、HgI+、
。其中,Hg2+、HgI+、 、
、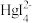 四种离子浓度的对数lgc与I-浓度的对数lgc(I-)关系如图所示(图中虚线及虚线的上方是HgI2的沉淀区)。下列说法正确的是
四种离子浓度的对数lgc与I-浓度的对数lgc(I-)关系如图所示(图中虚线及虚线的上方是HgI2的沉淀区)。下列说法正确的是
 、
、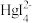 。其中,Hg2+、HgI+、
。其中,Hg2+、HgI+、 、
、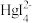 四种离子浓度的对数lgc与I-浓度的对数lgc(I-)关系如图所示(图中虚线及虚线的上方是HgI2的沉淀区)。下列说法正确的是
四种离子浓度的对数lgc与I-浓度的对数lgc(I-)关系如图所示(图中虚线及虚线的上方是HgI2的沉淀区)。下列说法正确的是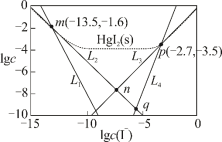
| A.Ksp(HgI2)的数量级为10-28 |
| B.n点的坐标为(-7.15,-7.95) |
C.反应 (aq) (aq) HgI2(s)+I-(aq)的平衡常数为K=10-0.8 HgI2(s)+I-(aq)的平衡常数为K=10-0.8 |
D.q点溶液中存在:c(H+)+2c(Hg2+)=c(OH-)+c(I-)+c(HgI )+c(HgI )+c(HgI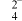 ) ) |
更新时间:2024-05-29 22:56:11
|
相似题推荐
多选题
|
较难
(0.4)
名校
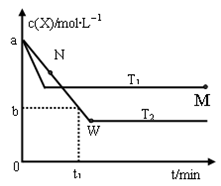
【推荐1】在恒容密闭容器中通入X并发生反应:2X(g) Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是
Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是
 Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是
Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是
| A.该反应进行到M点放出的热量大于进行到W点放出的热量 |
B.T2下,在0~t1时间内,υ(Y)=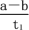 mol/(L·min) mol/(L·min) |
| C.M点的正反应速率υ正大于N点的逆反应速率υ逆 |
| D.M点时再加入一定量的X,平衡后X的转化率增大 |
您最近一年使用:0次
【推荐2】一定温度下,向2L恒容容器中充入 A和
A和 B,发生反应
B,发生反应 ,经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确的是
,经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确的是
 A和
A和 B,发生反应
B,发生反应 ,经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确的是
,经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确的是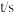 | 0 | 5 | 15 | 25 | 35 |
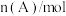 | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
A.前5s的平均反应速率 |
| B.由题目信息可知,正反应为放热反应 |
C.保持温度不变,起始时向容器中充入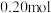 A、 A、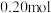 B和 B和 C,反应达平衡前 C,反应达平衡前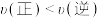 |
D.保持温度不变,起始时向容器中充入 C,达平衡时,C的转化率等于80% C,达平衡时,C的转化率等于80% |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐1】反应 N2O4(g)  2NO2(g) ΔH>0,经常用于研究化学平衡问题。在温度为360.8K下有甲、乙两个密闭容器,甲维持外压恒定为300kPa,乙保持容积恒定为1L。现向甲、乙各充入1mol N2O4气体,反应达到平衡时甲中N2O4的转化率为20%。已知360.8K、300kPa时气体的摩尔体积为10L/mol。下列说法正确的是
2NO2(g) ΔH>0,经常用于研究化学平衡问题。在温度为360.8K下有甲、乙两个密闭容器,甲维持外压恒定为300kPa,乙保持容积恒定为1L。现向甲、乙各充入1mol N2O4气体,反应达到平衡时甲中N2O4的转化率为20%。已知360.8K、300kPa时气体的摩尔体积为10L/mol。下列说法正确的是
 2NO2(g) ΔH>0,经常用于研究化学平衡问题。在温度为360.8K下有甲、乙两个密闭容器,甲维持外压恒定为300kPa,乙保持容积恒定为1L。现向甲、乙各充入1mol N2O4气体,反应达到平衡时甲中N2O4的转化率为20%。已知360.8K、300kPa时气体的摩尔体积为10L/mol。下列说法正确的是
2NO2(g) ΔH>0,经常用于研究化学平衡问题。在温度为360.8K下有甲、乙两个密闭容器,甲维持外压恒定为300kPa,乙保持容积恒定为1L。现向甲、乙各充入1mol N2O4气体,反应达到平衡时甲中N2O4的转化率为20%。已知360.8K、300kPa时气体的摩尔体积为10L/mol。下列说法正确的是A.360.8K时,该反应的Kc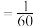 |
| B.若向平衡后的甲中再充入1mol N2O4气体,重新平衡后N2O4的体积分数与原平衡相比将增加 |
| C.若有绝热、容积恒定为1L的容器丙,起始温度为360.8K。向丙中充入1mol N2O4气体,达平衡时N2O4的平衡转化率α丙<α乙 |
D.平衡时乙容器中c(NO2)= mol/L mol/L |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐2】有Ⅰ~Ⅳ四个体积均为0.5 L的恒容密闭容器,在Ⅰ、Ⅱ、Ⅲ中按不同投料比(Z)充入HCl和O2(如下表),加入催化剂发生反应4HCl(g)+O2(g) 2Cl2(g)+2H2O(g);ΔH,HCl的平衡转化率(α)与Z和温度(t)的关系如图所示。下列说法正确的是( )
2Cl2(g)+2H2O(g);ΔH,HCl的平衡转化率(α)与Z和温度(t)的关系如图所示。下列说法正确的是( )

 2Cl2(g)+2H2O(g);ΔH,HCl的平衡转化率(α)与Z和温度(t)的关系如图所示。下列说法正确的是( )
2Cl2(g)+2H2O(g);ΔH,HCl的平衡转化率(α)与Z和温度(t)的关系如图所示。下列说法正确的是( )| 容器 | 起始时 | ||
| t/℃ | n(HCl)/mol | Z | |
| Ⅰ | 300 | 0.25 | a |
| Ⅱ | 300 | 0.25 | b |
| Ⅲ | 300 | 0.25 | 4 |

| A.ΔH<0,a<4<b |
| B.300℃该反应的平衡常数的值为64 |
| C.容器Ⅲ某时刻处在R点,则R点的υ正>υ逆,压强:p(R)>p(Q) |
| D.若起始时,在容器Ⅳ中充入0.25molCl2和0.25molH2O(g),300℃达平衡时容器中c(HCl)=0.1mol·L-1 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐1】已知25℃,某一元酸Ka(HA)=1.75 ,向20mL0.5mol·L-1的HA溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如下图所示。下列关于混合溶液的相关说法中正确的是
,向20mL0.5mol·L-1的HA溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如下图所示。下列关于混合溶液的相关说法中正确的是

 ,向20mL0.5mol·L-1的HA溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如下图所示。下列关于混合溶液的相关说法中正确的是
,向20mL0.5mol·L-1的HA溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如下图所示。下列关于混合溶液的相关说法中正确的是
| A.HA的电离平衡常数:B点<A点 |
| B.由水电离出的c(OH-):B点>C点 |
| C.从A点到B点,混合溶液中可能存在:c(A-)=c(Na+) |
| D.从B点到C点,混合溶液中一直存在:c(Na+)>c(A-)>c(OH-)>c(H+) |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐2】已知25℃时有关弱酸的电离平衡常数
则下列有关说法不正确的是( )
| 弱酸 | 氢氟酸 | 硼酸[B(OH)3](一元酸) | 草酸(H2C2O4) |
| 电离平衡常数(25℃) | 6.6×10-4 | 5.8×10-10 | K1=5.9×10-2 K2=6.4×10-5 |
| A.硼酸为一元弱酸 |
| B.amol·L-1 HF溶液与b mol·L-1 NaOH溶液等体积混合后,所得溶液中c(Na+)>c(F-),则b一定大于a |
| C.同温下,NaHC2O4溶液中HC2O4-的电离常数大于K2(草酸的二级电离) |
| D.NaHC2O4和Na2C2O4混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-) |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐1】机车车辆配件制造过程中,为了增加配件耐腐蚀能力,要使用盐酸浸透除锈。某研究所加入屏蔽剂后使用乙基紫(变色范围 )为指示剂采取酸碱滴定的方法滴定并计算酸洗废液中的盐酸浓度,所得滴定曲线如图所示。下列说法正确的是
)为指示剂采取酸碱滴定的方法滴定并计算酸洗废液中的盐酸浓度,所得滴定曲线如图所示。下列说法正确的是
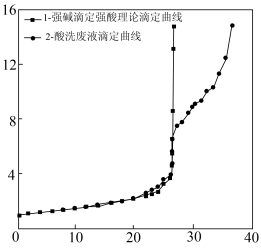
 )为指示剂采取酸碱滴定的方法滴定并计算酸洗废液中的盐酸浓度,所得滴定曲线如图所示。下列说法正确的是
)为指示剂采取酸碱滴定的方法滴定并计算酸洗废液中的盐酸浓度,所得滴定曲线如图所示。下列说法正确的是
A.酸洗废液中的主要杂质离子为 和 和 |
B.若酸洗废液中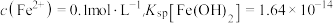 ,理论上无需屏蔽 ,理论上无需屏蔽 |
| C.滴定过程中,眼睛要紧盯滴定管的刻度变化 |
| D.图中两条曲线不能完全重合,故该方法不能达到实验目的 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
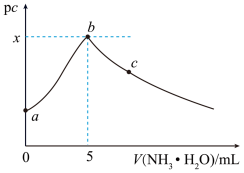
【推荐2】常温下,向 一定浓度的硫酸铜溶液中逐滴滴入
一定浓度的硫酸铜溶液中逐滴滴入 的氨水,首先析出浅蓝色的
的氨水,首先析出浅蓝色的 沉淀,氨水过量时此沉淀溶解,形成
沉淀,氨水过量时此沉淀溶解,形成 络离子(假定溶液混合后体积不变)。滴加过程中
络离子(假定溶液混合后体积不变)。滴加过程中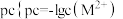 ,
, 为
为 或
或 与氨水体积的关系如图所示。下列说法错误的是
与氨水体积的关系如图所示。下列说法错误的是
 一定浓度的硫酸铜溶液中逐滴滴入
一定浓度的硫酸铜溶液中逐滴滴入 的氨水,首先析出浅蓝色的
的氨水,首先析出浅蓝色的 沉淀,氨水过量时此沉淀溶解,形成
沉淀,氨水过量时此沉淀溶解,形成 络离子(假定溶液混合后体积不变)。滴加过程中
络离子(假定溶液混合后体积不变)。滴加过程中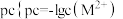 ,
, 为
为 或
或 与氨水体积的关系如图所示。下列说法错误的是
与氨水体积的关系如图所示。下列说法错误的是
A.硫酸铜溶液的浓度为 |
B.常温下, 点溶液中水的电离程度低于纯水的 点溶液中水的电离程度低于纯水的 |
C. 点溶液中存在 点溶液中存在 |
D.常温下,忽略 的影响,可得 的影响,可得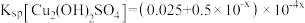 |
您最近一年使用:0次

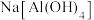 溶液中滴入
溶液中滴入 溶液
溶液 比
比 结合质子能力强
结合质子能力强 悬浊液中加入适量
悬浊液中加入适量 固体
固体 溶液和淀粉
溶液和淀粉 溶液
溶液 气体的容器
气体的容器 的方向移动
的方向移动 2NH3(g)。按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
2NH3(g)。按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
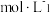 )表示CaF2的溶解度。
)表示CaF2的溶解度。
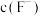 +c(HF)
+c(HF) ,则水中S(CaF2)=
,则水中S(CaF2)= 

 时,用
时,用 溶液分别滴定
溶液分别滴定 三种溶液,
三种溶液, [p表示负对数,M表示
[p表示负对数,M表示 ]随
]随 变化关系如图所示,已知
变化关系如图所示,已知 ,一般认为当溶液中离子浓度
,一般认为当溶液中离子浓度 时,该离子沉淀完全。下列有关分析正确的是
时,该离子沉淀完全。下列有关分析正确的是 
 溶液的变化关系
溶液的变化关系 溶液至a点时,溶液中
溶液至a点时,溶液中
 时,溶液中:
时,溶液中:



