名校
解题方法
1 . 已知水的电离平衡曲线如图所示:
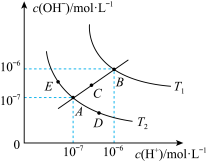
试回答下列问题:
(1)图中
_______  (用“>”、“<”、“=”回答)
(用“>”、“<”、“=”回答)
(2)图中五点的 间的关系是
间的关系是_______ 。
(3)若从A点到E点,可采用的措施是_______ 。
a.升温 b.加入少量的盐酸 c.加入少量的NaOH溶液
(4)点E对应的温度下,将 的NaOH溶液与
的NaOH溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则NaOH溶液与
,则NaOH溶液与 溶液的体积比为
溶液的体积比为_______ 。
(5)点B对应的温度下,若100体积 的某强酸溶液与1体积
的某强酸溶液与1体积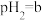 的某强碱溶液混合后溶液呈中性,则混合前,该强酸的
的某强碱溶液混合后溶液呈中性,则混合前,该强酸的 与强碱的
与强碱的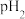 之间应满足的关系是
之间应满足的关系是_______ 。
(6)写出用pH试纸测溶液pH的操作_______ 。

试回答下列问题:
(1)图中

 (用“>”、“<”、“=”回答)
(用“>”、“<”、“=”回答)(2)图中五点的
 间的关系是
间的关系是(3)若从A点到E点,可采用的措施是
a.升温 b.加入少量的盐酸 c.加入少量的NaOH溶液
(4)点E对应的温度下,将
 的NaOH溶液与
的NaOH溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则NaOH溶液与
,则NaOH溶液与 溶液的体积比为
溶液的体积比为(5)点B对应的温度下,若100体积
 的某强酸溶液与1体积
的某强酸溶液与1体积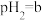 的某强碱溶液混合后溶液呈中性,则混合前,该强酸的
的某强碱溶液混合后溶液呈中性,则混合前,该强酸的 与强碱的
与强碱的 之间应满足的关系是
之间应满足的关系是(6)写出用pH试纸测溶液pH的操作
您最近一年使用:0次
2022-11-10更新
|
345次组卷
|
3卷引用:江苏省常熟市王淦昌高级中学2022-2023学年高二3月月考化学试题
名校
解题方法
2 . 盐在化学工业中有重要的应用,请回答下列问题。
(1)用离子方程式表示明矾可作净水剂的原因:_______ 。
(2)常温下,在pH=3的硫酸与pH=11的Na2S溶液中,水电离出来的c(OH-)之比为_______ 。
(3)物质的量浓度相等的下列溶液①NH4Cl;②NH4HSO4;③(NH4)2SO4;④CH3COONH4;⑤NH3·H2O,溶液中的pH由大到小的顺序是_______ (用序号表示)
(4)25℃,两种酸的电离平衡常数如下表:
①0.10mol/L NaHSO3溶液中离子浓度由大到小的顺序为_______ ;
②向Na2S溶液中通入足量二氧化硫时反应的离子方程式_______ 。
③向NaHS溶液中通入少量CO2时反应的离子方程式_______ 。
(1)用离子方程式表示明矾可作净水剂的原因:
(2)常温下,在pH=3的硫酸与pH=11的Na2S溶液中,水电离出来的c(OH-)之比为
(3)物质的量浓度相等的下列溶液①NH4Cl;②NH4HSO4;③(NH4)2SO4;④CH3COONH4;⑤NH3·H2O,溶液中的pH由大到小的顺序是
(4)25℃,两种酸的电离平衡常数如下表:
| H2SO3 | H2CO3 | H2S | |
| Ka1 | 1.3×10-2 | 4.2×10-7 | 1.9×10-8 |
| Ka2 | 6.3×10-8 | 5.6×10-11 | 1.0×10-12 |
①0.10mol/L NaHSO3溶液中离子浓度由大到小的顺序为
②向Na2S溶液中通入足量二氧化硫时反应的离子方程式
③向NaHS溶液中通入少量CO2时反应的离子方程式
您最近一年使用:0次
解题方法
3 . 25℃时,下列各组离子在指定溶液中一定能大量共存的是
A.由水电离产生的c(H+)=1×10-13mol·L-1的溶液中:Na+、Ba2+、NO 、Cl- 、Cl- |
B.在含有大量HCO 的溶液中:Na+、NO 的溶液中:Na+、NO 、Cl-、AlO 、Cl-、AlO |
C.1.0 mol·L-1的HNO3溶液中:K+、[Ag(NH3)2]+、Cl-、SO |
| D. 0.1mol·L-1的Fe(NO3)2溶液中:Na+、H+、SCN-、Cl- |
您最近一年使用:0次
4 . 应用化学反应原理知识解决下列问题
(1)写出醋酸(CH3COOH) 的电离方程式:_____________ 。
(2)明矾净水的原理为(用离子方程式表示)____________________________ 。
(3)一定条件下,56g金属铁与足量CO2气体完全反应生成碳单质和氧化铁固体时,放出117kJ热量,该反应的热化学方程式为_______________________ 。
(4)现有浓度为0.1mol/L 的三种电解质溶液①NaHCO3 ②Na2CO3 ③NaOH 这三种溶液的pH 由小到大的顺序是__________________ (填编号)。
(5)常温下,下列事实能证明HA是弱电解质的是________ (填编号)。
a.某NaA溶液的pH=9
b.用HA 溶液做导电实验,灯泡很暗
c.等物质的量浓度、等体积的硫酸和HA溶液分别与足量锌反应,硫酸产生的氢气多d.0.1mol/LHA 溶液的pH≈2.8
(6)已知在100℃时,水的离子积为1×10-12,此时将 pH= 11 的 NaOH 溶液V1 L 与pH=2的H2SO4溶液V2 L均匀混合后,若所得混合溶液的pH=10,则V1: V2为______ 。
(1)写出醋酸(CH3COOH) 的电离方程式:
(2)明矾净水的原理为(用离子方程式表示)
(3)一定条件下,56g金属铁与足量CO2气体完全反应生成碳单质和氧化铁固体时,放出117kJ热量,该反应的热化学方程式为
(4)现有浓度为0.1mol/L 的三种电解质溶液①NaHCO3 ②Na2CO3 ③NaOH 这三种溶液的pH 由小到大的顺序是
(5)常温下,下列事实能证明HA是弱电解质的是
a.某NaA溶液的pH=9
b.用HA 溶液做导电实验,灯泡很暗
c.等物质的量浓度、等体积的硫酸和HA溶液分别与足量锌反应,硫酸产生的氢气多d.0.1mol/LHA 溶液的pH≈2.8
(6)已知在100℃时,水的离子积为1×10-12,此时将 pH= 11 的 NaOH 溶液V1 L 与pH=2的H2SO4溶液V2 L均匀混合后,若所得混合溶液的pH=10,则V1: V2为
您最近一年使用:0次
10-11高一·江苏泰州·期中
5 . (1)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。请把与下面元素有关性质相符的曲线标号(a、b、c、d)填入相应的空格中:
①ⅡA族元素的最外层电子数_____ ; ②第3周期元素的最高化合价____ ;
③F-、 Na+ 、Mg2+、Al3+的离子半径___ ;

(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M原子的最外层电子数与次外电子数之比为3∶4;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,据此回答:
①Y和M形成的常见化合物的化学式是________________________ 。
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1∶1∶1,若A能抑制水的电离,B能促进水的电离,则化合物A的化学式为_________ ,B的化学式是_______ 。
③Z与Y形成的稳定化合物的电子式为__________ 。
④X与Y、X与M均可形成18电子分子,写出这两种分子在水溶液中反应生成M单质的化学方程式:________________________________ ;该反应中转移的电子数目为______ 。
①ⅡA族元素的最外层电子数
③F-、 Na+ 、Mg2+、Al3+的离子半径

(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M原子的最外层电子数与次外电子数之比为3∶4;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,据此回答:
①Y和M形成的常见化合物的化学式是
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1∶1∶1,若A能抑制水的电离,B能促进水的电离,则化合物A的化学式为
③Z与Y形成的稳定化合物的电子式为
④X与Y、X与M均可形成18电子分子,写出这两种分子在水溶液中反应生成M单质的化学方程式:
您最近一年使用:0次



