名校
1 . 下列图示与对应的叙述相符的是
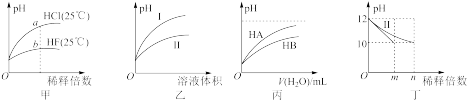

| A.由图甲可知,a点Kw的数值比b点Kw的数值大 |
| B.图乙表示用水稀释pH相同的盐酸和醋酸,I表示醋酸,II表示盐酸 |
| C.图丙表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同浓度时NaA溶液的pH小于同浓度的NaB溶液的pH |
| D.图丁表示分别稀释10mLpH均为12的NaOH溶液和氨水时pH的变化,曲线I表示氨水,n>100 |
您最近一年使用:0次
2021-09-16更新
|
558次组卷
|
8卷引用:黑龙江省双鸭山市第一中学2021-2022学年高二上学期期中考试化学试题
黑龙江省双鸭山市第一中学2021-2022学年高二上学期期中考试化学试题黑龙江省大兴安岭呼玛县高级中学2021-2022学年高二上学期期末考试化学试题河北正定中学2020-2021学年高二上学期第一次半月考化学试题(已下线)必考点07 盐类的水解-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)(已下线)3.3.1 盐类水解的原理-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)山东省淄博市高青县第一中学2021-2022学年高二上学期期中考试化学试题江西省吉安市遂川中学2021-2022学年高二上学期第三次月考(B)化学试题安徽省合肥市肥东县综合高中2021-2022学年高二下学期5月月考化学试题
名校
解题方法
2 . 下列说法正确的是
| A.常温下,pH=2的HCl溶液中水电离的H+浓度为0.01 mol/L |
| B.0.1 mol/L 醋酸溶液中c(H+) + c(CH3COO-) + c(CH3COOH)= 0.1 mol/L |
| C.已知0.1 mol/L KHC2O4溶液呈酸性,则该溶液中存在如下关系:c(K+) >c(HC2O4-)> c(H2C2O4) >c(C2O42-) |
| D.在Na2CO3溶液中存在如下守恒关系:c(H+)-c(HCO3-)-2c(H2CO3) = c(OH-) |
您最近一年使用:0次
名校
解题方法
3 . 请回答下列问题。
(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度。
①100℃时1 mol·L-1的NaOH溶液中,由水电离出的c(H+)=______ mol·L-1,Kw(25℃)________ Kw(100℃) (填“>”、“<”或“=”)。
②25℃时,向水的电离平衡体系中加入少量 NH4Cl固体,对水的电离平衡的影响是_____ (填“促进”、“抑制”或“不影响”)。
(2)电离平衡常数是衡量弱电解质电离程度强弱的量。已知如表数据。
①25℃时,有等浓度的a.NaCN溶液 b.CH3COONa 溶液 c.Na2CO3溶液,三种溶液的pH由大到小的顺序为_____________________ ;(填序号)
②25℃时,等浓度的CH3COOH溶液和NaOH溶液等体积混合,则c(Na+)__________ c(CH3COO-)(填“>”、“<”或“=”);
(3)25℃,两种酸的电离平衡常数如下表。
①HSO3-的电离平衡常数表达式K=_________ 。
②H2SO3溶液和NaHCO3溶液反应的主要离子方程式为__________________ 。
(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度。

①100℃时1 mol·L-1的NaOH溶液中,由水电离出的c(H+)=
②25℃时,向水的电离平衡体系中加入少量 NH4Cl固体,对水的电离平衡的影响是
(2)电离平衡常数是衡量弱电解质电离程度强弱的量。已知如表数据。
| 化学式 | 电离平衡常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25℃时,有等浓度的a.NaCN溶液 b.CH3COONa 溶液 c.Na2CO3溶液,三种溶液的pH由大到小的顺序为
②25℃时,等浓度的CH3COOH溶液和NaOH溶液等体积混合,则c(Na+)
(3)25℃,两种酸的电离平衡常数如下表。
| Ka1 | Ka2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-4 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
①HSO3-的电离平衡常数表达式K=
②H2SO3溶液和NaHCO3溶液反应的主要离子方程式为
您最近一年使用:0次
2017-04-07更新
|
511次组卷
|
2卷引用:黑龙江省大庆市第四中学2019-2020学年高二上学期第三次月考化学试题
4 . 某校化学课外学习小组发现将镁粉按图投入纯水中现象不明显,而投入氯化铵溶液中,两者立即发生反应,产生大量气泡。经检验该过程产生两种气体,其中一种气体有刺激性气味。
(1)实验开始时用校准过的pH传感器测定纯水的pH,发现纯水的pH总是在7.30左右,其原因可能是_____________________
(2)请设计简单的实验方案检验上述实验中有刺激性气味的气体:__________________
(3)实验中0.2mol/L氯化铵溶液的pH为5.90,请用离子方程式解释原因:_________________
(4)该小组同学为探究镁与氯化铵溶液反应的原因设计了如下实验方案:
①上述探究实验1-2选用的盐酸为_____________ (填字母)。
A、1 mol·L-1 B、pH=1.0 C、0.2 mol·L-1 D、pH=5.90
②通过实验对比,说明NH4Cl 水解产生的H+ 对反应影响_____ NH4+ 对反应影响(填“小于”、“大于”或“等于”)。
(5)该小组同学继续探究镁粉与氯化铵溶液反应剧烈的影响因素。
①实验2-1与实验2-2中实验现象说明Cl-对反应速率的影响很小,请补充完成实验方案所需的试剂。
②实验3-1与实验3-2的结论说明NH4+对反应速率影响很大,则两支试管中实验现象的不同之处是___________________
(6)写出镁与氯化铵溶液反应生成Mg2+的离子方程式_______________ 。

(1)实验开始时用校准过的pH传感器测定纯水的pH,发现纯水的pH总是在7.30左右,其原因可能是
(2)请设计简单的实验方案检验上述实验中有刺激性气味的气体:
(3)实验中0.2mol/L氯化铵溶液的pH为5.90,请用离子方程式解释原因:
(4)该小组同学为探究镁与氯化铵溶液反应的原因设计了如下实验方案:
序号 | 实验试剂 | 实验现象 | |
实验1-1 | 0.20g镁粉 | 3.0mL 0.2mol/LNH4Cl溶液 | 反应明显,有气泡产生 |
实验1-2 | 0.20g镁粉 | 3.0mL盐酸 | 反应不明显,几乎没有气泡产生 |
①上述探究实验1-2选用的盐酸为
A、1 mol·L-1 B、pH=1.0 C、0.2 mol·L-1 D、pH=5.90
②通过实验对比,说明NH4Cl 水解产生的H+ 对反应影响
(5)该小组同学继续探究镁粉与氯化铵溶液反应剧烈的影响因素。
实验序号 | 实验试剂 | |
实验2-1 | 0.20g镁粉 | |
实验2-2 | 0.20g镁粉 | |
实验3-1 | 0.20g镁粉 | 3.0mL0.2mol/L NH4NO3溶液 |
实验3-2 | 0.20g镁粉 | 3.0mL0.2mol/L KNO3溶液 |
①实验2-1与实验2-2中实验现象说明Cl-对反应速率的影响很小,请补充完成实验方案所需的试剂。
②实验3-1与实验3-2的结论说明NH4+对反应速率影响很大,则两支试管中实验现象的不同之处是
(6)写出镁与氯化铵溶液反应生成Mg2+的离子方程式
您最近一年使用:0次
2017-03-17更新
|
536次组卷
|
2卷引用:2017届黑龙江省虎林市高级中学高三4月模拟理综化学试卷
名校
5 . 某温度(T ℃)下的溶液中,c(H+)=10-x mol·L-1,c(OH-)=10-y mol·L-1,x与y的关系如图所示,请回答下列问题:

(1)此温度下,水的离子积Kw为________ ,则该温度T______ 25(填“>”、“<”或“=”)。
(2)在此温度下,向Ba(OH)2溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH如表所示。
假设溶液混合前后的体积变化忽略不计,则a=________ ,实验②中由水电离产生的c(OH-)=______ mol·L-1。
(3)在此温度下,将0.1 mol·L-1的NaHSO4溶液与0.1 mol·L-1的Ba(OH)2溶液按下表中甲、乙、丙、丁不同方式混合:
①按丁方式混合后,所得溶液显________ (填“酸”、“碱”或“中”)性。
②写出按乙方式混合后,反应的离子方程式:________________________ 。
③按甲方式混合后,所得溶液的pH为__________ 。

(1)此温度下,水的离子积Kw为
(2)在此温度下,向Ba(OH)2溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH如表所示。
| 实验序号 | Ba(OH)2溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |
假设溶液混合前后的体积变化忽略不计,则a=
(3)在此温度下,将0.1 mol·L-1的NaHSO4溶液与0.1 mol·L-1的Ba(OH)2溶液按下表中甲、乙、丙、丁不同方式混合:
| 甲 | 乙 | 丙 | 丁 | |
| 0.1 mol·L-1 Ba(OH)2溶液体积/mL | 10 | 10 | 10 | 10 |
| 0.1 mol·L-1 NaHSO4溶液体积/mL | 5 | 10 | 15 | 20 |
①按丁方式混合后,所得溶液显
②写出按乙方式混合后,反应的离子方程式:
③按甲方式混合后,所得溶液的pH为
您最近一年使用:0次
2016-12-09更新
|
773次组卷
|
11卷引用:黑龙江省七台河市勃利县高级中学2021-2022学年高二上学期9月月考化学试题
黑龙江省七台河市勃利县高级中学2021-2022学年高二上学期9月月考化学试题2015-2016学年河北省邢台一中高二上第一次月考化学试卷2015-2016学年四川省成都市六校高二上学期期中联考化学试卷山东省枣庄市第八中学东校区2020-2021学年高二上学期第二次质量检测化学试题(已下线)第03章 水溶液中的离子反应与平衡(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第二节 水的电离和溶液的pH 课时2 溶液的酸碱性与pH湖北省巴东县第二高级中学2020-2021学年高二上学期期中考试化学试题选择性必修1(SJ)专题3第二单元课时1 溶液的酸碱性与pH选择性必修1 专题3 第二单元 课时1 溶液的酸碱性山西省怀仁市第一中学2021-2022学年高二上学期期中理科综合化学试题河北省石家庄市部分学校2023-2024学年高二上学期11月联考化学试题



