1 . 化学是一门实验的科学,滴定法是一种常用的化学定量分析的方法。室温下,用 溶液分别滴定体积均为20.00mL、浓度均为
溶液分别滴定体积均为20.00mL、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液的pH随加入NaOH溶液体积而变化的两条滴定曲线。
的盐酸和醋酸溶液,得到滴定过程中溶液的pH随加入NaOH溶液体积而变化的两条滴定曲线。
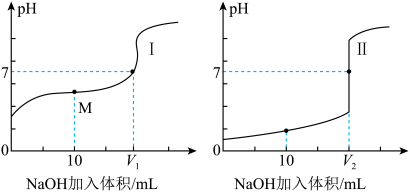
(1)滴定醋酸溶液的曲线是___________ 。(填“Ⅰ”或“Ⅱ”)。
(2)若采用氨水滴定醋酸,写出氨水与醋酸反应的离子反应方程式___________ 。
(3)滴定开始前,三种溶液中由水电离出的 最大的是
最大的是______ 。
A. 溶液 B.
溶液 B. 盐酸 C.
盐酸 C. 醋酸
醋酸
(4)该 溶液的pH为
溶液的pH为______ ;给该溶液加热,pH______ (填“变大”“变小”或“不变”)。
(5)在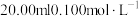 的盐酸中,滴加
的盐酸中,滴加 溶液后,此时溶液的pH=
溶液后,此时溶液的pH=___________ 。
(6)取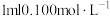 的盐酸稀释1000倍后,溶液pH=
的盐酸稀释1000倍后,溶液pH=___________ ,此时水电离出的 浓度为
浓度为___________ 。
(7)下列离子一定能大量共存的是___________。
(8)下列叙述正确的是___________。
(9)下列有关实验的说法,正确的是___________。
 溶液分别滴定体积均为20.00mL、浓度均为
溶液分别滴定体积均为20.00mL、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液的pH随加入NaOH溶液体积而变化的两条滴定曲线。
的盐酸和醋酸溶液,得到滴定过程中溶液的pH随加入NaOH溶液体积而变化的两条滴定曲线。
(1)滴定醋酸溶液的曲线是
(2)若采用氨水滴定醋酸,写出氨水与醋酸反应的离子反应方程式
(3)滴定开始前,三种溶液中由水电离出的
 最大的是
最大的是A.
 溶液 B.
溶液 B. 盐酸 C.
盐酸 C. 醋酸
醋酸(4)该
 溶液的pH为
溶液的pH为(5)在
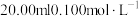 的盐酸中,滴加
的盐酸中,滴加 溶液后,此时溶液的pH=
溶液后,此时溶液的pH=(6)取
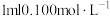 的盐酸稀释1000倍后,溶液pH=
的盐酸稀释1000倍后,溶液pH= 浓度为
浓度为(7)下列离子一定能大量共存的是___________。
A.甲基橙呈黄色的溶液中: 、 、 、 、 、 、 |
B.加入铝粉后产生大量氢气的溶液中: 、 、 、 、 、 、 |
C.石蕊呈蓝色的溶液中: 、 、 、 、 、 、 |
D.pH=1的溶液中: 、 、 、 、 、 、 |
(8)下列叙述正确的是___________。
A.无论是纯水,还是酸性、碱性或中性稀溶液,在常温下其 |
B.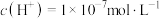 的溶液一定是中性溶液 的溶液一定是中性溶液 |
C.向水中加入少量固体 ,水的电离平衡逆向移动, ,水的电离平衡逆向移动, 减小 减小 |
D.将水加热, 增大,pH不变 增大,pH不变 |
(9)下列有关实验的说法,正确的是___________。
| A.测定HClO溶液pH时,用玻璃棒蘸取溶液,点在干燥pH试纸上 |
| B.等体积、等pH的硫酸与醋酸溶液分别与足量锌反应,醋酸产生的氢气多 |
| C.等体积、等浓度的盐酸和醋酸分别与相同大小的锌粒反应,醋酸初始反应速率快 |
| D.使用pH试纸测定溶液的pH时,若先润湿,则测得溶液的pH一定有误差 |
您最近一年使用:0次
名校
解题方法
2 . 化学是一门实验的科学,滴定法是化学上常用的定量分析的方法,有酸碱中和滴定、氧化还原滴定、沉淀滴定等。
I.酸碱中和滴定:常温下,用0.1000mol/LNaOH溶液分别滴定20.00mL等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:________ (填“1”或“2”),滴加2~3滴________ 作指示剂(填“甲基橙”或“酚酞”)。
(2)达到B、D状态时,反应消耗NaOH溶液的体积a___________b(填编号)。
(3)A、B、C、E四点水的电离程度由大到小顺序为:E>________ 。
(4)某次用氢氧化钠滴定未知浓度的醋酸的滴定结果如表所示:
________ mL。
(5)下列操作中造成第2次所测测定结果明显偏差的是___________。
Ⅱ.氧化还原滴定:
如测定血液中钙的含量时,进行如下实验:
i.可将amL血液用蒸馏水稀释后,向其中加入足量草酸铵 晶体,反应生成CaC2O4沉淀,过滤、洗涤,将沉淀用稀硫酸处理得H2C2O4溶液。
晶体,反应生成CaC2O4沉淀,过滤、洗涤,将沉淀用稀硫酸处理得H2C2O4溶液。
ii.将i得到的H2C2O4溶液,再用KMnO4酸性溶液滴定,氧化产物为CO2,还原产物为 。
。
iii.终点时用去bmL 的KMnO4溶液。
的KMnO4溶液。
(6)写出用KMnO4酸性溶液滴定H2C2O4的离子方程式___________ 。
(7)如何判定滴定终点___________ 。
(8)计算:血液中含钙离子的浓度为___________ mol/L(用字母表示)。
Ⅲ.沉淀滴定法:
(9)用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中 ,利用
,利用 与
与 生成砖红色沉淀,指示到达滴定终点。当溶液中
生成砖红色沉淀,指示到达滴定终点。当溶液中 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于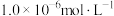 )时,溶液中
)时,溶液中 为
为___________  (已知
(已知 )。
)。
I.酸碱中和滴定:常温下,用0.1000mol/LNaOH溶液分别滴定20.00mL等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:
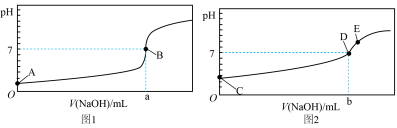
(2)达到B、D状态时,反应消耗NaOH溶液的体积a___________b(填编号)。
| A.> | B.< | C.= | D.不确定 |
(3)A、B、C、E四点水的电离程度由大到小顺序为:E>
(4)某次用氢氧化钠滴定未知浓度的醋酸的滴定结果如表所示:
| 滴定次数 | 待测液体积(mL) | 标准溶液的体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 1 | 20.00 | 1.02 | 18.97 |
| 2 | 20.00 | 0.60 | 见图 |
| 3 | 20.00 | 0.20 | 18.25 |

(5)下列操作中造成第2次所测测定结果明显偏差的是___________。
| A.盛放醋酸溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| B.配制标准溶液的固体NaOH中混有KOH杂质 |
| C.盛装NaOH标准溶液的滴定管在滴定前尖嘴处有气泡,滴定后气泡消失 |
| D.读取NaOH标准溶液的体积时,开始时仰视读数,滴定结束时俯视读数 |
Ⅱ.氧化还原滴定:
如测定血液中钙的含量时,进行如下实验:
i.可将amL血液用蒸馏水稀释后,向其中加入足量草酸铵
 晶体,反应生成CaC2O4沉淀,过滤、洗涤,将沉淀用稀硫酸处理得H2C2O4溶液。
晶体,反应生成CaC2O4沉淀,过滤、洗涤,将沉淀用稀硫酸处理得H2C2O4溶液。ii.将i得到的H2C2O4溶液,再用KMnO4酸性溶液滴定,氧化产物为CO2,还原产物为
 。
。iii.终点时用去bmL
 的KMnO4溶液。
的KMnO4溶液。(6)写出用KMnO4酸性溶液滴定H2C2O4的离子方程式
(7)如何判定滴定终点
(8)计算:血液中含钙离子的浓度为
Ⅲ.沉淀滴定法:
(9)用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中
 ,利用
,利用 与
与 生成砖红色沉淀,指示到达滴定终点。当溶液中
生成砖红色沉淀,指示到达滴定终点。当溶液中 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于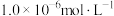 )时,溶液中
)时,溶液中 为
为 (已知
(已知 )。
)。
您最近一年使用:0次
2023-12-18更新
|
304次组卷
|
2卷引用:上海市七宝中学2023-2024学年高三上学期期中考试化学试题
名校
解题方法
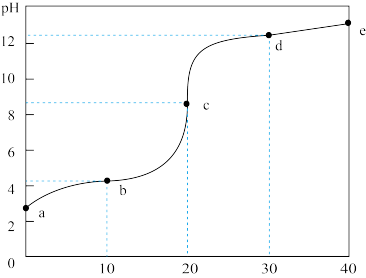
3 . 向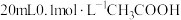 溶液中不断滴入等浓度的
溶液中不断滴入等浓度的 溶液,反应后溶液的
溶液,反应后溶液的 变化如图所示。下列分析
变化如图所示。下列分析错误 的是
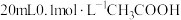 溶液中不断滴入等浓度的
溶液中不断滴入等浓度的 溶液,反应后溶液的
溶液,反应后溶液的 变化如图所示。下列分析
变化如图所示。下列分析
A.a点: |
B.b点: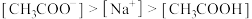 |
C.e点: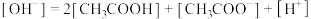 |
| D.水的电离程度由大到小的顺序为:c>d>b |
您最近一年使用:0次
2023-01-12更新
|
354次组卷
|
3卷引用:上海市七宝中学2022-2023学年高二上学期期末考试化学试题
上海市七宝中学2022-2023学年高二上学期期末考试化学试题上海市行知中学2022-2023学年高二下学期3月月考化学试题(已下线)题型02 溶液中粒子浓度大小比较-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)
名校
解题方法
4 . 常温下,往20mL0.1mol·L-1NH4HSO4溶液中逐滴加入0.1mol·L-1的NaOH溶液,溶液中由水电离的c水(H+)与所加NaOH溶液体积的关系如图所示(假设:混合后溶液体积的变化忽略不计,整个过程无氨气的逸出)。下列分析正确的是
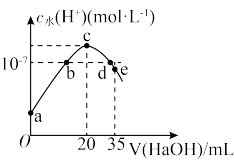
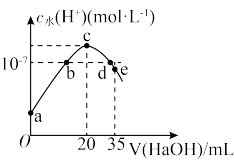
A.a~c之间,主要反应为NH +OH—=NH3·H2O +OH—=NH3·H2O |
| B.b点、d点对应溶液的pH均为7 |
C.d~e之间,溶液中c(Na+)+c(SO )=0.05mol/L )=0.05mol/L |
D.pH=7时,溶液中c(Na+)>c(SO )>c(NH )>c(NH )>c(OH—)=c(H+) )>c(OH—)=c(H+) |
您最近一年使用:0次
2022-01-16更新
|
467次组卷
|
3卷引用:上海市静安区2022届高三一模化学试题
5 . 下列实验现象或数据不能用勒沙特列原理解释的是
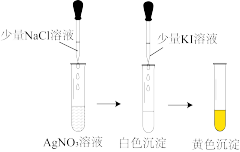 | 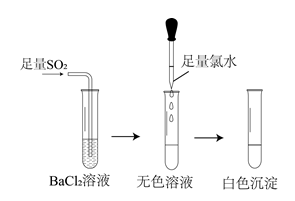 | ||||||
| A.探究卤化银沉淀的转化 | B.探究难溶性钡盐的生成 | ||||||
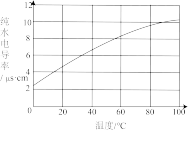 |
| ||||||
| C.测定不同温度纯水的导电性 | D.测定不同浓度氨水的pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 浓度均为0.1mol·L-1、体积均为V0的HX、HY溶液,分别加水稀释至体积为V,pH随lg 的变化关系如图所示。下列叙述正确的是
的变化关系如图所示。下列叙述正确的是
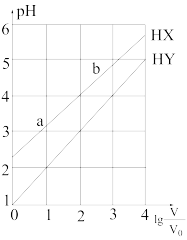
 的变化关系如图所示。下列叙述正确的是
的变化关系如图所示。下列叙述正确的是
| A.HX比HY易电离 |
| B.常温下,由水电离出的c(H+):a<b |
| C.相同温度下,电离常数K(HX):a>b |
| D.未稀释时两溶液的导电能力相同 |
您最近一年使用:0次
2021-09-27更新
|
805次组卷
|
4卷引用:上海交通大学附属中学2021-2022高二上学期开学摸底测试化学试题
上海交通大学附属中学2021-2022高二上学期开学摸底测试化学试题(已下线)必考点06 水的电离和溶液pH-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)吉林省延吉市第一高级中学2021-2022年学年高二上学期期中考试化学试题(已下线)T5-电解质溶液
名校
7 . 常温下,等体积等物质的量浓度的①氨水②盐酸③氯化铵溶液,下列说法错误的是
A.①中C(NH3·H2O) > C(OH-) > C(NH ) > C(H+) ) > C(H+) |
| B.①②混合后,铵根离子浓度小于③的二分之一 |
C.①③混合后,溶液呈碱性,则C(Cl-) > C(NH ) > C(OH-) ) > C(OH-) |
| D.②溶液中水的电离程度最小 |
您最近一年使用:0次
2020-12-31更新
|
236次组卷
|
2卷引用:上海市奉贤区2021届高三一模化学试卷



