名校
解题方法
1 . Ⅰ. 下的某溶液中,
下的某溶液中,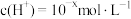 ,
,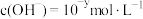 ,
, 与
与 的关系如下图所示:
的关系如下图所示:
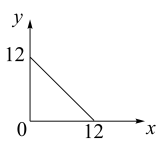
(1)在此温度下,向 溶液中逐滴加入
溶液中逐滴加入 的盐酸,测得混合溶液的部分
的盐酸,测得混合溶液的部分 如表所示:
如表所示:
假设溶液混合前后的体积变化忽略不计,则
_______ ,实验②中由水电离产生的
_______  。
。
(2)在此温度下,将 的
的 溶液
溶液 与
与 的
的 溶液
溶液 混合,所得溶液的
混合,所得溶液的 为
为_______ 。
Ⅱ.在保持体系总压为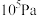 的条件下进行反应:
的条件下进行反应: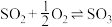 ,原料气中
,原料气中 和
和 的物质的量之比
的物质的量之比 不同时,
不同时, 的平衡转化率与温度
的平衡转化率与温度 的关系如图所示:
的关系如图所示:

(3)图中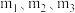 的大小顺序为
的大小顺序为_______ 。
(4)图中A点原料气的成分: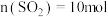 ,
,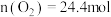 ,
, ,达平衡时
,达平衡时 的分压
的分压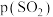 为
为_______  (分压=总压
(分压=总压 物质的量分数)。
物质的量分数)。
(5)若在容积均为2L的密闭容器内, 时按不同方式投入反应物,发生反应:
时按不同方式投入反应物,发生反应: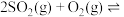
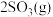
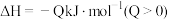 ,保持恒温恒容。初始投料与各容器达到平衡时的有关数据如下:
,保持恒温恒容。初始投料与各容器达到平衡时的有关数据如下:
三个容器中的反应分别达平衡时下列各组数据关系正确的是_______(填字母)。
Ⅲ. 与
与 发生羰化反应形成的络合物可作为催化剂。
发生羰化反应形成的络合物可作为催化剂。 的羰化反应为:
的羰化反应为: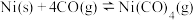
 ,
, 温度下测得一定的实验数据,计算
温度下测得一定的实验数据,计算 和
和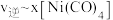 的关系如图所示:
的关系如图所示:
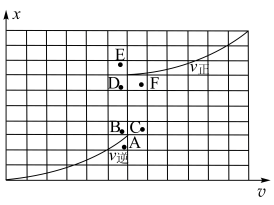
(6)当降低温度时,反应重新达到平衡, 和
和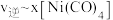 相对应的点分别为
相对应的点分别为_______ 、_______ (填字母)。
 下的某溶液中,
下的某溶液中,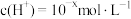 ,
,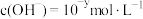 ,
, 与
与 的关系如下图所示:
的关系如下图所示:
(1)在此温度下,向
 溶液中逐滴加入
溶液中逐滴加入 的盐酸,测得混合溶液的部分
的盐酸,测得混合溶液的部分 如表所示:
如表所示:| 实验序号 |  溶液的体积/mL 溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |


 。
。(2)在此温度下,将
 的
的 溶液
溶液 与
与 的
的 溶液
溶液 混合,所得溶液的
混合,所得溶液的 为
为Ⅱ.在保持体系总压为
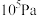 的条件下进行反应:
的条件下进行反应: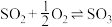 ,原料气中
,原料气中 和
和 的物质的量之比
的物质的量之比 不同时,
不同时, 的平衡转化率与温度
的平衡转化率与温度 的关系如图所示:
的关系如图所示:
(3)图中
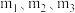 的大小顺序为
的大小顺序为(4)图中A点原料气的成分:
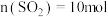 ,
,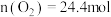 ,
, ,达平衡时
,达平衡时 的分压
的分压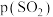 为
为 (分压=总压
(分压=总压 物质的量分数)。
物质的量分数)。(5)若在容积均为2L的密闭容器内,
 时按不同方式投入反应物,发生反应:
时按不同方式投入反应物,发生反应: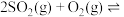
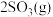
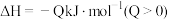 ,保持恒温恒容。初始投料与各容器达到平衡时的有关数据如下:
,保持恒温恒容。初始投料与各容器达到平衡时的有关数据如下:| 实验 | 甲 | 乙 | 丙 |
| 初始投料 | 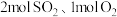 | 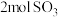 |  |
平衡时n( ) ) |  |  |  |
| 反应的能量变化 | 放出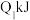 | 吸收 | 放出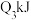 |
| 体系的压强 |  |  |  |
| 反应物的转化率 |  |  | 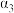 |
A.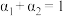 |
B.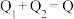 |
C. |
D. |
E. |
F.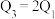 |
Ⅲ.
 与
与 发生羰化反应形成的络合物可作为催化剂。
发生羰化反应形成的络合物可作为催化剂。 的羰化反应为:
的羰化反应为: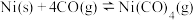
 ,
, 温度下测得一定的实验数据,计算
温度下测得一定的实验数据,计算 和
和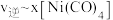 的关系如图所示:
的关系如图所示:
(6)当降低温度时,反应重新达到平衡,
 和
和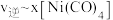 相对应的点分别为
相对应的点分别为
您最近一年使用:0次
解题方法
2 . 草酸 是二元弱酸,常温下,用
是二元弱酸,常温下,用 溶液滴定草酸溶液,溶液中
溶液滴定草酸溶液,溶液中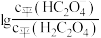 或
或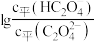 与混合溶液
与混合溶液 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是

 是二元弱酸,常温下,用
是二元弱酸,常温下,用 溶液滴定草酸溶液,溶液中
溶液滴定草酸溶液,溶液中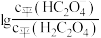 或
或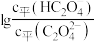 与混合溶液
与混合溶液 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
A.草酸的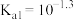 | B.水的电离程度 |
C. 点时, 点时, | D.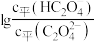 随溶液 随溶液 的变化为曲线Ⅱ 的变化为曲线Ⅱ |
您最近一年使用:0次
2023-12-03更新
|
310次组卷
|
2卷引用:山东省日照市2023-2024学年高二上学期期中校际联合考试化学试题
名校
解题方法
3 . 已知水的电离平衡曲线如图所示:
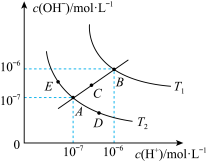
试回答下列问题:
(1)图中
_______  (用“>”、“<”、“=”回答)
(用“>”、“<”、“=”回答)
(2)图中五点的 间的关系是
间的关系是_______ 。
(3)若从A点到E点,可采用的措施是_______ 。
a.升温 b.加入少量的盐酸 c.加入少量的NaOH溶液
(4)点E对应的温度下,将 的NaOH溶液与
的NaOH溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则NaOH溶液与
,则NaOH溶液与 溶液的体积比为
溶液的体积比为_______ 。
(5)点B对应的温度下,若100体积 的某强酸溶液与1体积
的某强酸溶液与1体积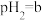 的某强碱溶液混合后溶液呈中性,则混合前,该强酸的
的某强碱溶液混合后溶液呈中性,则混合前,该强酸的 与强碱的
与强碱的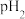 之间应满足的关系是
之间应满足的关系是_______ 。
(6)写出用pH试纸测溶液pH的操作_______ 。

试回答下列问题:
(1)图中

 (用“>”、“<”、“=”回答)
(用“>”、“<”、“=”回答)(2)图中五点的
 间的关系是
间的关系是(3)若从A点到E点,可采用的措施是
a.升温 b.加入少量的盐酸 c.加入少量的NaOH溶液
(4)点E对应的温度下,将
 的NaOH溶液与
的NaOH溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则NaOH溶液与
,则NaOH溶液与 溶液的体积比为
溶液的体积比为(5)点B对应的温度下,若100体积
 的某强酸溶液与1体积
的某强酸溶液与1体积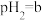 的某强碱溶液混合后溶液呈中性,则混合前,该强酸的
的某强碱溶液混合后溶液呈中性,则混合前,该强酸的 与强碱的
与强碱的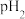 之间应满足的关系是
之间应满足的关系是(6)写出用pH试纸测溶液pH的操作
您最近一年使用:0次
2022-11-10更新
|
345次组卷
|
3卷引用:山东省菏泽市2022-2023学年高二上学期期中考试(B)化学试题
名校
解题方法
4 . 常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.0.1mol•L-1的(NH4)2SO4溶液中:Na+、Cu2+、Cl-、OH- |
B. =10-12的溶液中:Na+、NO =10-12的溶液中:Na+、NO 、[Al(OH)4]-、CO 、[Al(OH)4]-、CO |
C.水电离的c(H+)=1×10-13mol•L-1溶液中:Na+、K+、NO 、HCO 、HCO |
D.0.1mol•L-1的FeCl3溶液中:K+、Mg2+、SO 、SCN- 、SCN- |
您最近一年使用:0次
解题方法
5 . 室温下,向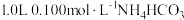 溶液中加入
溶液中加入 稀溶液,溶液中主要微粒的分布系数【如
稀溶液,溶液中主要微粒的分布系数【如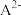 的分布系数
的分布系数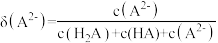 】以及
】以及 随
随 变化如图。
变化如图。
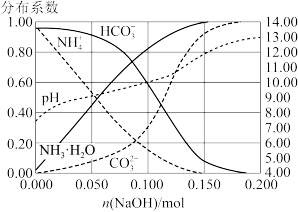
下列叙述错误的是
 溶液中加入
溶液中加入 稀溶液,溶液中主要微粒的分布系数【如
稀溶液,溶液中主要微粒的分布系数【如 的分布系数
的分布系数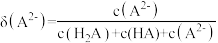 】以及
】以及 随
随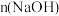 变化如图。
变化如图。
下列叙述错误的是
A.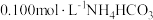 溶液中 溶液中 ,水电离受到促进 ,水电离受到促进 |
B.加入 稀溶液过程中,溶液满足关系式 稀溶液过程中,溶液满足关系式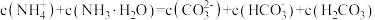 |
C.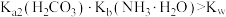 |
D.加入少量 时, 时, 先与 先与 发生主要反应 发生主要反应 |
您最近一年使用:0次
名校
解题方法
6 . 常温下,浓度相同的一元弱酸 稀溶液和一元弱碱
稀溶液和一元弱碱 稀溶液互相滴定,溶液中
稀溶液互相滴定,溶液中 与
与 或
或 的关系如图所示。已知
的关系如图所示。已知 和
和 的电离常数为
的电离常数为 和
和 ,且b和b′点的纵坐标之和为14。下列说法错误的是
,且b和b′点的纵坐标之和为14。下列说法错误的是
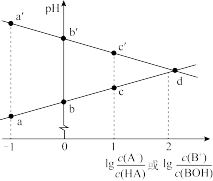
 稀溶液和一元弱碱
稀溶液和一元弱碱 稀溶液互相滴定,溶液中
稀溶液互相滴定,溶液中 与
与 或
或 的关系如图所示。已知
的关系如图所示。已知 和
和 的电离常数为
的电离常数为 和
和 ,且b和b′点的纵坐标之和为14。下列说法错误的是
,且b和b′点的纵坐标之和为14。下列说法错误的是
A.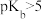 | B.a和a′点的纵坐标之和为14 |
C.水的电离程度: | D.溶液中的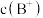 :c点大于c′点 :c点大于c′点 |
您最近一年使用:0次
2022-05-05更新
|
614次组卷
|
3卷引用:山东省济南市2022届高三第二次模拟化学试题
解题方法
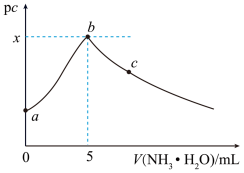
7 . 常温下,向 一定浓度的硫酸铜溶液中逐滴滴入
一定浓度的硫酸铜溶液中逐滴滴入 的氨水,首先析出浅蓝色的
的氨水,首先析出浅蓝色的 沉淀,氨水过量时此沉淀溶解,形成
沉淀,氨水过量时此沉淀溶解,形成 络离子(假定溶液混合后体积不变)。滴加过程中
络离子(假定溶液混合后体积不变)。滴加过程中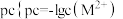 ,
, 为
为 或
或 与氨水体积的关系如图所示。下列说法错误的是
与氨水体积的关系如图所示。下列说法错误的是
 一定浓度的硫酸铜溶液中逐滴滴入
一定浓度的硫酸铜溶液中逐滴滴入 的氨水,首先析出浅蓝色的
的氨水,首先析出浅蓝色的 沉淀,氨水过量时此沉淀溶解,形成
沉淀,氨水过量时此沉淀溶解,形成 络离子(假定溶液混合后体积不变)。滴加过程中
络离子(假定溶液混合后体积不变)。滴加过程中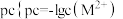 ,
, 为
为 或
或 与氨水体积的关系如图所示。下列说法错误的是
与氨水体积的关系如图所示。下列说法错误的是
A.硫酸铜溶液的浓度为 |
B.常温下, 点溶液中水的电离程度低于纯水的 点溶液中水的电离程度低于纯水的 |
C. 点溶液中存在 点溶液中存在 |
D.常温下,忽略 的影响,可得 的影响,可得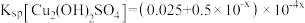 |
您最近一年使用:0次
名校
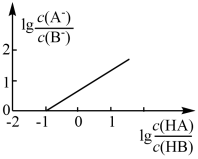
8 . 常温下,向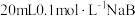 溶液中滴入等物质的量浓度的
溶液中滴入等物质的量浓度的 溶液,所得溶液中
溶液,所得溶液中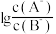 与
与 的关系如图所示,已知
的关系如图所示,已知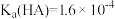 。下列说法正确的是
。下列说法正确的是
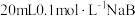 溶液中滴入等物质的量浓度的
溶液中滴入等物质的量浓度的 溶液,所得溶液中
溶液,所得溶液中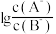 与
与 的关系如图所示,已知
的关系如图所示,已知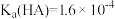 。下列说法正确的是
。下列说法正确的是
A.滴加过程反应为 |
B.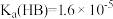 |
| C.滴加过程溶液中水的电离程度先增大后减小 |
D.滴入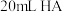 ,溶液中 ,溶液中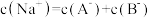 |
您最近一年使用:0次
2022-02-03更新
|
462次组卷
|
3卷引用:山东省青岛市黄岛区2021-2022学年高三上学期期末考试化学试题
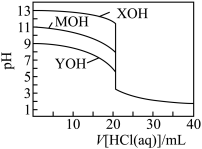
9 . 常温下,用 盐酸分别逐滴加入到
盐酸分别逐滴加入到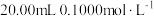 的三种一元碱溶液中,溶液的
的三种一元碱溶液中,溶液的 随加入盐酸体积的变化如图所示。下列叙述错误的是
随加入盐酸体积的变化如图所示。下列叙述错误的是
 盐酸分别逐滴加入到
盐酸分别逐滴加入到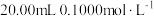 的三种一元碱溶液中,溶液的
的三种一元碱溶液中,溶液的 随加入盐酸体积的变化如图所示。下列叙述错误的是
随加入盐酸体积的变化如图所示。下列叙述错误的是
A.一元碱电离常数大小关系为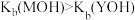 |
B.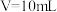 时, 时,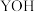 溶液中 溶液中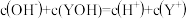 |
C.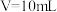 时,三种溶液中阳离子总浓度大小顺序为 时,三种溶液中阳离子总浓度大小顺序为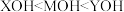 |
D. 时,三种溶液中水的电离程度最大的是 时,三种溶液中水的电离程度最大的是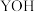 |
您最近一年使用:0次
2022-02-03更新
|
267次组卷
|
2卷引用:山东省青岛市黄岛区2021-2022学年高二上学期期末考试化学试题
名校
解题方法
10 . 常温下,向20 mL某浓度的硫酸溶液中滴入0.1 mol·L-1氨水,溶液中水电离的氢离子浓度随加入氨水的体积变化如图。下列分析正确的是
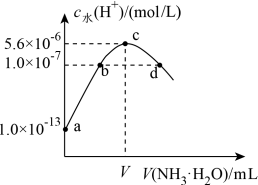

| A.V=40 |
| B.c点所示溶液中:c(H+)-c(OH-)=2c(NH3·H2O) |
| C.NH3·H2O的电离常数K=10-4 |
D.d点所示溶液中:c(NH )=2c(SO )=2c(SO ) ) |
您最近一年使用:0次
2022-01-21更新
|
535次组卷
|
16卷引用:2016届山东省临沂市高三下学期教学质检一模化学试卷
2016届山东省临沂市高三下学期教学质检一模化学试卷2015-2016学年福建省厦门市海沧中学高二下学期期末化学试卷2016-2017学年辽宁省沈阳铁路中学高二上第一次月考化学试卷江西省景德镇市第一中学2016-2017学年高二(素质班)下学期期末考试化学试题【全国百强校】山西省长治市第二中学2018-2019学年高二上学期第二次月考(期中)化学试题百所名校联考-水溶液中的离子平衡夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——盐类水解中三大守恒的应用2020届高三化学选修4二轮专题练——混合溶液中微粒浓度大小的比较专题【精编23题】江西省南昌市南昌县莲塘第三中学2020-2021学年高二上学期第二次月考化学试题(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)第6讲 离子平衡坐标图像-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题13 水溶液中的离子平衡-2022年高考化学二轮复习重点专题常考点突破练新疆乌鲁木齐市第七十中学2022-2023学年高二上学期期中考试化学试题



