名校
解题方法
1 . 室温时,向20mL0.1mol/L的两种酸HA、HB中分别滴加0.1mol/LNaOH 溶液,其pH变化分别对应下图中的I、Ⅱ。下列说法不正确的是


| A.向NaA溶液中滴加HB可产生HA |
| B.a点,溶液中微粒浓度:c(A-)>c(Na+)>c(HA) |
| C.滴加20mLNaOH溶液时,I中H2O的电离程度大于Ⅱ中 |
| D.滴加NaOH溶液至pH=7时,两种溶液中c(A-)=c(B-) |
您最近一年使用:0次
2022高三·全国·专题练习
解题方法
2 . 室温下,向10mL0.1mol·L-1HA溶液中滴加0.1mol·L-1的NaOH溶液,溶液的酸度(AG)与NaOH溶液体积的关系如图所示。已知:AG=lg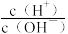 。
。
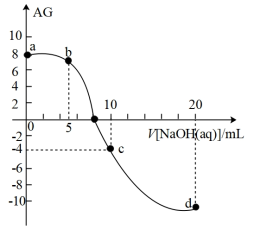
下列说法错误的是
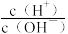 。
。
下列说法错误的是
| A.在a、b、c、d点对应的溶液中,c点时水的电离程度最大 |
| B.b点对应的溶液中:c(A-)>c(Na+)>c(H+)>c(OH-) |
| C.d点对应的溶液中:c(OH-)=c(H+)+c(HA)+c(A-) |
| D.室温下,HA的电离常数Ka约为1.0×10-4 |
您最近一年使用:0次
2022-04-30更新
|
354次组卷
|
3卷引用:河北省保定市部分学校2021-2022学年高三上学期期中考试化学试题
河北省保定市部分学校2021-2022学年高三上学期期中考试化学试题广东省韶关市2021-2022学年高三上学期期中考试化学试题(已下线)押新高考卷13题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(新高考通版)
名校
3 . 下列图示与对应的叙述不相符的是
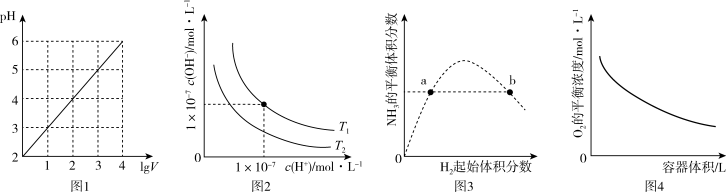
| A.图1表示1LpH=2的HCl溶液加水稀释至VL,pH随lgV的变化 |
| B.图2表示不同温度下水溶液中H+和OH-浓度的变化的曲线,图中温度T1>T2 |
| C.图3表示一定条件下的合成氨反应中,NH3的平衡体积分数随H2起始体积分数(N2的起始量恒定)的变化,图中a点N2的转化率小于b点 |
D.图4表示同一温度下,在不同容积的容器中进行反应2BaO2(s) 2BaO(s)+O2(g),O2的平衡浓度与容器容积的关系 2BaO(s)+O2(g),O2的平衡浓度与容器容积的关系 |
您最近一年使用:0次
2022-04-04更新
|
751次组卷
|
3卷引用:黑龙江省鸡西市一中2021-2022学年高二上学期期中考试化学试题
4 . 25℃时,三种酸的电离平衡常数如下:
回答下列问题:
(1)一般情况下,当温度升高时,Ka___________ (填“增大”、“减小”或“不变”)。
(2)下列四种离子结合质子能力由大到小的顺序是___________ (填字母)。
a.CO b.ClO— c.CH3COO— d.HCO
b.ClO— c.CH3COO— d.HCO
(3)下列反应不能发生的是___________ (填字母)。
a. CO +2CH3COOH=2CH3COO—+CO2↑+H2O b. ClO—+CH3COOH=CH3COO—+HClOc. CO
+2CH3COOH=2CH3COO—+CO2↑+H2O b. ClO—+CH3COOH=CH3COO—+HClOc. CO +2HClO=CO2↑+H2O+2ClO—d. 2ClO—+CO2+H2O=CO
+2HClO=CO2↑+H2O+2ClO—d. 2ClO—+CO2+H2O=CO +2HClO
+2HClO
(4)用蒸馏水稀释0.10mol·L-1的醋酸,下列各式表示的数值随水量的增加而增大的是___________ (填字母)。
a. b.
b.  c.
c.  d.
d.
(5)体积均为10 mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000 mL,稀释过程中pH变化如图所示。则HX的电离平衡常数___________ (填“>”、“=”或“<”,下同)醋酸的电离平衡常数;稀释后,HX溶液中水电离出来的c(H+)___________ 醋酸溶液中水电离出来的c(H+);用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸___________ HX。

(6)25℃时,若测得CH3COOH与CH3COONa的混合溶液的pH=6,则溶液中c(CH3COO—)—c(Na+)=___________ mol·L-1(填精确数值)。
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
回答下列问题:
(1)一般情况下,当温度升高时,Ka
(2)下列四种离子结合质子能力由大到小的顺序是
a.CO
 b.ClO— c.CH3COO— d.HCO
b.ClO— c.CH3COO— d.HCO
(3)下列反应不能发生的是
a. CO
 +2CH3COOH=2CH3COO—+CO2↑+H2O b. ClO—+CH3COOH=CH3COO—+HClOc. CO
+2CH3COOH=2CH3COO—+CO2↑+H2O b. ClO—+CH3COOH=CH3COO—+HClOc. CO +2HClO=CO2↑+H2O+2ClO—d. 2ClO—+CO2+H2O=CO
+2HClO=CO2↑+H2O+2ClO—d. 2ClO—+CO2+H2O=CO +2HClO
+2HClO(4)用蒸馏水稀释0.10mol·L-1的醋酸,下列各式表示的数值随水量的增加而增大的是
a.
 b.
b.  c.
c.  d.
d.
(5)体积均为10 mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000 mL,稀释过程中pH变化如图所示。则HX的电离平衡常数

(6)25℃时,若测得CH3COOH与CH3COONa的混合溶液的pH=6,则溶液中c(CH3COO—)—c(Na+)=
您最近一年使用:0次
名校
5 . 室温下,向V mL  的二元弱酸
的二元弱酸 溶液中滴加
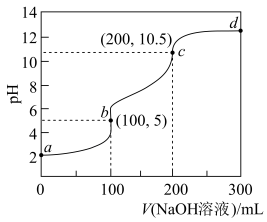
溶液中滴加 NaOH溶液,溶液的pH随NaOH溶液体积的变化曲线如下图所示。下列有关说法正确的是
NaOH溶液,溶液的pH随NaOH溶液体积的变化曲线如下图所示。下列有关说法正确的是
 的二元弱酸
的二元弱酸 溶液中滴加
溶液中滴加 NaOH溶液,溶液的pH随NaOH溶液体积的变化曲线如下图所示。下列有关说法正确的是
NaOH溶液,溶液的pH随NaOH溶液体积的变化曲线如下图所示。下列有关说法正确的是
| A.a→d的过程中,水的电离程度一直增大 |
B.选择酚酞作指示剂,滴定终点时,只有反应 发生 发生 |
C.加入NaOH溶液50 mL,混合溶液中: |
D.加入NaoH溶液150 mL,混合溶液中: |
您最近一年使用:0次
2021-11-27更新
|
826次组卷
|
4卷引用:重庆市巴蜀中学2021-2022学年高二上期期中考试化学试题
名校
6 . 在某温度时,将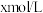 氨水滴入
氨水滴入
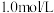 盐酸中,溶液
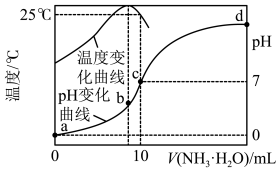
盐酸中,溶液 和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是
和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是
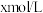 氨水滴入
氨水滴入
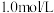 盐酸中,溶液
盐酸中,溶液 和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是
和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是
A.a点: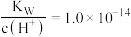 |
B.氨水的浓度为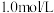 |
C.b点溶液中加入 溶液至中性后, 溶液至中性后,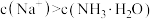 |
D.b、c、d三点水的电离程度大小关系是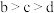 |
您最近一年使用:0次
2021-11-26更新
|
660次组卷
|
4卷引用:上海市复旦大学附属中学2021-2022学年高三上学期期中考试化学试题
解题方法
7 . 已知水的电离平衡曲线如图所示,下列说法中正确的是
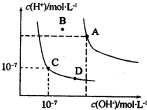

| A.水的离子积常数关系为:KW(B)>KW(A)>KW(C)>KW(D) |
| B.恒温下向水中加入氢氧化钠固体,可从C点到D点 |
| C.B点对应的温度下,pH=4的硫酸与pH=10的氢氧化钠溶液等体积混合后所得溶液的pH=7 |
| D.温度升高可实现由C点到D点 |
您最近一年使用:0次
名校
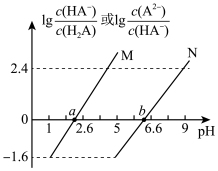
8 . 常温下将NaOH溶液滴加到 溶液中,混合溶液的pH与离子浓度变化的关系如图所示,[纵坐标为
溶液中,混合溶液的pH与离子浓度变化的关系如图所示,[纵坐标为 或
或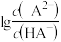 ]下列叙述错误的是
]下列叙述错误的是
 溶液中,混合溶液的pH与离子浓度变化的关系如图所示,[纵坐标为
溶液中,混合溶液的pH与离子浓度变化的关系如图所示,[纵坐标为 或
或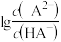 ]下列叙述错误的是
]下列叙述错误的是
A.曲线M表示pH与 的关系 的关系 |
B.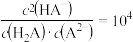 |
C.b点对应溶液中: |
| D.溶液pH从2.6到6.6的过程中,水的电离程度先增大后减小 |
您最近一年使用:0次
2021-11-19更新
|
815次组卷
|
3卷引用:四川省成都市石室中学2021-2022学年高三上学期期中考试化学试题
名校
解题方法
9 . 利用烟道气中的 生产
生产 晶体的工艺流程如下所示。下列说法错误的是
晶体的工艺流程如下所示。下列说法错误的是
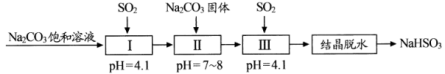
 生产
生产 晶体的工艺流程如下所示。下列说法错误的是
晶体的工艺流程如下所示。下列说法错误的是
A. 时,步骤Ⅰ中溶液为 时,步骤Ⅰ中溶液为 溶液 溶液 |
B.步骤Ⅲ所得溶液中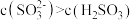 |
C.向 饱和溶液中通入 饱和溶液中通入 的过程,水的电离程度先增大后减小 的过程,水的电离程度先增大后减小 |
D.步骤Ⅱ中发生的反应之一为: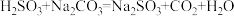 ,则 ,则 的 的 大于 大于 的 的 |
您最近一年使用:0次
名校
10 . 常温下,向20 mL某浓度的硫酸中滴入0.1 mol/L氨水,溶液中水电离出的氢离子的浓度随加入氨水的体积变化如图所示。下列说法正确的是


| A.V=20 |
B.b点所示溶液中:c( )=2c( )=2c( ) ) |
| C.c点所示溶液中:c(H+)-c(OH-)=c(NH3∙H2O) |
| D.该硫酸的浓度为0.1 mol/L |
您最近一年使用:0次
2021-11-17更新
|
112次组卷
|
2卷引用:河北省石家庄市石家庄二中教育集团2021-2022学年高一上学期期中考试化学试题



