名校
1 . 草酸是植物(特别是草本植物)常具有的成分,具有广泛的用途。草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数K1=5.4×10-2,K2=5.4×10-5。回答下列问题:
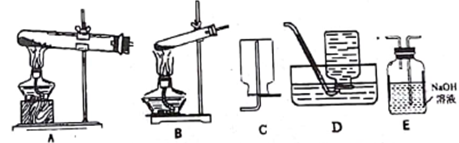
I.拟用下列装置分解草酸制备少量纯净的CO,其合理的连接顺序为________ (填字母序号)。
Ⅱ.设计实验证明草酸为弱酸的方案及其现象均正确的有______ (填序号)。
A.室温下,取0.010mol/L的H2C2O4溶液,测其pH=2;
B.室温下,取0.010mol/L的NaHC2O4溶液,测其pH>7;
C. 室温下,取pH=a(a<3)的H2C2O4溶液稀释100倍后,测其pH
D.标况下,取0.10mol/L的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL
Ⅲ.医学上常用酸性KMnO4溶液和草酸(H2C2O4)溶液反应来测血液中血钙的含量。测定方法是:取2mL血液用蒸馏水稀释后.向其中加入足量的(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①溶解沉淀时______ (填“能”或“不能”)用稀盐酸,原因是_________ 。
②滴定时,用______ (填“酸”或“碱”)式滴定管装KMnO4溶液,滴定达到终点的现象是______ 。
③ 滴定过程中发生的离子反应方程式______________ 。
④ 若上述滴定中消耗了1.0×10-4mol/LKMnO4的溶液20mL,则200mL该血液中含钙_____ g。
⑤ 下列操作会引起测定结果偏高的是__________ (填序号)
A.滴定管在盛装KMnO4溶液前未润洗
B.滴定过程中,锥形瓶振荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.装待测液的锥形瓶用蒸馏水洗涤后,没用待测液冲洗
I.拟用下列装置分解草酸制备少量纯净的CO,其合理的连接顺序为

Ⅱ.设计实验证明草酸为弱酸的方案及其现象均正确的有
A.室温下,取0.010mol/L的H2C2O4溶液,测其pH=2;
B.室温下,取0.010mol/L的NaHC2O4溶液,测其pH>7;
C. 室温下,取pH=a(a<3)的H2C2O4溶液稀释100倍后,测其pH
D.标况下,取0.10mol/L的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL
Ⅲ.医学上常用酸性KMnO4溶液和草酸(H2C2O4)溶液反应来测血液中血钙的含量。测定方法是:取2mL血液用蒸馏水稀释后.向其中加入足量的(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①溶解沉淀时
②滴定时,用
③ 滴定过程中发生的离子反应方程式
④ 若上述滴定中消耗了1.0×10-4mol/LKMnO4的溶液20mL,则200mL该血液中含钙
⑤ 下列操作会引起测定结果偏高的是
A.滴定管在盛装KMnO4溶液前未润洗
B.滴定过程中,锥形瓶振荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.装待测液的锥形瓶用蒸馏水洗涤后,没用待测液冲洗
您最近一年使用:0次
2010·北京西城·一模
2 .
| 编号 | 实验操作 | 目的 |
| A | 取4 g NaOH加入96 mL水中 (水的密度近似看作1 g/cm3) | 配制4 % NaOH溶液 |
| B | 滴定实验中,用待测液润洗锥形瓶 | 避免造成误差使滴定结果偏低 |
| C | 向CH3COONa溶液中滴入酚酞溶液,加热 | 证明升高温度能促进CH3COONa水解 |
| D | 向盛有铜片的试管中加入浓硫酸,加热 | 证明浓硫酸具有强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
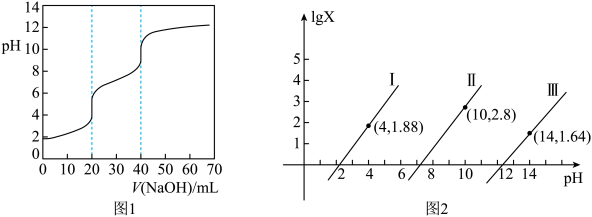
3 . 常温下用NaOH标准溶液滴定20mL等浓度的三元酸 ,得到pH与V(NaOH)、
,得到pH与V(NaOH)、 [
[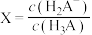 或
或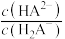 或
或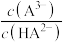 ]的关系分别如图1、图2所示。下列说法错误的是
]的关系分别如图1、图2所示。下列说法错误的是
 ,得到pH与V(NaOH)、
,得到pH与V(NaOH)、 [
[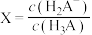 或
或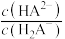 或
或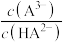 ]的关系分别如图1、图2所示。下列说法错误的是
]的关系分别如图1、图2所示。下列说法错误的是
A.当pH=10时,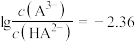 |
B. ,对应2.12<pH<7.2 ,对应2.12<pH<7.2 |
| C.20mL到40mL滴定过程中,水的电离程度逐渐增大 |
| D.用NaOH标准液滴定NaH2A溶液时,可选用酚酞做指示剂 |
您最近一年使用:0次
2022-12-29更新
|
515次组卷
|
2卷引用:辽宁省大连市2022-2023学年高三双基考试化学试题
4 . 用标准盐酸溶液滴定未知浓度的氢氧化钠溶液,用酚酞作指示剂,下列说法不正确的是
| A.用量筒量取25.00mLNaOH待测液置于锥形瓶中 |
| B.滴定前不能用待测液润洗锥形瓶 |
| C.滴定终点读数时,俯视滴定管的刻度,测定结果偏低 |
| D.当滴加半滴酸后,溶液颜色从粉红色刚好变为无色,且半分钟内不变色,说明已达终点 |
您最近一年使用:0次
名校
解题方法
5 . 取未知浓度的硫酸、盐酸和醋酸各25.00mL,分别用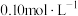 的NaOH溶液或
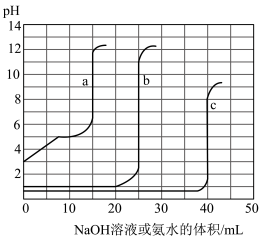
的NaOH溶液或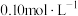 的稀氨水滴定得到下图所示曲线。下列说法不正确的是
的稀氨水滴定得到下图所示曲线。下列说法不正确的是
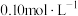 的NaOH溶液或
的NaOH溶液或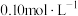 的稀氨水滴定得到下图所示曲线。下列说法不正确的是
的稀氨水滴定得到下图所示曲线。下列说法不正确的是
| A.由图可知曲线c为NaOH滴定硫酸 |
| B.由图可知可求出硫酸的物质的量浓度小于盐酸的物质的量浓度 |
| C.曲线b、c的滴定实验可用酚酞作指示剂 |
| D.由图可知滴定前醋酸电离百分比约为1.67% |
您最近一年使用:0次
6 . 25℃时,0.1L某二元弱酸 溶液用
溶液用 溶液调节pH,溶液中
溶液调节pH,溶液中 、
、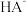 及
及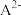 的物质的量浓度变化如图所示。下列说法错误的是
的物质的量浓度变化如图所示。下列说法错误的是

 溶液用
溶液用 溶液调节pH,溶液中
溶液调节pH,溶液中 、
、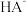 及
及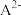 的物质的量浓度变化如图所示。下列说法错误的是
的物质的量浓度变化如图所示。下列说法错误的是
A.曲线B代表 |
B.在Y点时, |
C. 的 的 |
D. 溶液中: 溶液中: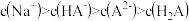 |
您最近一年使用:0次
名校
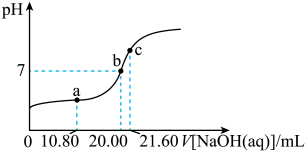
7 . 常温下,用某未知浓度的 溶液滴定
溶液滴定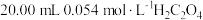 溶液,滴定曲线如图所示,c点溶液中,
溶液,滴定曲线如图所示,c点溶液中,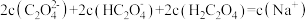 。下列说法错误的是
。下列说法错误的是
 溶液滴定
溶液滴定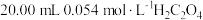 溶液,滴定曲线如图所示,c点溶液中,
溶液,滴定曲线如图所示,c点溶液中,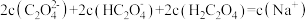 。下列说法错误的是
。下列说法错误的是
| A.c点为反应终点 |
B.该 溶液的物质的量浓度为 溶液的物质的量浓度为 |
C.b点溶液中,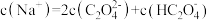 |
D.a点溶液中, |
您最近一年使用:0次
2024-03-04更新
|
116次组卷
|
3卷引用:辽宁省朝阳市建平县实验中学2023-2024学年高二上学期期末化学试题
8 . 分别用 的
的 溶液滴定
溶液滴定 等浓度的
等浓度的 溶液或
溶液或 的
的 溶液滴定
溶液滴定 等浓度的盐酸,滴定过程中溶液的导电能力变化如图所示,下列说法错误的是
等浓度的盐酸,滴定过程中溶液的导电能力变化如图所示,下列说法错误的是

 的
的 溶液滴定
溶液滴定 等浓度的
等浓度的 溶液或
溶液或 的
的 溶液滴定
溶液滴定 等浓度的盐酸,滴定过程中溶液的导电能力变化如图所示,下列说法错误的是
等浓度的盐酸,滴定过程中溶液的导电能力变化如图所示,下列说法错误的是
A.等浓度的盐酸与 溶液导电能力相同 溶液导电能力相同 |
| B.a点溶液中的阴离子总浓度大于b点溶液中的阴离子总浓度 |
C.b点溶液中离子浓度: |
D.c点溶液中: |
您最近一年使用:0次
解题方法
9 . 某温度下, 滴定
滴定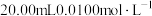 盐酸的滴定曲线如图所示。下列说法错误的是
盐酸的滴定曲线如图所示。下列说法错误的是

 滴定
滴定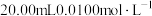 盐酸的滴定曲线如图所示。下列说法错误的是
盐酸的滴定曲线如图所示。下列说法错误的是
| A.该温度高于室温 |
B.b点时溶液中 |
| C.滴定过程中,水的电离程度先增大后减小 |
D.相同条件下,若使用 溶液滴定,反应终点由b变为a点 溶液滴定,反应终点由b变为a点 |
您最近一年使用:0次
2023-03-21更新
|
563次组卷
|
4卷引用:辽宁省名校联盟2022-2023年学高二下学期3月联考化学
名校
解题方法
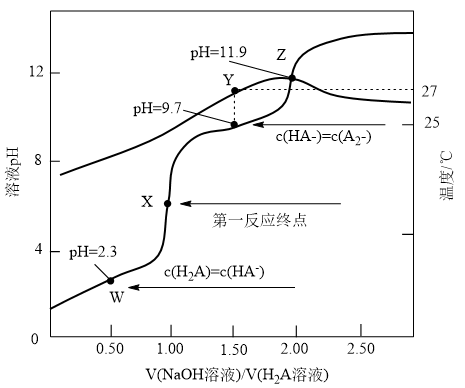
10 . 按一定的速率用0.10mol·L-1NaOH溶液滴定10.0mL0.10 mol·L-1H2A溶液,溶液pH和温度随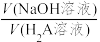 的变化曲线如图所示。下列说法
的变化曲线如图所示。下列说法不正确 的是
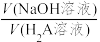 的变化曲线如图所示。下列说法
的变化曲线如图所示。下列说法
| A.从W至Z点,水的电离程度和KW逐渐增大 |
B.当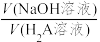 =1时c(Na+)=c(H2A)+c(HA-)+c(A2-) =1时c(Na+)=c(H2A)+c(HA-)+c(A2-) |
C.27℃,H2A的电离常数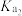 =10-9.7 =10-9.7 |
| D.可用酚酞作为第二反应终点的指示剂 |
您最近一年使用:0次
2021-11-12更新
|
484次组卷
|
6卷引用:一轮巩固卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(辽宁专用)
(已下线)一轮巩固卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(辽宁专用)辽宁省沈阳市第一二〇中学2021-2022学年高三下学期4月独立作业化学试题 浙江省金华十校2021-2022学年高三上学期11月模拟考试化学试题(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密10 水溶液中的离子平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)湖南省湘潭市湘乡市东山学校2022学年高三下学期期中考试化学试题



