1 . 草酸(H2C2O4)是一种易溶于水的二元有机弱酸,常用作还原剂、沉淀剂等,可与酸性KMnO4溶液发生反应:5H2C2O4+2MnO +6H+=2Mn2++10CO2↑+8H2O。
+6H+=2Mn2++10CO2↑+8H2O。
(1)探究外界条件对反应速率的影响。
①完成此实验设计,其中:V1=_____ ,V2=_____ 。
②对比实验1、2可探究_____ 对反应速率的影响。
③已知Mn2+对H2C2O4和KMnO4溶液的反应有催化作用,请设计实验4证明_____ 。
(2)某兴趣小组用草酸及草酸盐的性质测定硬水中钙离子的浓度。
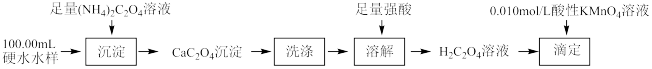
根据消耗酸性KMnO4标准溶液的体积即可测定硬水样品中Ca2+的浓度。
①实验过程提及的下列仪器,在使用之前一定要润洗的是_____ (填字母)。
A.容量瓶 B.烧杯 C.锥形瓶 D.滴定管
②滴定过程中______ (填“需要”或“不需要”)另加指示剂,如何判断滴定终点_____ 。
③本实验滴定管起点和终点的液面位置如图所示,则滴定过程中消耗的KMnO4标准溶液为_____ mL。该硬水样品中Ca2+的浓度为_____ mol∙L−1。

④下列不当操作会使测得的硬水样品Ca2+的浓度偏高的是_____ (填字母)。
A.滴定管未用标准溶液润洗 B.草酸钙(H2C2O4)沉淀洗涤不充分
C.滴定前仰视读数并记录数据 D.盛放草酸溶液的锥形瓶没有干燥
 +6H+=2Mn2++10CO2↑+8H2O。
+6H+=2Mn2++10CO2↑+8H2O。(1)探究外界条件对反应速率的影响。
| 实验编号 | 所加试剂及用量/mL | 条件 | 溶液颜色褪至无色所需时间/min | |||
| 0.01 mol∙L−1H2C2O4溶液 | 0.01 mol∙L−1KMnO4溶液 | 3.0 mol∙L−1稀H2SO4 | 水 | 温度℃ | ||
| 1 | 12.0 | 2.0 | 3.0 | 3.0 | 20 | t1 |
| 2 | 6.0 | 2.0 | 3.0 | V1 | 20 | t2 |
| 3 | V2 | 2.0 | 3.0 | 9.0 | 30 | t3 |
②对比实验1、2可探究
③已知Mn2+对H2C2O4和KMnO4溶液的反应有催化作用,请设计实验4证明
(2)某兴趣小组用草酸及草酸盐的性质测定硬水中钙离子的浓度。

根据消耗酸性KMnO4标准溶液的体积即可测定硬水样品中Ca2+的浓度。
①实验过程提及的下列仪器,在使用之前一定要润洗的是
A.容量瓶 B.烧杯 C.锥形瓶 D.滴定管
②滴定过程中
③本实验滴定管起点和终点的液面位置如图所示,则滴定过程中消耗的KMnO4标准溶液为

④下列不当操作会使测得的硬水样品Ca2+的浓度偏高的是
A.滴定管未用标准溶液润洗 B.草酸钙(H2C2O4)沉淀洗涤不充分
C.滴定前仰视读数并记录数据 D.盛放草酸溶液的锥形瓶没有干燥
您最近一年使用:0次
名校
2 . 回答下列问题
(1)依据反应: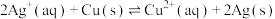 设计的原电池如下图甲所示。
设计的原电池如下图甲所示。
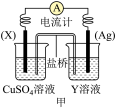
①电极 的材料是
的材料是_______ ;Y溶液可以是_______ ;
②银电极上发生的电极反应式是_______ , 电极上发生的电极反应为
电极上发生的电极反应为_______ 反应(填“氧化”或“还原”);外电路中的电子_______ (填“流出”或“流向”)Ag电极。
(2)次磷酸 是一种精细化工产品,已知
是一种精细化工产品,已知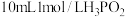 与
与 的
的 溶液充分反应后生成组成为
溶液充分反应后生成组成为 的盐,则:
的盐,则:
①次磷酸 属于
属于_______ (填“一元酸”“二元酸”或“无法确定”)。
②设计实验方案,证明次磷酸是弱酸:_______ 。
(3)某课外兴趣小组用 的
的 标准溶液滴定未知浓度的盐酸溶液,实验操作如下,请完成以下问题。
标准溶液滴定未知浓度的盐酸溶液,实验操作如下,请完成以下问题。
①该小组同学选用酚酞做指示剂,滴定终点的现象为_______ 。
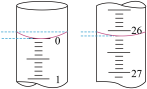
②该小组某一次滴定操作中,酸式滴定管的始终液面如图所示,则本次滴入的盐酸体积为_______  。
。
③下列操作中,可能使所测盐酸溶液的浓度值偏低的是_______
A.碱式滴定管末用标准氢氧化钠溶液润洗就直接注入标准溶液
B.碱式滴定管在滴定前有气泡,滴定后气泡消失
C.读取氢氧化钠体积时,滴定结束时俯视读数
D.滴定前盛放盐酸溶液的锥形瓶用蒸馏水洗净后没有干燥
(1)依据反应:
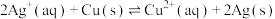 设计的原电池如下图甲所示。
设计的原电池如下图甲所示。
①电极
 的材料是
的材料是②银电极上发生的电极反应式是
 电极上发生的电极反应为
电极上发生的电极反应为(2)次磷酸
 是一种精细化工产品,已知
是一种精细化工产品,已知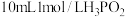 与
与 的
的 溶液充分反应后生成组成为
溶液充分反应后生成组成为 的盐,则:
的盐,则:①次磷酸
 属于
属于②设计实验方案,证明次磷酸是弱酸:
(3)某课外兴趣小组用
 的
的 标准溶液滴定未知浓度的盐酸溶液,实验操作如下,请完成以下问题。
标准溶液滴定未知浓度的盐酸溶液,实验操作如下,请完成以下问题。①该小组同学选用酚酞做指示剂,滴定终点的现象为
②该小组某一次滴定操作中,酸式滴定管的始终液面如图所示,则本次滴入的盐酸体积为
 。
。
③下列操作中,可能使所测盐酸溶液的浓度值偏低的是
A.碱式滴定管末用标准氢氧化钠溶液润洗就直接注入标准溶液
B.碱式滴定管在滴定前有气泡,滴定后气泡消失
C.读取氢氧化钠体积时,滴定结束时俯视读数
D.滴定前盛放盐酸溶液的锥形瓶用蒸馏水洗净后没有干燥
您最近一年使用:0次
2023-01-08更新
|
179次组卷
|
2卷引用:广东省广州中学2022-2023学年高二上学期期末考试化学试题
2022·全国·模拟预测
名校
3 . 用下列装置能达到实验目的的是
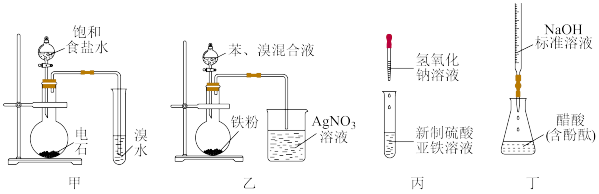

| A.用装置甲证明乙炔可使溴水褪色 |
| B.用装置乙验证苯与液溴的反应属于取代反应 |
| C.用装置丙制备氢氧化亚铁并观察其颜色 |
| D.用装置丁测定醋酸的浓度 |
您最近一年使用:0次
解题方法
4 . 某研究性学习小组为了探究醋酸的电离情况,进行了如下实验:
(1)取冰醋酸配制250 mL 0.4 mol·L-1的醋酸溶液,用0.4 mol·L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
①将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如右图所示。则稀释过程中溶液的pH由大到小的顺序______ (填字母)。

②配制250 mL 0.4 mol·L-1 醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和____________ 。
③为标定该醋酸溶液的准确浓度,用0.2000 mol·L-1的NaOH溶液对20.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
该醋酸溶液的准确浓度为_____________ (保留小数点后四位),上述标定过程中,造成测定结果偏高的原因可能是_______________ (多选、错选不得分)。
a.未用标准液润洗碱式滴定管
b.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
c.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
d.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
(2)该小组同学探究浓度对醋酸电离程度的影响时,用pH计测定25℃时不同浓度的醋酸的pH,其结果如下:
①根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是______________________________________________________________ 。
②简述用pH试纸测 0.1mol·L-1 醋酸溶液pH的方法___________ 。
③利用水解理论设计实验证明醋酸的酸性比碳酸的强:______________________ 。
(1)取冰醋酸配制250 mL 0.4 mol·L-1的醋酸溶液,用0.4 mol·L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
①将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如右图所示。则稀释过程中溶液的pH由大到小的顺序

②配制250 mL 0.4 mol·L-1 醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和
③为标定该醋酸溶液的准确浓度,用0.2000 mol·L-1的NaOH溶液对20.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
a.未用标准液润洗碱式滴定管
b.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
c.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
d.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
(2)该小组同学探究浓度对醋酸电离程度的影响时,用pH计测定25℃时不同浓度的醋酸的pH,其结果如下:
| 醋酸浓度( mol·L-1) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
②简述用pH试纸测 0.1mol·L-1 醋酸溶液pH的方法
③利用水解理论设计实验证明醋酸的酸性比碳酸的强:
您最近一年使用:0次
2017-12-17更新
|
301次组卷
|
4卷引用:广东省普宁市华美实验学校2017-2018学年高二上学期第二次月考化学试题
解题方法
5 . 锡及其化合物在生产、生活中有着重要的用途。已知:Sn的熔点为231 ℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为-33 ℃、沸点为114 ℃。请按要求回答下列相关问题:
(1)元素锡比同主族碳的周期数大3,锡的原子序数为________ 。
(2)用于微电子器件生产的锡粉纯度测定:
①取1.19 g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;
②加入过量的Fe2(SO4)3;
③用0.1 000 mol/L K2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00 mL。步骤②中加入Fe2(SO4)3的作用是__________________ ;此锡粉样品中锡的质量分数:____________ 。
(3)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:
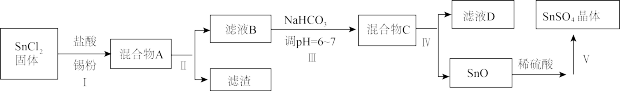
①步骤Ⅰ加入Sn粉的作用:____________________ 及调节溶液pH。
②步骤Ⅱ用到的玻璃仪器有烧杯、________________________ 。
③步骤Ⅲ生成SnO的离子方程式:__________________________ 。
④步骤Ⅳ中检验SnO是否洗涤干净的操作是___________________ ,证明已洗净。
⑤步骤Ⅴ操作依次为___________________ 、过滤、洗涤、低温干燥。
(4)SnCl4蒸气遇氨及水汽呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为:_____________ 。实验室欲用下图装置制备少量SnCl4(夹持装置略),该装置存在明显缺陷,改进方法是_______________
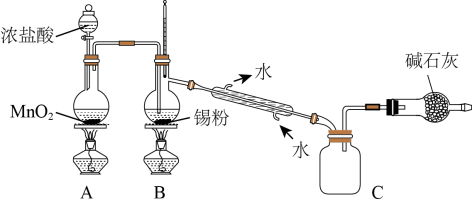
(5)利用改进后的装置进行实验,当开始装置C中收集到有SnCl4时即可熄灭B处酒精灯,反应仍可持续进行的理由是______________________ 。
(1)元素锡比同主族碳的周期数大3,锡的原子序数为
(2)用于微电子器件生产的锡粉纯度测定:
①取1.19 g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;
②加入过量的Fe2(SO4)3;
③用0.1 000 mol/L K2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00 mL。步骤②中加入Fe2(SO4)3的作用是
(3)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:
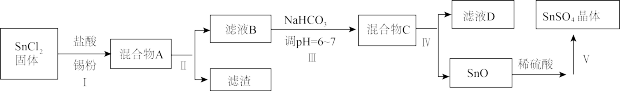
①步骤Ⅰ加入Sn粉的作用:
②步骤Ⅱ用到的玻璃仪器有烧杯、
③步骤Ⅲ生成SnO的离子方程式:
④步骤Ⅳ中检验SnO是否洗涤干净的操作是
⑤步骤Ⅴ操作依次为
(4)SnCl4蒸气遇氨及水汽呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为:

(5)利用改进后的装置进行实验,当开始装置C中收集到有SnCl4时即可熄灭B处酒精灯,反应仍可持续进行的理由是
您最近一年使用:0次
2016-12-09更新
|
256次组卷
|
4卷引用:2017届广东省华侨中学高三上学期摸底考试理综化学试卷
名校
6 . 已知常温时CH3COOH的电离平衡常数为Ka,该温度下向20mL0.1 mol/L CH3COOH溶液中逐滴加入0.1 mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法不正确 的是
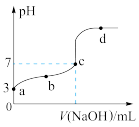

| A.d点表示的溶液中c(OH-)>c(H+) |
| B.该滴定实验可以用紫色石蕊试液做指示剂 |
| C.由图可知0.1 mol/L CH3COOH溶液pH=3 |
D.b、c点表示的溶液中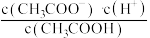 的值相等 的值相等 |
您最近一年使用:0次
2023-11-21更新
|
145次组卷
|
2卷引用:广东省梅州市大埔县虎山中学2023-2024学年高二上学期10月期中考试化学试题
名校
7 . 纯过氧化氢( )是淡蓝色的黏稠液体,可与水以任意比混合,水溶液俗称双氧水,为无色透明液体,用途广泛。回答下列问题:
)是淡蓝色的黏稠液体,可与水以任意比混合,水溶液俗称双氧水,为无色透明液体,用途广泛。回答下列问题:
(1)生产双氧水带采用蒽醌法,其反应原理和生产流程如图所示:

写出反应的化学方程式:___________ 。
(2)该兴趣小组的同学查阅资料后发现 为二元弱酸,
为二元弱酸, ,
, 。
。
①写出 在水溶液中的电离方程式:
在水溶液中的电离方程式:___________ 。
②如果常温下 溶液
溶液 ,
, 的酸式酸根离子与
的酸式酸根离子与 的浓度比为
的浓度比为___________ 。
(3)①同学们用装有 的酸性
的酸性 标准溶液的
标准溶液的___________ (填滴定管名称)滴定某试样中过氧化氢的含量。反应的离子方程式为___________ 。
②取 试样置于锥形瓶中,用酸性
试样置于锥形瓶中,用酸性 标准溶液测定,当
标准溶液测定,当___________ (填写滴定达到终点的现象),重复滴定两次,每次消耗的酸性 标准溶液体积如下表所示:
标准溶液体积如下表所示:
则试样中过氧化氢的浓度为___________  。
。
(4)向滴加了酚酞的NaOH溶液中加入 后,溶液中红色消失。关于褪色原因,甲同学认为
后,溶液中红色消失。关于褪色原因,甲同学认为 是二元弱酸,消耗了
是二元弱酸,消耗了 使红色消失;乙同学认为
使红色消失;乙同学认为 具有漂白性使溶液褪色(生成了其他物质)。请设计个简单的实验方案判断甲、乙同学的说法是否正确:
具有漂白性使溶液褪色(生成了其他物质)。请设计个简单的实验方案判断甲、乙同学的说法是否正确:___________ 。
 )是淡蓝色的黏稠液体,可与水以任意比混合,水溶液俗称双氧水,为无色透明液体,用途广泛。回答下列问题:
)是淡蓝色的黏稠液体,可与水以任意比混合,水溶液俗称双氧水,为无色透明液体,用途广泛。回答下列问题:(1)生产双氧水带采用蒽醌法,其反应原理和生产流程如图所示:

写出反应的化学方程式:
(2)该兴趣小组的同学查阅资料后发现
 为二元弱酸,
为二元弱酸, ,
, 。
。①写出
 在水溶液中的电离方程式:
在水溶液中的电离方程式:②如果常温下
 溶液
溶液 ,
, 的酸式酸根离子与
的酸式酸根离子与 的浓度比为
的浓度比为(3)①同学们用装有
 的酸性
的酸性 标准溶液的
标准溶液的②取
 试样置于锥形瓶中,用酸性
试样置于锥形瓶中,用酸性 标准溶液测定,当
标准溶液测定,当 标准溶液体积如下表所示:
标准溶液体积如下表所示:| 第一次 | 第二次 | 第三次 | |
| 体积 |  |  |  |
 。
。(4)向滴加了酚酞的NaOH溶液中加入
 后,溶液中红色消失。关于褪色原因,甲同学认为
后,溶液中红色消失。关于褪色原因,甲同学认为 是二元弱酸,消耗了
是二元弱酸,消耗了 使红色消失;乙同学认为
使红色消失;乙同学认为 具有漂白性使溶液褪色(生成了其他物质)。请设计个简单的实验方案判断甲、乙同学的说法是否正确:
具有漂白性使溶液褪色(生成了其他物质)。请设计个简单的实验方案判断甲、乙同学的说法是否正确:
您最近一年使用:0次
2020·浙江·模拟预测
8 . 室温下,向20.00mL0.1000mol•L-1盐酸中滴加0.1000mol•L-1NaOH溶液,溶液的pH随NaOH溶液体积的变化如图。已知lg5≈0.7。下列说法不正确的是
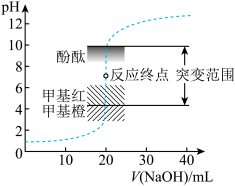
| A.NaOH与盐酸恰好完全反应时,pH=7 |
| B.选择变色范围在pH突变范围内的指示剂,可减小实验误差 |
| C.选择甲基红指示反应终点,误差比甲基橙的大 |
| D.V(NaOH)=30.00mL时,pH≈12.3 |
您最近一年使用:0次
2023-10-21更新
|
877次组卷
|
51卷引用:广东省化州市第一中学2019-2020学年高二4月线上统一测试化学试题
广东省化州市第一中学2019-2020学年高二4月线上统一测试化学试题(已下线)浙江省2020年1月选考(学考)化学试题2020年浙江省高考化学试卷(1月选考)浙江省丽水市松阳县第二中学2019-2020学年高二4月线上教学检测化学试题江苏省启东中学2020-2021学年高二上学期第一次月考化学试题湖南省怀化市2020-2021学年高二上学期10月联考化学试题(已下线)【浙江新东方】【2020】【高二上】【期中】【HD-LP409】【化学】(已下线)【浙江新东方】99(已下线)小题必刷31 酸碱中和滴定及拓展应用——2021年高考化学一轮复习小题必刷(通用版本)山东省济南市大学城实验高级中学2021届高三1月阶段性考试化学试题(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)广西贵港市覃塘区覃塘高级中学2020-2021学年高二下学期3月月考化学试题浙江省杭州市长征中学2020-2021学年高二下学期第二学期阶段性练习化学试题选择性必修1(SJ)专题3专题培优专练选择性必修1 专题3素养检测(已下线)考点24 水的电离和溶液的酸碱性-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点24 水的电离和溶液的酸碱性-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)课时41 酸碱中和滴定及拓展应用-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题3.2.2 酸碱中和滴定和pH的计算(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)湖北省麻城市实验高级中学2021-2022学年高二上学期9月月考化学(B卷)试卷内蒙古鄂尔多斯市第一中学2021-2022学年高二上学期第一次月考化学试题(已下线)3.2.2 酸碱中和滴定和pH的计算-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)专题14.水溶液中的离子平衡-十年(2012-2021)高考化学真题分项汇编(浙江专用)安徽师范大学附属中学2021-2022学年高二上学期期中考查化学试题浙江省浙北G2(湖州中学、嘉兴一中)2021-2022学年高二上学期期中联考化学试题(已下线)专题25 水的电离和溶液的酸碱性(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练(已下线)专题12 水溶液中的离子平衡-备战2022年高考化学学霸纠错(全国通用)内蒙古霍林郭勒市第一中学2021-2022学年高二上学期期中考试化学试题(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题18 酸碱混合图像为载体考查离子平衡-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)专题4 滴定终点专练(已下线)考点27 水的电离和溶液的pH-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第31练 水的电离和溶液的pH-2023年高考化学一轮复习小题多维练(全国通用)陕西省汉中中学2021-2022学年高二上学期第四次月考化学试题(已下线)第24讲 水的电离和溶液的pH(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第22讲 水的电离与溶液的pH(讲)-2023年高考化学一轮复习讲练测(新教材新高考)湖南省株洲市五雅中学2022-2023学年高二上学期11月期中考试化学试题 广西钦州市2022-2023学年高二上学期第2次教学质量监测化学试卷(已下线)题型133 酸碱中和滴定实验及误差分析(已下线)第八章 水溶液中的离子反应与平衡 第48练 酸碱中和反应及中和滴定上海市华东政法大学附属中学2022-2023学年高二下学期期中考试(等级考)化学试题(已下线)第12讲 酸碱中和滴定和氧化还原反应滴定-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)作业(十六) 酸碱中和滴定(已下线)考点27 水的电离与溶液的pH(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第3讲 酸碱中和滴定河北省衡水市第二中学2023-2024学年高三上学期学科素养评估(三调)化学试题【定心卷】3.2.3 酸碱中和滴定随堂练习-人教版2023-2024学年选择性必修1江苏省无锡市锡东高级中学2023-2024学年高二下学期期中考试化学试题天津市和平区2023-2024学年高三下学期第二次质量调查化学试卷
名校
解题方法
9 . 常温下,用0.1000 mol·L NaOH溶液滴定20.00 mL 0.1000 mol·L
NaOH溶液滴定20.00 mL 0.1000 mol·L
 溶液,所得滴定曲线如图,下列说法中正确的是
溶液,所得滴定曲线如图,下列说法中正确的是

 NaOH溶液滴定20.00 mL 0.1000 mol·L
NaOH溶液滴定20.00 mL 0.1000 mol·L
 溶液,所得滴定曲线如图,下列说法中正确的是
溶液,所得滴定曲线如图,下列说法中正确的是
A.点①所示溶液中: |
B.点②所示溶液中: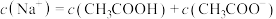 |
C.点③所示溶液中: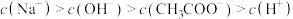 |
D.点②所示的溶液中: |
您最近一年使用:0次
名校
解题方法
10 . 常温下,向20mL0.1mol/L一元碱MOH溶液中滴加等浓度的一元酸HX溶液,滴定过程中溶液pH值的变化曲线如下图所示,已知4<m<6,下列说法不正确的是

| A.该滴定过程中应选用酚酞作指示剂 | B.一元酸HX的Ka=5×10-5 |
| C.溶液中水的电离程度:b>c>a | D.c点溶液中:c(M+)>c(X-)>c(H+)>c(OH-) |
您最近一年使用:0次
2024-01-15更新
|
340次组卷
|
4卷引用:广东省梅州市大埔县虎山中学2023-2024学年高二下学期4月期中考试化学试题
广东省梅州市大埔县虎山中学2023-2024学年高二下学期4月期中考试化学试题2024届陕西省宝鸡市高考模拟监测(一) 理科综合试题湖南省常德市第一中学2023-2024学年高二上学期期末考试化学试题(已下线)专题07 水溶液中的离子反应与平衡-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)



