1 . 维生素C(C6H8O6,M=176)具有重要生理调节功能,在酸性介质中较为稳定,在碱性溶液中易被空气氧化。维生素C通常用I2标准溶液进行滴定,反应原理是:C6H8O6+I2═C6H6O6+2H++2I﹣。回答下列问题:
(1)I2标准溶液的配制与标定
①配制:配制一定浓度的I2标准溶液。碘水见光易分解,配制好的I2标准溶液应保存在___________ 色试剂瓶中。
②标定:标定碘液的Na2S2O3溶液在酸性条件下不稳定,溶液容易出现浑浊,该反应的离子方程式为___________ ,因此配制时往往调溶液至碱性。用Na2S2O3标准溶液标定①中配制的I2标准溶液,计算得I2标准溶液浓度为0.05000mol•L﹣1。
(2)维生素C含量的测定
准确称取2.000g维生素C药片,磨成粉末,配制成250mL溶液,取25.00mL至锥形瓶,用I2标准溶液进行滴定,用淀粉作指示剂。
①维生素C很容易被氧气氧化,因此需往该待测液中加入___________ 来保存。
A.醋酸溶液 B.硝酸溶液 C.碳酸钠溶液 D.烧碱溶液
②确定时应选择___________ (填“酸式“或“碱式”)滴定管盛装I2标准溶液。滴定终点的现象是___________ 。
③维C含量的计算
实验过程中测得数据如表:
根据以上数据可得,该药片中维C的质量分数为___________ 。
(3)实际测得药片中维生素C含量比说明书中的含量更高,可能的原因是___________(填标号)。
(1)I2标准溶液的配制与标定
①配制:配制一定浓度的I2标准溶液。碘水见光易分解,配制好的I2标准溶液应保存在
②标定:标定碘液的Na2S2O3溶液在酸性条件下不稳定,溶液容易出现浑浊,该反应的离子方程式为
(2)维生素C含量的测定
准确称取2.000g维生素C药片,磨成粉末,配制成250mL溶液,取25.00mL至锥形瓶,用I2标准溶液进行滴定,用淀粉作指示剂。
①维生素C很容易被氧气氧化,因此需往该待测液中加入
A.醋酸溶液 B.硝酸溶液 C.碳酸钠溶液 D.烧碱溶液
②确定时应选择
③维C含量的计算
实验过程中测得数据如表:
| 编号 | 1 | 2 | 3 | 4 |
| V(I2标准溶液)/mL | 20.80 | 20.81 | 21.70 | 20.79 |
(3)实际测得药片中维生素C含量比说明书中的含量更高,可能的原因是___________(填标号)。
| A.盛I2标准溶液的酸式滴定管未进行润洗 |
| B.滴定过程中有少量锥形瓶内液体溅出 |
| C.滴定结束时仰视读数 |
| D.用I2标准溶液滴定时操作过慢 |
您最近一年使用:0次
名校
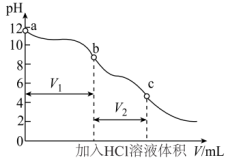
2 . 可用酚酞和甲基橙双指示剂法测定部分变质的烧碱中 的含量。先将部分变质的烧碱配制成一定浓度溶液并加入一种指示剂,用一定浓度的HCl溶液滴定至变色后,再加入另一种指示剂,继续用该HCl溶液滴定至变色,分别记录两个变色点加入HCl溶液体积进行计算。滴定过程中溶液pH的变化如图所示。下列说法错误的是
的含量。先将部分变质的烧碱配制成一定浓度溶液并加入一种指示剂,用一定浓度的HCl溶液滴定至变色后,再加入另一种指示剂,继续用该HCl溶液滴定至变色,分别记录两个变色点加入HCl溶液体积进行计算。滴定过程中溶液pH的变化如图所示。下列说法错误的是
 的含量。先将部分变质的烧碱配制成一定浓度溶液并加入一种指示剂,用一定浓度的HCl溶液滴定至变色后,再加入另一种指示剂,继续用该HCl溶液滴定至变色,分别记录两个变色点加入HCl溶液体积进行计算。滴定过程中溶液pH的变化如图所示。下列说法错误的是
的含量。先将部分变质的烧碱配制成一定浓度溶液并加入一种指示剂,用一定浓度的HCl溶液滴定至变色后,再加入另一种指示剂,继续用该HCl溶液滴定至变色,分别记录两个变色点加入HCl溶液体积进行计算。滴定过程中溶液pH的变化如图所示。下列说法错误的是
| A.指示剂的添加顺序为先加酚酞,后加甲基橙 |
B.b点时溶液中的溶质主要为NaCl和 |
C.若 ,则a点溶液中存在 ,则a点溶液中存在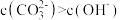 |
D.原固体混合物中碳酸钠的质量分数表示为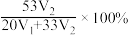 |
您最近一年使用:0次
2021-07-04更新
|
425次组卷
|
2卷引用:广东省茂名市2020-2021学年度下学期高二期末考试化学试题
3 . 工业上,处理低品位黄铜矿[二硫化亚铁铜(CuFeS2)含量较低]常采用生物堆浸法。堆浸所得的溶液可用于制备绿矾(FeSO4·7H2O)和胆矾(CuSO4·5H2O)。相关流程如下图。
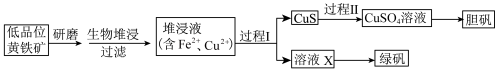
已知:①生物堆浸使用的氧化亚铁硫杆菌(T.f细菌)在pH 1.0~6.0范围内可保持活性。
②金属离子沉淀的pH如下表。
(1)生物堆浸前,需先将矿石进行研磨,目的是__________________ 。
(2)生物堆浸过程的反应在T.f细菌的作用下进行,主要包括两个阶段,第一阶段的反应为:CuFeS2 +4H+ +O2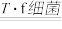 Cu2+ Fe2++ 2S+ 2H2O,第二阶段的反应为Fe2+继续被氧化转变成Fe3+,反应的离子方程式为
Cu2+ Fe2++ 2S+ 2H2O,第二阶段的反应为Fe2+继续被氧化转变成Fe3+,反应的离子方程式为__________ 。
(3)结合已知推断:生物堆浸过程中,应控制溶液的pH在__________ 范围内。
(4)过程I中,加入Na2S2O3固体会还原堆浸液中的Fe3+, 得到溶液X。为判断堆浸液中Fe3+是否被还原完全,可取少量溶液X,向其中加入_____________ 试剂(填试剂的化学式),观察溶液颜色变化。
(5)过程II中,用H2O2和稀硫酸处理后,CuS完全溶解 ,用离子方程式表示H2O2的作用是________ 。
(6)绿矾的纯度可通过KMnO4滴定法测定。取m g绿矾晶体,加适量稀硫酸溶解。用物质的量浓度为c mol/L的KMnO4溶液滴定。至恰好完全反应时,消耗KMnO4溶液的体积为V mL。绿矾晶体质量分数的计算式为______ 。(已知: FeSO4•7H2O的摩尔质量为278 g/mol )

已知:①生物堆浸使用的氧化亚铁硫杆菌(T.f细菌)在pH 1.0~6.0范围内可保持活性。
②金属离子沉淀的pH如下表。
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀时的pH | 1.5 | 4.2 | 6.3 |
| 完全沉淀时的pH | 2.8 | 6.7 | 8.3 |
(2)生物堆浸过程的反应在T.f细菌的作用下进行,主要包括两个阶段,第一阶段的反应为:CuFeS2 +4H+ +O2
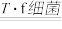 Cu2+ Fe2++ 2S+ 2H2O,第二阶段的反应为Fe2+继续被氧化转变成Fe3+,反应的离子方程式为
Cu2+ Fe2++ 2S+ 2H2O,第二阶段的反应为Fe2+继续被氧化转变成Fe3+,反应的离子方程式为(3)结合已知推断:生物堆浸过程中,应控制溶液的pH在
(4)过程I中,加入Na2S2O3固体会还原堆浸液中的Fe3+, 得到溶液X。为判断堆浸液中Fe3+是否被还原完全,可取少量溶液X,向其中加入
(5)过程II中,用H2O2和稀硫酸处理后,CuS
(6)绿矾的纯度可通过KMnO4滴定法测定。取m g绿矾晶体,加适量稀硫酸溶解。用物质的量浓度为c mol/L的KMnO4溶液滴定。至恰好完全反应时,消耗KMnO4溶液的体积为V mL。绿矾晶体质量分数的计算式为
您最近一年使用:0次
2020-11-06更新
|
454次组卷
|
3卷引用:2023年广东省广州市高三化学冲刺训练题(三)
10-11高三下·广东茂名·阶段练习
4 . 过氧化尿素[CO(NH2)2·H2O2]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域。其合成如下:

试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25—30℃,其主要原因是___________________________________ 。
(2)从母液中分离出H2O2和尿素,采用的操作是___________ 。
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O2 34%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容。准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000 mol/L KMnO4标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应)。
①KMnO4溶液应盛放在________ 式(选填:“酸”、“碱”)滴定管中。
②完成并配平方程式:__ MnO4-+ ___ H2O2+___ H+=___ Mn2++ ____ H2O+________
③根据滴定结果,可确定产品中活性氧的质量分数为:___________ 。
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量______ (选填:“偏高”、“偏低”或“不变”)。
⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为_________ 。

试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25—30℃,其主要原因是
(2)从母液中分离出H2O2和尿素,采用的操作是
a.盐析、过滤 b.分液、过滤 c.减压蒸馏、结晶 d.常压蒸馏、萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O2 34%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容。准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000 mol/L KMnO4标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应)。
①KMnO4溶液应盛放在
②完成并配平方程式:
③根据滴定结果,可确定产品中活性氧的质量分数为:
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量
⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为
您最近一年使用:0次
名校
解题方法
5 . 化学实验室中常常需要配制溶液进行物质的制备与及物质成分的定量测定实验。
Ⅰ.制备 胶体
胶体
(1)实验室配制饱和 溶液时,将
溶液时,将 晶体溶于浓盐酸中,结合勒夏特列原理分析其操作的原因
晶体溶于浓盐酸中,结合勒夏特列原理分析其操作的原因___________ 。
(2)把少量饱和 溶液滴入大量沸水中,加热至溶液呈红褐色,制备
溶液滴入大量沸水中,加热至溶液呈红褐色,制备 胶体。这一制备实验中促进
胶体。这一制备实验中促进 水解的措施:
水解的措施:___________ 。若把少量饱和 溶液直接蒸干并灼烧,得到的固体物质是
溶液直接蒸干并灼烧,得到的固体物质是___________ (填化学式)。
Ⅱ.已知某 试样中含有
试样中含有 杂质,为测定试样中
杂质,为测定试样中 的质量分数,进行如下实验:
的质量分数,进行如下实验:
①称量 样品溶于水,配成
样品溶于水,配成 溶液;
溶液;
②准确量取所配溶液于维形瓶中;
③滴加几滴酚酞溶液;
④用 的盐酸标准液滴定三次,每次消耗盐酸的体积记录如下:
的盐酸标准液滴定三次,每次消耗盐酸的体积记录如下:
(3)准确量取 待测液需要使用的仪器是
待测液需要使用的仪器是___________
(4)滴定达到终点的标志是滴入最后半滴标准液,___________ 。
(5)试样中 的质量分数为
的质量分数为___________ 。
(6)若出现下列情况,测定结果偏高的是___________ (填序号)。
a.滴定前用蒸馏水冲洗锥形瓶
b.在振荡锥形瓶时不慎将瓶内溶液溅出
c.在滴定过程中不慎将数滴酸液滴在锥形瓶外
d.酸式滴定管滴至终点时,俯视读数
Ⅰ.制备
 胶体
胶体(1)实验室配制饱和
 溶液时,将
溶液时,将 晶体溶于浓盐酸中,结合勒夏特列原理分析其操作的原因
晶体溶于浓盐酸中,结合勒夏特列原理分析其操作的原因(2)把少量饱和
 溶液滴入大量沸水中,加热至溶液呈红褐色,制备
溶液滴入大量沸水中,加热至溶液呈红褐色,制备 胶体。这一制备实验中促进
胶体。这一制备实验中促进 水解的措施:
水解的措施: 溶液直接蒸干并灼烧,得到的固体物质是
溶液直接蒸干并灼烧,得到的固体物质是Ⅱ.已知某
 试样中含有
试样中含有 杂质,为测定试样中
杂质,为测定试样中 的质量分数,进行如下实验:
的质量分数,进行如下实验:①称量
 样品溶于水,配成
样品溶于水,配成 溶液;
溶液;②准确量取所配溶液于维形瓶中;
③滴加几滴酚酞溶液;
④用
 的盐酸标准液滴定三次,每次消耗盐酸的体积记录如下:
的盐酸标准液滴定三次,每次消耗盐酸的体积记录如下:| 滴定序号 | 待测液体积/ | 所消耗盐酸标准液的体积/ | |
| 滴定前读数 | 滴定后读数 | ||
| 1 | 25.00 | 0.50 | 20.60 |
| 2 | 25.00 | 6.00 | 26.00 |
| 3 | 25.00 | 1.10 | 21.00 |
 待测液需要使用的仪器是
待测液需要使用的仪器是(4)滴定达到终点的标志是滴入最后半滴标准液,
(5)试样中
 的质量分数为
的质量分数为(6)若出现下列情况,测定结果偏高的是
a.滴定前用蒸馏水冲洗锥形瓶
b.在振荡锥形瓶时不慎将瓶内溶液溅出
c.在滴定过程中不慎将数滴酸液滴在锥形瓶外
d.酸式滴定管滴至终点时,俯视读数
您最近一年使用:0次
名校
解题方法
6 . 已知某烧碱样品中含有NaCl杂质,为测定该样品中NaOH的质量分数,进行如下实验:
①称量1.00g样品溶于水配成250mL溶液:
②用碱式滴定管准确量取25.00mL所配溶液于锥形瓶中,滴加2—3滴指示剂:
③用 的标准盐酸滴定并重复三次,每次实验数据记录如下:
的标准盐酸滴定并重复三次,每次实验数据记录如下:
请回答下列问题:
(1)实验步骤②中所滴加的指示剂是___________ 。
(2)排除碱式滴定管胶管中气泡的方法是__________ (填字母)。

(3)在该实验的滴定过程中用左手控制_______ 。(填仪器及部位),眼睛________ ,直至滴定终点。
(4)判断达到滴定终点时的现象为_____________________________________________ 。
(5)若出现下列情况,导致测定结果偏高的是___________ (填序号)。
a.滴定前用蒸馏水冲洗锥形瓶
b.滴定过程中振荡锥形瓶时不慎使瓶内溶液溅出
c.滴定过程中不慎将数滴酸液滴在锥形瓶外
d.酸式滴定管中在滴定前有气泡,滴定后气泡消失
e.滴定前仰视读数,滴定后俯视读数
f.酸式滴定管在使用前没有用标准液润洗
(6)通过计算可知该烧碱样品的纯度为___________ 。
①称量1.00g样品溶于水配成250mL溶液:
②用碱式滴定管准确量取25.00mL所配溶液于锥形瓶中,滴加2—3滴指示剂:
③用
 的标准盐酸滴定并重复三次,每次实验数据记录如下:
的标准盐酸滴定并重复三次,每次实验数据记录如下:滴定序号 | 待测液体积/mL | 消耗盐酸的体积/mL | |
滴定前 | 滴定后 | ||
1 2 3 | 25.00 25.00 25.00 | 0.50 6.00 1.10 | 20.60 26.00 21.00 |
(1)实验步骤②中所滴加的指示剂是
(2)排除碱式滴定管胶管中气泡的方法是

(3)在该实验的滴定过程中用左手控制
(4)判断达到滴定终点时的现象为
(5)若出现下列情况,导致测定结果偏高的是
a.滴定前用蒸馏水冲洗锥形瓶
b.滴定过程中振荡锥形瓶时不慎使瓶内溶液溅出
c.滴定过程中不慎将数滴酸液滴在锥形瓶外
d.酸式滴定管中在滴定前有气泡,滴定后气泡消失
e.滴定前仰视读数,滴定后俯视读数
f.酸式滴定管在使用前没有用标准液润洗
(6)通过计算可知该烧碱样品的纯度为
您最近一年使用:0次
名校
7 . 滴定实验是化学学科中重要的定量实验。
Ⅰ.酸碱中和滴定——已知某NaOH试样中含有NaCl杂质,为测定试样中NaOH的质量分数,进行如下步骤实验:
①称量1.00g样品溶于水,配成250mL溶液;
②准确量取25.00mL所配溶液于锥形瓶中;
③滴加几滴甲基橙指示剂;
④用0.10mol/L的标准盐酸滴定三次,每次消耗盐酸的体积记录如下:
(1)该酸碱中和滴定(题干中②③④步)所需仪器有___________ (填字母)。
A.酸式滴定管(50mL) B.碱式滴定管(50mL) C.量筒(10mL) D.铁架台 E.滴定管夹 F.玻璃棒
(2)排去碱式滴定管中气泡的方法应采用操作___________ 。

(3)滴定达到终点的现象是___________ 。
(4)试样中NaOH的质量分数为___________ 。
(5)若出现下列情况,测定结果偏高的是___________ 。
a.滴定前用蒸馏水冲洗锥形瓶
b.酸式滴定管滴至终点时,俯视读数
c.酸式滴定管用蒸馏水洗后,未用标准液润洗
d.酸式滴定管尖嘴部分有气泡,滴定后消失
Ⅱ.氧化还原滴定—取草酸(H2C2O4,弱酸)溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol·L-1的高锰酸钾溶液滴定。
(6)发生反应的离子方程式为:___________ 。
(7)滴定时,KMnO4溶液应装在酸式滴定管中,滴定终点时锥形瓶内的颜色变化为:由___________ 变为___________ 。
Ⅰ.酸碱中和滴定——已知某NaOH试样中含有NaCl杂质,为测定试样中NaOH的质量分数,进行如下步骤实验:
①称量1.00g样品溶于水,配成250mL溶液;
②准确量取25.00mL所配溶液于锥形瓶中;
③滴加几滴甲基橙指示剂;
④用0.10mol/L的标准盐酸滴定三次,每次消耗盐酸的体积记录如下:
| 滴定序号 | 待测液体积(mL) | 消耗盐酸标准的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 25.00 | 0.50 | 20.60 |
| 2 | 25.00 | 6.00 | 26.00 |
| 3 | 25.00 | 1.10 | 21.00 |
A.酸式滴定管(50mL) B.碱式滴定管(50mL) C.量筒(10mL) D.铁架台 E.滴定管夹 F.玻璃棒
(2)排去碱式滴定管中气泡的方法应采用操作

(3)滴定达到终点的现象是
(4)试样中NaOH的质量分数为
(5)若出现下列情况,测定结果偏高的是
a.滴定前用蒸馏水冲洗锥形瓶
b.酸式滴定管滴至终点时,俯视读数
c.酸式滴定管用蒸馏水洗后,未用标准液润洗
d.酸式滴定管尖嘴部分有气泡,滴定后消失
Ⅱ.氧化还原滴定—取草酸(H2C2O4,弱酸)溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol·L-1的高锰酸钾溶液滴定。
(6)发生反应的离子方程式为:
(7)滴定时,KMnO4溶液应装在酸式滴定管中,滴定终点时锥形瓶内的颜色变化为:由
您最近一年使用:0次
2023-06-07更新
|
711次组卷
|
5卷引用:广东省华南师范大学附属中学2022-2023学年高二上学期1月期末化学试题
名校
8 . I、某学生欲用已知物质的量浓度的盐酸来测定未知物质的最浓度的氢氧化钠溶液时,选择酚酞作指示剂。请填写下列空白。
(1)用标准的盐酸溶液滴定待测的氯氧化钠溶液时,标准的盐酸溶液应该装在______ (填仪器名称)中;滴定达到终点的现象为:______ 。
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是______ (填序号)。
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)某学生根据三次实验分别记录有关数据如表:
请选用数据计算该氢氧化钠溶液的物质的量浓度: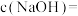
______ mol/L(保留小数点后4位)
Ⅱ、某学习小组用“间接碘量法”测定含有晶体的试样(不含能与厂发生反应的氧化性杂质)的纯度。过程如下:取0.36 g试样溶于水,加过量KI固体,充分反应,生成白色沉淀 。用0.1000 mol/L
。用0.1000 mol/L  标准溶液滴定,到达滴定终点时,消耗
标准溶液滴定,到达滴定终点时,消耗 标准溶液20.00 mL。
标准溶液20.00 mL。
已知:① ②
②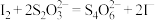
(4)选用______ 作滴定指示剂,试样中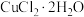 的质量分数为
的质量分数为______ 。(保留小数点后一位)
(1)用标准的盐酸溶液滴定待测的氯氧化钠溶液时,标准的盐酸溶液应该装在
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)某学生根据三次实验分别记录有关数据如表:
滴定次数 | 待测NaOH溶液的体积/mL | 0.1000 mol/L盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
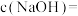
Ⅱ、某学习小组用“间接碘量法”测定含有晶体的试样(不含能与厂发生反应的氧化性杂质)的纯度。过程如下:取0.36 g试样溶于水,加过量KI固体,充分反应,生成白色沉淀
 。用0.1000 mol/L
。用0.1000 mol/L  标准溶液滴定,到达滴定终点时,消耗
标准溶液滴定,到达滴定终点时,消耗 标准溶液20.00 mL。
标准溶液20.00 mL。已知:①
 ②
②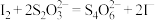
(4)选用
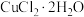 的质量分数为
的质量分数为
您最近一年使用:0次
名校
9 . 某兴趣小组利用图甲装置(夹持装置略)收集某葡萄酒中的 ,并对其含量进行测定。某标准中规定葡萄酒中
,并对其含量进行测定。某标准中规定葡萄酒中 最大使用量为
最大使用量为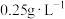 。
。

回答下列问题:
(1)仪器
 的名称是
的名称是 的进口为
的进口为 ”或“
”或“ ”)。
”)。(2)
 中加入
中加入 葡萄酒和适量稀硫酸,加热使
葡萄酒和适量稀硫酸,加热使 全部逸出并与仪器
全部逸出并与仪器 中
中 完全反应。仪器
完全反应。仪器 中发生反应的化学方程式为
中发生反应的化学方程式为(3)除去
 中过量的
中过量的 ,然后用
,然后用 标准溶液进行滴定,滴定前排气泡时,应选择图乙中的
标准溶液进行滴定,滴定前排气泡时,应选择图乙中的 滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积
滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积a.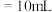 b.
b.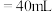 c.
c.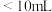 d.
d.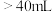
(4)判断滴定达到终点的现象为
 溶液
溶液 ,该葡萄酒中
,该葡萄酒中 含量为
含量为 。
。(5)下列操作会导致实验结果偏低的是
a.滴定管在装液前未用标准溶液润洗
b.滴定过程中,锥形瓶振荡得太剧烈,锥形瓶内有液滴浅出
c.达到滴定终点时,仰视读数
d.装标准溶液的滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
您最近一年使用:0次
名校
10 . 氧化还原滴定实验与中和滴定原理相似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之),也是分析化学中常用的分析手段。
I.现有0.1mol/L酸性 和未知浓度的
和未知浓度的 水溶液。反应离子方程式是:
水溶液。反应离子方程式是: 。
。
请回答下列问题:
(1)该滴定实验不需要用到的仪器有___________(填序号)。
(2)滴定时是否需要添加指示剂_________ (填“是”或“否”),并说明理由:__________________ 。
II.用氧化还原滴定方法测定粗品中 的质量分数。
的质量分数。
实验步骤:称取6g粗品配制250mL的溶液待用。用酸式滴定管取25.00mL0.01mol/L 溶液于锥形瓶中,然后加入过量的KI溶液并酸化,加几滴淀粉溶液,立即用配制的
溶液于锥形瓶中,然后加入过量的KI溶液并酸化,加几滴淀粉溶液,立即用配制的 溶液滴定至终点(反应为
溶液滴定至终点(反应为 ),消耗
),消耗 溶液25.00mL。
溶液25.00mL。
(3)向 溶液中加入过量的KI溶液并酸化,
溶液中加入过量的KI溶液并酸化, 被还原成
被还原成 ,写出该反应的离子方程式:
,写出该反应的离子方程式:____ 。
(4)用 溶液滴定至终点的现象为:
溶液滴定至终点的现象为:___________ 。
(5)粗品中 的质量分数为
的质量分数为____________ 。
(6)下列操作中,可能使所测样品纯度偏高的是_______。
I.现有0.1mol/L酸性
 和未知浓度的
和未知浓度的 水溶液。反应离子方程式是:
水溶液。反应离子方程式是: 。
。请回答下列问题:
(1)该滴定实验不需要用到的仪器有___________(填序号)。
| A.酸式滴定管(50mL) | B.碱式滴定管(50mL) |
| C.锥形瓶 | D.量筒(10mL) |
II.用氧化还原滴定方法测定粗品中
 的质量分数。
的质量分数。实验步骤:称取6g粗品配制250mL的溶液待用。用酸式滴定管取25.00mL0.01mol/L
 溶液于锥形瓶中,然后加入过量的KI溶液并酸化,加几滴淀粉溶液,立即用配制的
溶液于锥形瓶中,然后加入过量的KI溶液并酸化,加几滴淀粉溶液,立即用配制的 溶液滴定至终点(反应为
溶液滴定至终点(反应为 ),消耗
),消耗 溶液25.00mL。
溶液25.00mL。(3)向
 溶液中加入过量的KI溶液并酸化,
溶液中加入过量的KI溶液并酸化, 被还原成
被还原成 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(4)用
 溶液滴定至终点的现象为:
溶液滴定至终点的现象为:(5)粗品中
 的质量分数为
的质量分数为(6)下列操作中,可能使所测样品纯度偏高的是_______。
| A.使用的锥形瓶用蒸馏水洗干净后未烘干 |
| B.盛放标准液的滴定管,滴定前有气泡,滴定后气泡消失 |
| C.用滴定管量取待测液时,未用待测液润洗滴定管 |
| D.用标准液滴定时,滴定前仰视刻度线,滴定终点时俯视刻度线 |
您最近一年使用:0次



