2022·江苏·模拟预测
解题方法
1 . 铁矿石中含铁量的测定是铁元素提炼的基础和前提,目前主要采用重铬酸钾法测定铁矿石中的铁含量,其流程如图所示:
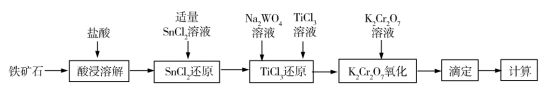
已知:①氧化性顺序: >Fe3+>WO
>Fe3+>WO ;
;
②Sn在溶液中的主要存在形式为Sn2+和SnCl ;
;
③二苯胺磺酸钠可作氧化还原指示剂,氧化型为紫红色,还原型为无色。
回答下列问题:
(1)提高“酸浸溶解”速率可采取的措施有_______ (任写两条)。
(2)“SnCl2还原”过程的离子反应方程式为_______ 。
(3)“SnCl2还原”后溶液仍呈浅黄色,而“TiCl3还原”后溶液呈现蓝色溶液(五价钨溶液为蓝色),则蓝色溶液中铁元素的主要存在形式为_______ ,Na2WO4的作用为_______ 。
(4)滴定前先进行“K2Cr2O7氧化”,即滴加K2Cr2O7溶液至溶液蓝色褪去,请分析该过程的目的是_______ 。
(5)“滴定”过程以二苯胺磺酸钠为指示剂,用酸性K2Cr2O7标准溶液滴定,滴定的反应离子方程式为_______ ;平行滴定5次,其中一组数据异常,所测c(Fe3+)偏大,原因可能是_______ (填标号)。
A.滴定终点读数时仰视滴定管刻度线
B.摇动锥形瓶时有液体溅出
C.未进行“K2Cr2O7氧化”过程就开始滴定
D.加入二苯胺磺酸钠指示剂的量过多
(6)现称取mg铁矿石进行测定,“滴定”时共消耗VmLcmol·L−1K2Cr2O7,则该铁矿石中铁的质量分数为_______ (用含m、c、V的代数式表示)。

已知:①氧化性顺序:
 >Fe3+>WO
>Fe3+>WO ;
;②Sn在溶液中的主要存在形式为Sn2+和SnCl
 ;
;③二苯胺磺酸钠可作氧化还原指示剂,氧化型为紫红色,还原型为无色。
回答下列问题:
(1)提高“酸浸溶解”速率可采取的措施有
(2)“SnCl2还原”过程的离子反应方程式为
(3)“SnCl2还原”后溶液仍呈浅黄色,而“TiCl3还原”后溶液呈现蓝色溶液(五价钨溶液为蓝色),则蓝色溶液中铁元素的主要存在形式为
(4)滴定前先进行“K2Cr2O7氧化”,即滴加K2Cr2O7溶液至溶液蓝色褪去,请分析该过程的目的是
(5)“滴定”过程以二苯胺磺酸钠为指示剂,用酸性K2Cr2O7标准溶液滴定,滴定的反应离子方程式为
A.滴定终点读数时仰视滴定管刻度线
B.摇动锥形瓶时有液体溅出
C.未进行“K2Cr2O7氧化”过程就开始滴定
D.加入二苯胺磺酸钠指示剂的量过多
(6)现称取mg铁矿石进行测定,“滴定”时共消耗VmLcmol·L−1K2Cr2O7,则该铁矿石中铁的质量分数为
您最近一年使用:0次
名校
2 . 碘是人体必需的微量元素,也可用于工业、医药等领域。大量的碘富集于海藻灰(主要成分是NaI)中,因此从海藻灰中提取碘,可有效利用海洋资源。
(1)某兴趣小组以海藻灰为原料进行I2的制备实验。具体步骤如下:将海藻灰加热浸泡后,得到了NaI溶液,将适量Na2SO3固体溶于NaI溶液,再将CuSO4饱和溶液滴入上述溶液中,生成白色CuI沉淀,该反应的离子方程式为___ 。
(2)待I-沉淀完全后,过滤,将沉淀物置于小烧杯中,在搅拌下逐滴加入适量浓HNO3,观察到___ (颜色)气体放出,___ (颜色)晶体析出。该反应的化学方程式为___ 。
(3)用倾析法弃去上清液,固体物质用少量水洗涤后得到粗I2,进一步精制时,选择必需的仪器搭建装置,并按次序排列:___ (夹持装置略)。
A. B.
B. C.
C. D.
D. E.
E. F.
F.
(4)将精制得到的I2配成浓度为cmol•L-1的标准溶液,用来测定某样品中维生素C(相对分子质量为M)的含量。具体操作如下:准确称量ag样品,溶于新煮沸过并冷却至室温的蒸馏水中,煮沸蒸馏水的目的是___ 。用250mL容量瓶定容,使用滴定管量取25.00mL样品溶液于锥形瓶中,再加入10mL1:1醋酸溶液和适量的__ 指示剂,立即用I2标准溶液滴定,溶液显稳定的___ (颜色)即为滴定终点(提示:用指示剂与有关物质发生反应的颜色变化指示化学反应已经完全),消耗I2标准溶液VmL,则样品中维生素C的质量分数是___ (写出表达式)。
已知滴定反应方程式: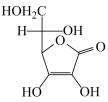 +I2→
+I2→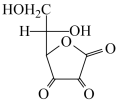 +2HI
+2HI
(1)某兴趣小组以海藻灰为原料进行I2的制备实验。具体步骤如下:将海藻灰加热浸泡后,得到了NaI溶液,将适量Na2SO3固体溶于NaI溶液,再将CuSO4饱和溶液滴入上述溶液中,生成白色CuI沉淀,该反应的离子方程式为
(2)待I-沉淀完全后,过滤,将沉淀物置于小烧杯中,在搅拌下逐滴加入适量浓HNO3,观察到
(3)用倾析法弃去上清液,固体物质用少量水洗涤后得到粗I2,进一步精制时,选择必需的仪器搭建装置,并按次序排列:
A.
 B.
B. C.
C. D.
D. E.
E. F.
F.
(4)将精制得到的I2配成浓度为cmol•L-1的标准溶液,用来测定某样品中维生素C(相对分子质量为M)的含量。具体操作如下:准确称量ag样品,溶于新煮沸过并冷却至室温的蒸馏水中,煮沸蒸馏水的目的是
已知滴定反应方程式:
 +I2→
+I2→ +2HI
+2HI
您最近一年使用:0次
名校
3 . 三草酸合铁酸钾晶体{K3[Fe(C2O4)3]·xH2O)}是一种光敏材料,可用于摄影和蓝色印刷。为测定该晶体中铁的含量,某实验小组做了如下实验:
(1)已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。现称量5.000g三草酸合铁酸钾晶体,配制成250mL溶液。取所配溶液25.00mL于锥形瓶中加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部被氧化成二氧化碳。向反应后的溶液中加入足量锌粉,加热至溶液完全由黄色变为浅绿色时,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性。加入锌粉的目的是_______ 。
(2)向(1)锥形瓶中先加入足量稀硫酸,后用0.010mol·L-1KMnO4溶液滴定上一步骤所得溶液至终点,消耗KMnO4溶液20.02mL,滴定中 被还原成Mn2+。写出发生反应的离子方程式:
被还原成Mn2+。写出发生反应的离子方程式:_______ 。
(3)上述实验滴定时,指示剂应该_______ (填“加”或“不加”),判断滴定终点的现象是_______ 。
(4)再重复(1)、(2)步骤操作两次,滴定消耗0.010mol·L-1KMnO4溶液平均每次为19.98mL。计算确定该晶体中铁的质量分数(写出计算过程)___________ 。
(1)已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。现称量5.000g三草酸合铁酸钾晶体,配制成250mL溶液。取所配溶液25.00mL于锥形瓶中加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部被氧化成二氧化碳。向反应后的溶液中加入足量锌粉,加热至溶液完全由黄色变为浅绿色时,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性。加入锌粉的目的是
(2)向(1)锥形瓶中先加入足量稀硫酸,后用0.010mol·L-1KMnO4溶液滴定上一步骤所得溶液至终点,消耗KMnO4溶液20.02mL,滴定中
 被还原成Mn2+。写出发生反应的离子方程式:
被还原成Mn2+。写出发生反应的离子方程式:(3)上述实验滴定时,指示剂应该
(4)再重复(1)、(2)步骤操作两次,滴定消耗0.010mol·L-1KMnO4溶液平均每次为19.98mL。计算确定该晶体中铁的质量分数(写出计算过程)
您最近一年使用:0次
名校
解题方法
4 . 硫的化合物在生产生活中有广泛应用。
(1)硫化钠主要用于皮革、毛纺、高档纸张、染料等行业。生产硫化钠大多采用无水芒硝(Na2SO4)-炭粉还原法,其流程示意图如下:
① 上述流程中采用稀碱液比用热水更好,理由是__________________ 。
② 取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌。若反应后测得溶液的pH=4,则此时溶液中c( S2-)=______ mol·L-1。(已知:常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20)
(2)工业上常利用废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2制备无水Na2SO3。KIO3滴定法可测定成品中Na2SO3的含量:室温下将0.1260g 成品溶于水并加入淀粉做指示剂,再用0.01000 mol·L−1 KIO3酸性标准溶液滴定至终点,消耗KIO3溶液31.25mL。
① 滴定终点观察到的现象为:_____________________ 。
② 成品中Na2SO3的质量分数是_________ (请写出计算过程)。
(1)硫化钠主要用于皮革、毛纺、高档纸张、染料等行业。生产硫化钠大多采用无水芒硝(Na2SO4)-炭粉还原法,其流程示意图如下:
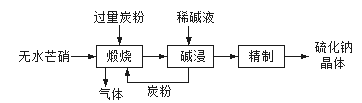
① 上述流程中采用稀碱液比用热水更好,理由是
② 取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌。若反应后测得溶液的pH=4,则此时溶液中c( S2-)=
(2)工业上常利用废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2制备无水Na2SO3。KIO3滴定法可测定成品中Na2SO3的含量:室温下将0.1260g 成品溶于水并加入淀粉做指示剂,再用0.01000 mol·L−1 KIO3酸性标准溶液滴定至终点,消耗KIO3溶液31.25mL。
① 滴定终点观察到的现象为:
② 成品中Na2SO3的质量分数是
您最近一年使用:0次
5 . 某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。请填写下列空白:
Ⅰ.测定过氧化氢的含量
(1)移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250 mL_______ (填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00 mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式为________ 。
(3)判断滴定到达终点的现象是_________________________ 。
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为____________ 。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________ (填“偏高”或“偏低”或“不变”)。
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)
请将他们的实验方法和实验现象填入下表:
Ⅰ.测定过氧化氢的含量
(1)移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250 mL
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式为
(3)判断滴定到达终点的现象是
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)
请将他们的实验方法和实验现象填入下表:
| 实验内容 | 实验方法 | 实验现象 |
| 验证氧化性 | ||
| 验证不稳定性 |
您最近一年使用:0次
2016-12-09更新
|
571次组卷
|
4卷引用:2015届江苏省扬州中学高三质量检测化学试卷
2015届江苏省扬州中学高三质量检测化学试卷福建省2020届高三化学总复习专题训练——过氧化氢氧化性、还原性的探究三轮冲刺2020届高三化学考题必刷——“拓展综合型”实验探究题(已下线)微专题24 H2O2性质“四重性”探究及应用-备战2022年高考化学考点微专题
名校
6 . 滴定实验是化学学科中重要的定量实验。请回答下列问题:
(1)某学生用 的标准
的标准 溶液滴定未知浓度的盐酸,用酚䣭为指示剂。
溶液滴定未知浓度的盐酸,用酚䣭为指示剂。
①排出碱式滴定管中气泡的方法应采用操作_____ ,(填序号)然后轻轻挤压玻璃球使尖嘴部分充满碱液。

②判断滴定终点的现象是:_____ 。
③下列操作会造成测定结果(待测 溶液浓度值)偏低的有
溶液浓度值)偏低的有_____ 。
A.配制标准溶液定容时,加水超过刻度 B.锥形瓶蒸馏水洗后直接装待测液
C.酸式滴定管水洗后未用待测稀盐酸溶液润洗 D.滴定到达终点时,俯视读出滴定管读数
E.碱式滴定管尖嘴部分有气泡,滴定后消失 F.摇动锥形瓶时有少量液体溅出瓶外
(2)常温下,用 溶液滴定
溶液滴定 溶液,滴定曲线如下图所示。下列说法
溶液,滴定曲线如下图所示。下列说法不正确 的是___________。

(3)样品中亚硝基硫酸质量分数的测定
称取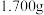 产品放入
产品放入 的锥形瓶中,加入
的锥形瓶中,加入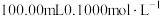 的
的 溶液和少量稀
溶液和少量稀 ,发生反应:
,发生反应: ,产品中其他杂质不与
,产品中其他杂质不与 反应。反应完全后,用
反应。反应完全后,用 的
的 标准溶液滴定过量的
标准溶液滴定过量的 ,发生反应:
,发生反应: ,消耗
,消耗 标准溶液
标准溶液 。
。
请确定样品中亚硝基硫酸(相对分子质量为127)的质量分数__________ ,并写出计算过程。
(1)某学生用
 的标准
的标准 溶液滴定未知浓度的盐酸,用酚䣭为指示剂。
溶液滴定未知浓度的盐酸,用酚䣭为指示剂。①排出碱式滴定管中气泡的方法应采用操作

②判断滴定终点的现象是:
③下列操作会造成测定结果(待测
 溶液浓度值)偏低的有
溶液浓度值)偏低的有A.配制标准溶液定容时,加水超过刻度 B.锥形瓶蒸馏水洗后直接装待测液
C.酸式滴定管水洗后未用待测稀盐酸溶液润洗 D.滴定到达终点时,俯视读出滴定管读数
E.碱式滴定管尖嘴部分有气泡,滴定后消失 F.摇动锥形瓶时有少量液体溅出瓶外
(2)常温下,用
 溶液滴定
溶液滴定 溶液,滴定曲线如下图所示。下列说法
溶液,滴定曲线如下图所示。下列说法
A. |
B.滴定过程中,可能存在: |
| C.若用甲基橙作指示剂,滴定终点的颜色变化为红色变为橙色 |
D.若将盐酸换成相同浓度 醋酸,则滴定到 醋酸,则滴定到 时, 时, |
(3)样品中亚硝基硫酸质量分数的测定
称取
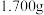 产品放入
产品放入 的锥形瓶中,加入
的锥形瓶中,加入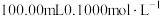 的
的 溶液和少量稀
溶液和少量稀 ,发生反应:
,发生反应: ,产品中其他杂质不与
,产品中其他杂质不与 反应。反应完全后,用
反应。反应完全后,用 的
的 标准溶液滴定过量的
标准溶液滴定过量的 ,发生反应:
,发生反应: ,消耗
,消耗 标准溶液
标准溶液 。
。请确定样品中亚硝基硫酸(相对分子质量为127)的质量分数
您最近一年使用:0次
7 . MnCO3常用于医药、电焊条辅料等,以软锰矿浆(主要成分为MnO2,杂质为Fe2O3、Al2O3、SiO2等)和烟气(含有SO2、O2)为原料制备MnCO3的流程如图:

(1)“浸取”时采取向一定量软锰矿浆液中匀速通入烟气。
①软锰矿浆液吸收烟气中SO2生成MnSO4,该反应化学方程式为_______ 。
②随着吸收时间增加,溶液中c(H2SO4)、c(MnSO4)随吸收时间的变化如图1所示,溶液中c(H2SO4)的增加呈现由慢到快的趋势,其主要原因是_______ 。

(2)“除杂”时,若溶液中c(Mn2+)=0.2mol•L-1,欲使溶液中Fe3+、Al3+均转化为沉淀,同时浓度均小于1×10-6mol•L-1,需控制的pH范围为_________ 。(已知:室温下Ksp[Al(OH)3]=1×10-33,Ksp[Fe(OH)3]=3×10-39,Ksp[Mn(OH)2]=2×10-13。)
(3)“沉锰”时发生反应的离子方程式为:________ ,将“沉锰”时所得滤液蒸发浓缩、冷却结晶,可得到的晶体化学式为________ 。
(4)已知MnO2一种晶型的晶胞结构如图2所示,已知该晶胞的体积为Vnm3,则该晶胞中锰离子的配位数为_______ ,MnO2晶体的密度为_______ g•cm-3。(阿伏加德罗常数的值用NA表示)

(5)测定软锰矿中MnO2含量的方法如下:
步骤一:称取0.1500g软锰矿样品于碘量瓶中,加适量硫酸及足量碘化钾溶液充分反应。
步骤二:待反应完全后加入少量淀粉溶液,用0.1000mol•L-1 Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液22.00mL,计算软锰矿中MnO2的质量分数,写出计算过程________ 。已知:I2+S2O →I-+S4O
→I-+S4O (未配平)
(未配平)

(1)“浸取”时采取向一定量软锰矿浆液中匀速通入烟气。
①软锰矿浆液吸收烟气中SO2生成MnSO4,该反应化学方程式为
②随着吸收时间增加,溶液中c(H2SO4)、c(MnSO4)随吸收时间的变化如图1所示,溶液中c(H2SO4)的增加呈现由慢到快的趋势,其主要原因是

(2)“除杂”时,若溶液中c(Mn2+)=0.2mol•L-1,欲使溶液中Fe3+、Al3+均转化为沉淀,同时浓度均小于1×10-6mol•L-1,需控制的pH范围为
(3)“沉锰”时发生反应的离子方程式为:
(4)已知MnO2一种晶型的晶胞结构如图2所示,已知该晶胞的体积为Vnm3,则该晶胞中锰离子的配位数为

(5)测定软锰矿中MnO2含量的方法如下:
步骤一:称取0.1500g软锰矿样品于碘量瓶中,加适量硫酸及足量碘化钾溶液充分反应。
步骤二:待反应完全后加入少量淀粉溶液,用0.1000mol•L-1 Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液22.00mL,计算软锰矿中MnO2的质量分数,写出计算过程
 →I-+S4O
→I-+S4O (未配平)
(未配平)
您最近一年使用:0次
名校
8 . 实验室以二氧化铈( )废渣为原料制备
)废渣为原料制备 含量少的
含量少的 ,其部分实验过程如下:
,其部分实验过程如下:
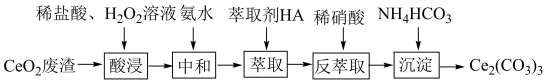
(1)“酸浸”时 与
与 反应生成
反应生成 并放出
并放出 ,该反应的离子方程式为
,该反应的离子方程式为___________
(2)pH约为7的 溶液与
溶液与 溶液反应可生成
溶液反应可生成 沉淀,同时放出
沉淀,同时放出 ,该沉淀中
,该沉淀中 含量与加料方式有关。
含量与加料方式有关。
①得到含 量较少的
量较少的 的加料方式为
的加料方式为___________ (填序号)。
A.将 溶液滴加到
溶液滴加到 溶液中 B.将
溶液中 B.将 溶液滴加到
溶液滴加到 溶液中
溶液中
② 溶液与
溶液与 溶液反应的离子方程式:
溶液反应的离子方程式:___________
(3)通过中和、萃取、反萃取、沉淀等过程,可制备 含量少的
含量少的 。已知
。已知 能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
①加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是___________ 。
②反萃取的目的是将有机层 转移到水层。使
转移到水层。使 尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有
尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有___________ 。
(4)实验中需要测定溶液中 的含量。已知水溶液中
的含量。已知水溶液中 可用准确浓度的
可用准确浓度的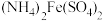 溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为
溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为 。请补充完整实验方案:①准确量取25.00 mL
。请补充完整实验方案:①准确量取25.00 mL  溶液[
溶液[ 约为
约为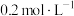 ],加氧化剂将
],加氧化剂将 完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到250 mL容量瓶中后定容;②按规定操作分别将
完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到250 mL容量瓶中后定容;②按规定操作分别将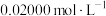
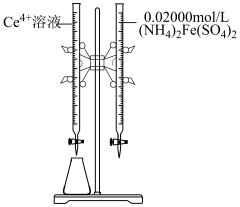
 和待测
和待测 溶液装入如图所示的滴定管中:③
溶液装入如图所示的滴定管中:③___________
 )废渣为原料制备
)废渣为原料制备 含量少的
含量少的 ,其部分实验过程如下:
,其部分实验过程如下:
(1)“酸浸”时
 与
与 反应生成
反应生成 并放出
并放出 ,该反应的离子方程式为
,该反应的离子方程式为(2)pH约为7的
 溶液与
溶液与 溶液反应可生成
溶液反应可生成 沉淀,同时放出
沉淀,同时放出 ,该沉淀中
,该沉淀中 含量与加料方式有关。
含量与加料方式有关。①得到含
 量较少的
量较少的 的加料方式为
的加料方式为A.将
 溶液滴加到
溶液滴加到 溶液中 B.将
溶液中 B.将 溶液滴加到
溶液滴加到 溶液中
溶液中②
 溶液与
溶液与 溶液反应的离子方程式:
溶液反应的离子方程式:(3)通过中和、萃取、反萃取、沉淀等过程,可制备
 含量少的
含量少的 。已知
。已知 能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
①加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是
②反萃取的目的是将有机层
 转移到水层。使
转移到水层。使 尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有
尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有(4)实验中需要测定溶液中
 的含量。已知水溶液中
的含量。已知水溶液中 可用准确浓度的
可用准确浓度的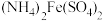 溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为
溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为 。请补充完整实验方案:①准确量取25.00 mL
。请补充完整实验方案:①准确量取25.00 mL  溶液[
溶液[ 约为
约为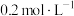 ],加氧化剂将
],加氧化剂将 完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到250 mL容量瓶中后定容;②按规定操作分别将
完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到250 mL容量瓶中后定容;②按规定操作分别将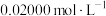
 和待测
和待测 溶液装入如图所示的滴定管中:③
溶液装入如图所示的滴定管中:③
您最近一年使用:0次
9 . I.分析某一种不纯的Na2S,已知其中除含有Na2S·9H2O外,还含有Na2S2O3·5H2O,取此试样10.00g配制成500.0mL溶液。
(1)取试样溶液25.00mL于碘量瓶中,加入50.00mL0.05250mol·L-1的I2,用0.1010mol·L-1Na2S2O3溶液滴定多余的I2,用去16.91mL。
(2)取50.00mL试样溶液,用ZnCO3悬浮液沉淀除去其中的Na2S后(忽略体积影响),取滤液的一半,用0.05000mol·L-1I2溶液滴定其中的Na2S2O3,用去5.65mL。
①请写出上述实验涉及的化学方程式_______
②根据以上实验结果,可算出该不纯的硫化钠样品中:Na2S·9H2O的质量分数为_______ ,Na2S2O3·5H2O的质量分数为_______ 。
II.人体正常血液的pH值维持在7.35-7.45间,且数值不会因为少量酸碱性的物质进入血液而发生明显变化,原因是血液中含有缓冲物质,主要由H2CO3/NaHCO3予以调节。人体运动时肌肉收缩产生的乳酸如果过多的进入血液,导致pH<7.3则会造成酸中毒(Acidosis)。计算血液pH与c(H2CO3)/c( )的关系式为:
)的关系式为:_______ ;当血液pH为7.35时,其中的c(H2CO3)/c( )比值为
)比值为_______ 。(已知H2CO3的电离常数pKa1=6.35,pKa2=10.33)
(1)取试样溶液25.00mL于碘量瓶中,加入50.00mL0.05250mol·L-1的I2,用0.1010mol·L-1Na2S2O3溶液滴定多余的I2,用去16.91mL。
(2)取50.00mL试样溶液,用ZnCO3悬浮液沉淀除去其中的Na2S后(忽略体积影响),取滤液的一半,用0.05000mol·L-1I2溶液滴定其中的Na2S2O3,用去5.65mL。
①请写出上述实验涉及的化学方程式
②根据以上实验结果,可算出该不纯的硫化钠样品中:Na2S·9H2O的质量分数为
II.人体正常血液的pH值维持在7.35-7.45间,且数值不会因为少量酸碱性的物质进入血液而发生明显变化,原因是血液中含有缓冲物质,主要由H2CO3/NaHCO3予以调节。人体运动时肌肉收缩产生的乳酸如果过多的进入血液,导致pH<7.3则会造成酸中毒(Acidosis)。计算血液pH与c(H2CO3)/c(
 )的关系式为:
)的关系式为: )比值为
)比值为
您最近一年使用:0次
名校
解题方法
10 . 食醋是日常饮食中的一种调味剂,国家标准规定酿造食醋中醋酸含量不得低于0.035g/mL,实验室用标准NaOH溶液测定食醋中醋酸的浓度,以检测食醋是否符合国家标准,某品牌白醋的醋酸浓度测定过程如图所示,请回答:
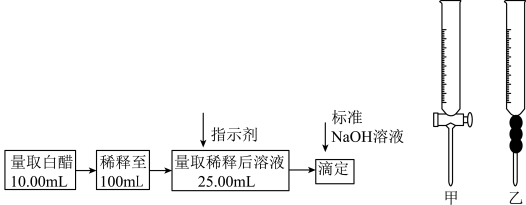
(1)选用上述___________ (填“甲”或“乙”)滴定管量取10.00mL白醋后,将白醋稀释至100mL时,需要使用的玻璃仪器有烧杯、玻璃棒和___________ 。
(2)某同学用酸碱中和滴定法测定该品牌白醋的醋酸浓度,当醋酸与氢氧化钠恰好完全反应时,测得溶液中 ,则此时溶液中的pH=
,则此时溶液中的pH=___________ 。(已知:室温下醋酸的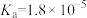 )
)
(3)根据该同学的计算结果,应该选___________ 作指示剂。(填“酚酞”、“甲基橙”或“石蕊”)
(4)该滴定达到终点时的现象是___________ 。
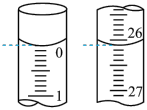
(5)某次实验滴定开始和结束时,碱式滴定管中的液面如下图所示,则所用NaOH溶液的体积为___________ mL。
(6)用标准的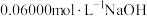 溶液滴定上述稀释后的醋酸溶液,滴定结果如下表所示:
溶液滴定上述稀释后的醋酸溶液,滴定结果如下表所示:
则该品牌白醋中醋酸含量为___________ mg/mL。
(7)下列操作中,可能使所测白醋中醋酸的浓度数值偏高的是___________。(填编号)。
(8)有一支50mL的酸式滴定管,其中盛有溶液,液面恰好在10.00mL刻度处,现把管内液体全部放出,用量筒接收,得到溶液的体积是___________。

(1)选用上述
(2)某同学用酸碱中和滴定法测定该品牌白醋的醋酸浓度,当醋酸与氢氧化钠恰好完全反应时,测得溶液中
 ,则此时溶液中的pH=
,则此时溶液中的pH=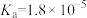 )
)(3)根据该同学的计算结果,应该选
(4)该滴定达到终点时的现象是
(5)某次实验滴定开始和结束时,碱式滴定管中的液面如下图所示,则所用NaOH溶液的体积为

(6)用标准的
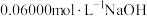 溶液滴定上述稀释后的醋酸溶液,滴定结果如下表所示:
溶液滴定上述稀释后的醋酸溶液,滴定结果如下表所示:| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00mL | 0.02 | 25.01 |
| 2 | 25.00mL | 0.70 | 25.71 |
| 3 | 25.00mL | 0.50 | 24.2 |
(7)下列操作中,可能使所测白醋中醋酸的浓度数值偏高的是___________。(填编号)。
| A.取待测液的滴管,取液前滴定管尖嘴处无气泡,取液后尖嘴处出现气泡 |
| B.滴定前盛放白醋稀溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.碱式滴定管未用标准NaOH溶液润洗就直接注入标准NaOH溶液 |
| D.读取NaOH溶液体积时,开始时俯视读数,滴定结束时仰视读数 |
| A.等于10mL | B.等于40mL | C.大于40mL | D.不能确定 |
您最近一年使用:0次
2023-04-21更新
|
200次组卷
|
2卷引用:江苏省常熟市2022-2023学年高二下学期期中考试化学试题



