1 . 电解质溶液中存在多种平衡,请回答下列问题:
(1)已知25℃时,体积均为10mL,pH均为2的HF溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程中pH的变化如图所示[已知: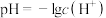 ]。则
]。则

①25℃时,HF的电离常数_______ HX的电离常数(填“>”“<”或“=”)。
②稀释100倍后,HF溶液中由水电离出的
_______ HX溶液中由水电离出的 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(2)实验室有一瓶未知浓度的 溶液,通过下列实验测定其浓度。
溶液,通过下列实验测定其浓度。
第一步:取 溶液于锥形瓶中,滴入指示剂2~3滴。
溶液于锥形瓶中,滴入指示剂2~3滴。
第二步:取一滴定管,依次查漏,洗涤,用 的
的 溶液润洗,然后注入该标准溶液,调整液面,记下读数。
溶液润洗,然后注入该标准溶液,调整液面,记下读数。
第三步:将锥形瓶置于滴定管下进行滴定,发生的反应为:
试回答下列问题:
①滴定过程中加入的指示剂是_______ ;滴定时,眼睛注视_______ 直至滴定终点;达到滴定终点的判断依据是_______ 。
②已知消耗标准液的实验数据如下表。
则该 溶液的物质的量浓度为
溶液的物质的量浓度为_______ 。
③下列操作会导致测定结果偏高的是_______ (填字母)。
A.滴定管在装标准溶液前未用标准溶液润洗
B.滴定过程中,锥形瓶振荡得太剧烈,锥形瓶内有液滴溅出
C.装标准溶液的滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D.达到滴定终点时,仰视读数
(1)已知25℃时,体积均为10mL,pH均为2的HF溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程中pH的变化如图所示[已知:
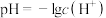 ]。则
]。则
①25℃时,HF的电离常数
②稀释100倍后,HF溶液中由水电离出的

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)实验室有一瓶未知浓度的
 溶液,通过下列实验测定其浓度。
溶液,通过下列实验测定其浓度。第一步:取
 溶液于锥形瓶中,滴入指示剂2~3滴。
溶液于锥形瓶中,滴入指示剂2~3滴。第二步:取一滴定管,依次查漏,洗涤,用
 的
的 溶液润洗,然后注入该标准溶液,调整液面,记下读数。
溶液润洗,然后注入该标准溶液,调整液面,记下读数。第三步:将锥形瓶置于滴定管下进行滴定,发生的反应为:

试回答下列问题:
①滴定过程中加入的指示剂是
②已知消耗标准液的实验数据如下表。
| 实验次数 | 始读数(mL) | 末读数(mL) |
| 1 | 0.10 | 19.20 |
| 2 | 1.85 | 20.75 |
| 3 | 0.00 | 24.06 |
 溶液的物质的量浓度为
溶液的物质的量浓度为③下列操作会导致测定结果偏高的是
A.滴定管在装标准溶液前未用标准溶液润洗
B.滴定过程中,锥形瓶振荡得太剧烈,锥形瓶内有液滴溅出
C.装标准溶液的滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D.达到滴定终点时,仰视读数
您最近一年使用:0次
解题方法
2 . 水的电离过程为H2O OH++OH-。在25℃、35℃时水的离子积常数分别为1.0×10-14、2.1×10-14。下列叙述正确的是
OH++OH-。在25℃、35℃时水的离子积常数分别为1.0×10-14、2.1×10-14。下列叙述正确的是
 OH++OH-。在25℃、35℃时水的离子积常数分别为1.0×10-14、2.1×10-14。下列叙述正确的是
OH++OH-。在25℃、35℃时水的离子积常数分别为1.0×10-14、2.1×10-14。下列叙述正确的是| A.水的电离是放热过程 | B.水的电离度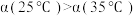 |
C.在35℃时,纯水中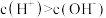 | D.纯水中 随着温度的升高而增大 随着温度的升高而增大 |
您最近一年使用:0次
2024-03-20更新
|
58次组卷
|
4卷引用:河北省石家庄康福外国语学校2023-2024学年高二上学期期中考试化学试题
3 . 在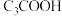 溶液中存在下列电离平衡:
溶液中存在下列电离平衡: 。
。
(1)加入少量的冰醋酸,平衡将_______ ,溶液中 将
将_______  填
填 增大
增大 减小
减小 或
或 不变
不变 。
。
(2)加入一定量蒸馏水,平衡将_______ ,溶液中 将
将_______  填
填 增大
增大 减小
减小 或
或 不变
不变 。
。
(3)加入少量 盐酸,平衡将
盐酸,平衡将_______ ,溶液 将
将_______  填
填 增大
增大 减小
减小 或
或 不变
不变 。
。
(4)加入 溶液,平衡将
溶液,平衡将_______ ,溶液中 将
将_______  填
填 增大
增大 减小
减小 或
或 不变
不变 。
。
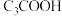 溶液中存在下列电离平衡:
溶液中存在下列电离平衡: 。
。(1)加入少量的冰醋酸,平衡将
 将
将 填
填 增大
增大 减小
减小 或
或 不变
不变 。
。(2)加入一定量蒸馏水,平衡将
 将
将 填
填 增大
增大 减小
减小 或
或 不变
不变 。
。(3)加入少量
 盐酸,平衡将
盐酸,平衡将 将
将 填
填 增大
增大 减小
减小 或
或 不变
不变 。
。(4)加入
 溶液,平衡将
溶液,平衡将 将
将 填
填 增大
增大 减小
减小 或
或 不变
不变 。
。
您最近一年使用:0次
名校
4 . 已知常温下部分弱电解质的电离平衡常数如下表:
(1)常温下,物质的量浓度相同的三种溶液①NaF溶液;②NaClO溶液;③ 溶液,其pH由大到小的顺序是
溶液,其pH由大到小的顺序是___________ (填序号)。
(2)浓度均为0.1 mol/L① ;②
;② ;③
;③ ;④氨水;⑤
;④氨水;⑤ 五种溶液中,
五种溶液中, 由大到小的顺序
由大到小的顺序___________ (填序号)。
(3)25℃时,将a mol/L的氨水与0.01 mol/L的盐酸等体积混合,反应完后溶液中 ,用含a的代数式表示
,用含a的代数式表示 的电离平衡常数
的电离平衡常数
___________ 。
(4)泡沫灭火器中盛有 、
、 两种溶液,当它们混合时,发生反应的离子方程式为
两种溶液,当它们混合时,发生反应的离子方程式为___________ 。
(5)室温下, 的NaOH溶液和
的NaOH溶液和 的
的 溶液,设由水电离产生的
溶液,设由水电离产生的 的物质的量浓度分别为A和B,则
的物质的量浓度分别为A和B,则 等于
等于___________ 。
(6)亚磷酸溶液中的 H3PO3、H2PO 、HPO
、HPO 的物质的量分数δ(x)随 c(H+)的变化如图所示。
的物质的量分数δ(x)随 c(H+)的变化如图所示。
已知: 。
。

图像中c点c(H3PO3)=c(HPO ),那c点对应的c(H+)=
),那c点对应的c(H+)=___________ mol/L(只列出计算式)。
(7)25℃时,H3PO4的电离常数为Ka1=7.5×10-3,Ka2=6.2×10-8,Ka3=4.4×10-13。足量NaF溶液和H3PO4溶液反应的离子方程式为___________ 。
| 化学式 | HF | HClO |  |  | H3PO3 |
| 电离常数 | 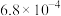 | 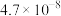 |  ; ; |  | Ka1=5.0×10-2Ka2=2.6×10-7 |
(1)常温下,物质的量浓度相同的三种溶液①NaF溶液;②NaClO溶液;③
 溶液,其pH由大到小的顺序是
溶液,其pH由大到小的顺序是(2)浓度均为0.1 mol/L①
 ;②
;② ;③
;③ ;④氨水;⑤
;④氨水;⑤ 五种溶液中,
五种溶液中, 由大到小的顺序
由大到小的顺序(3)25℃时,将a mol/L的氨水与0.01 mol/L的盐酸等体积混合,反应完后溶液中
 ,用含a的代数式表示
,用含a的代数式表示 的电离平衡常数
的电离平衡常数
(4)泡沫灭火器中盛有
 、
、 两种溶液,当它们混合时,发生反应的离子方程式为
两种溶液,当它们混合时,发生反应的离子方程式为(5)室温下,
 的NaOH溶液和
的NaOH溶液和 的
的 溶液,设由水电离产生的
溶液,设由水电离产生的 的物质的量浓度分别为A和B,则
的物质的量浓度分别为A和B,则 等于
等于(6)亚磷酸溶液中的 H3PO3、H2PO
 、HPO
、HPO 的物质的量分数δ(x)随 c(H+)的变化如图所示。
的物质的量分数δ(x)随 c(H+)的变化如图所示。已知:
 。
。
图像中c点c(H3PO3)=c(HPO
 ),那c点对应的c(H+)=
),那c点对应的c(H+)=(7)25℃时,H3PO4的电离常数为Ka1=7.5×10-3,Ka2=6.2×10-8,Ka3=4.4×10-13。足量NaF溶液和H3PO4溶液反应的离子方程式为
您最近一年使用:0次
名校
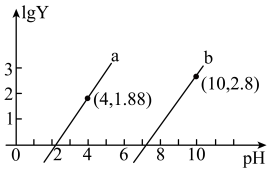
5 . 25℃时,向 的二元酸
的二元酸 溶液中逐滴滴入
溶液中逐滴滴入 溶液,测得溶液的pH与lgY[Y代表
溶液,测得溶液的pH与lgY[Y代表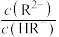 或
或 ]关系如图。下列相关结论错误的是
]关系如图。下列相关结论错误的是
 的二元酸
的二元酸 溶液中逐滴滴入
溶液中逐滴滴入 溶液,测得溶液的pH与lgY[Y代表
溶液,测得溶液的pH与lgY[Y代表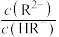 或
或 ]关系如图。下列相关结论错误的是
]关系如图。下列相关结论错误的是
A.曲线b表示pH与 的变化关系 的变化关系 |
B.25℃时, 的 的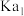 数量级为 数量级为 |
C.溶液的pH=7.2时, |
D.滴入20.00mLNaOH溶液时: |
您最近一年使用:0次
6 . 硼及其化合物在制造、化工等领域都有广泛应用,回答下列问题:
(1)基态硼原子的价电子排布图为__________ ,其占据最高能级电子的电子云轮廓图形状为__________ ,基态硼原子比基态氮原子的第一电离能 小,其原因为
小,其原因为__________ 。
(2) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得:
反应制得:
① 由
由 和
和 构成,
构成, 的空间结构为
的空间结构为__________ 。
② 中B原子的杂化轨道类型为
中B原子的杂化轨道类型为__________ 。
③ 的键角为
的键角为__________ 。
(3)写出B与 溶液反应的离子方程式:
溶液反应的离子方程式:__________ 。
(4) 为一元弱酸[常温下,
为一元弱酸[常温下,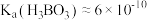 ]:
]:
① 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为__________ 。
②常温下, 的硼酸的pH约为
的硼酸的pH约为__________ (已知: ,
, )。
)。
(1)基态硼原子的价电子排布图为
 小,其原因为
小,其原因为(2)
 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得:
反应制得:①
 由
由 和
和 构成,
构成, 的空间结构为
的空间结构为②
 中B原子的杂化轨道类型为
中B原子的杂化轨道类型为③
 的键角为
的键角为(3)写出B与
 溶液反应的离子方程式:
溶液反应的离子方程式:(4)
 为一元弱酸[常温下,
为一元弱酸[常温下,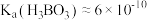 ]:
]:①
 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为②常温下,
 的硼酸的pH约为
的硼酸的pH约为 ,
, )。
)。
您最近一年使用:0次
2024-03-07更新
|
128次组卷
|
2卷引用:河北省邢台市四校联盟2023-2024学年高二上学期11月月考化学试题
名校
解题方法
7 . 氨水在工农业生产中有重要的应用。请回答下列问题:
(1)氨水中的主要溶质为 ,其电离方程式为
,其电离方程式为___________ 。
(2)某温度下,1 氨水中
氨水中 的电离度为
的电离度为 ,则其电离常数
,则其电离常数
___________ (用含 的代数式表示)。取1L上述氨水与1Lx
的代数式表示)。取1L上述氨水与1Lx 盐酸混合,所得溶液中
盐酸混合,所得溶液中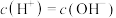 ,则x
,则x___________ 1(填“>”“<”或“=”,下同),
___________  。若氨水与盐酸恰好中和,所得溶液中离子浓度从大到小的顺序为
。若氨水与盐酸恰好中和,所得溶液中离子浓度从大到小的顺序为___________ 。
(3)已知:常温下, ,
, ,则
,则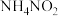 溶液呈
溶液呈___________ (填“酸性”“碱性”或“中性”)。等物质的量浓度的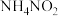 溶液和
溶液和 溶液中,
溶液中, 较大的是
较大的是___________ 。
(1)氨水中的主要溶质为
 ,其电离方程式为
,其电离方程式为(2)某温度下,1
 氨水中
氨水中 的电离度为
的电离度为 ,则其电离常数
,则其电离常数
 的代数式表示)。取1L上述氨水与1Lx
的代数式表示)。取1L上述氨水与1Lx 盐酸混合,所得溶液中
盐酸混合,所得溶液中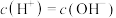 ,则x
,则x
 。若氨水与盐酸恰好中和,所得溶液中离子浓度从大到小的顺序为
。若氨水与盐酸恰好中和,所得溶液中离子浓度从大到小的顺序为(3)已知:常温下,
 ,
, ,则
,则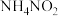 溶液呈
溶液呈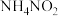 溶液和
溶液和 溶液中,
溶液中, 较大的是
较大的是
您最近一年使用:0次
名校
8 . 下列说法正确且一定能证明 是弱电解质的是
是弱电解质的是
 是弱电解质的是
是弱电解质的是A.25℃时,用 试纸测0.01 试纸测0.01  溶液的 溶液的 为4 为4 |
B. 水溶液中含有 水溶液中含有 分子和 分子和 、 、 |
C.10 0.01 0.01  溶液恰好与10 溶液恰好与10 0.01 0.01  溶液完全反应 溶液完全反应 |
D.用 溶液做导电性实验,灯泡很暗 溶液做导电性实验,灯泡很暗 |
您最近一年使用:0次
名校
9 . 常温下,向20.00mL 溶液中滴加
溶液中滴加 溶液,溶液中
溶液,溶液中 随pH的变化关系如图所示。下列说法正确的是
随pH的变化关系如图所示。下列说法正确的是

 溶液中滴加
溶液中滴加 溶液,溶液中
溶液,溶液中 随pH的变化关系如图所示。下列说法正确的是
随pH的变化关系如图所示。下列说法正确的是
| A.y=3.87 |
B.a点对应的溶液中: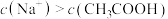 |
C.消耗NaOH溶液小于10.00mL时,溶液中 |
D.滴定过程中溶液的pH每增大1个单位, 增大量小于1个单位 增大量小于1个单位 |
您最近一年使用:0次
名校
解题方法
10 . 物质结构决定性质。下列叙述1和叙述2都正确且二者有相关性的是
| 叙述1 | 叙述2 | |
| A | NF3分子中N原子价层有4个电子对 | NF3分子是非极性分子 |
| B |
| 邻羟基苯甲酸的Ka2大于苯酚 |
| C | 酸性:HCOOH>CH3COOH | O-H的极性:HCOOH强于CH3COOH |
| D | O2与O3分子极性相同 | 都是由非极性键构成的非极性分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-05更新
|
213次组卷
|
2卷引用:河北省石家庄市第二中学2023-2024学年高三上学期期末考试化学试题

 分子内氢键较稳定
分子内氢键较稳定

