1 . I.酸碱中和滴定是一种重要的实验方法,用 标准溶液溶液滴定未知浓度的醋酸
标准溶液溶液滴定未知浓度的醋酸
(1) 标准溶液盛放在
标准溶液盛放在_______ (填“酸或碱”)式滴定管中。
(2)该实验中选择的指示剂是_______ 。
(3)根据下列数据,请计算待测醋酸的浓度:_______  。
。
(4)量取标准液的碱式滴定管未润洗,会造成测定结果_______ (填“偏高或偏低或不变”) 。
Ⅱ.按要求填空
(5)FeCl3溶液蒸发灼烧最终得到的物质_______ (写化学式 )。
(6)泡沫灭火器原理_______ (写离子反应方程式)。
 标准溶液溶液滴定未知浓度的醋酸
标准溶液溶液滴定未知浓度的醋酸(1)
 标准溶液盛放在
标准溶液盛放在(2)该实验中选择的指示剂是
(3)根据下列数据,请计算待测醋酸的浓度:
 。
。| 滴定次数 | 待测液体积(mL) | 标准液体积(mL | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.60 | 20.60 |
| 第二次 | 20.00 | 2.00 | 24.10 |
| 第三次 | 20.00 | 4.00 | 24.00 |
(4)量取标准液的碱式滴定管未润洗,会造成测定结果
Ⅱ.按要求填空
(5)FeCl3溶液蒸发灼烧最终得到的物质
(6)泡沫灭火器原理
您最近一年使用:0次
2 . 按要求回答下列问题。
(1)铁盐可用作净水剂,用离子方程式表示其原理:___________ 。配制 溶液时,需将
溶液时,需将 晶体溶解到较浓的
晶体溶解到较浓的___________ 中,然后再加水稀释到所需的浓度。将 溶液蒸干并灼烧,得到的产物是
溶液蒸干并灼烧,得到的产物是___________ (填化学式)。
(2)某 溶液中含有
溶液中含有 杂质,可向溶液中加入足量的
杂质,可向溶液中加入足量的___________ ,充分反应后过滤,即可除去 。
。
(3)在 的
的 溶液中,含有杂质
溶液中,含有杂质 。若通过直接调节
。若通过直接调节 的方法使
的方法使 沉淀完全,是否同时会有
沉淀完全,是否同时会有 沉淀生成?
沉淀生成?___________ (填“是”或“否”)。向溶液中加入 将
将 氧化为
氧化为 ,调节
,调节 使
使 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 ),此时溶液的
),此时溶液的 约为
约为___________ 。(已知 时
时 、
、 、
、 的
的 分别为
分别为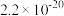 、
、 、
、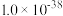 )
)
(1)铁盐可用作净水剂,用离子方程式表示其原理:
 溶液时,需将
溶液时,需将 晶体溶解到较浓的
晶体溶解到较浓的 溶液蒸干并灼烧,得到的产物是
溶液蒸干并灼烧,得到的产物是(2)某
 溶液中含有
溶液中含有 杂质,可向溶液中加入足量的
杂质,可向溶液中加入足量的 。
。(3)在
 的
的 溶液中,含有杂质
溶液中,含有杂质 。若通过直接调节
。若通过直接调节 的方法使
的方法使 沉淀完全,是否同时会有
沉淀完全,是否同时会有 沉淀生成?
沉淀生成? 将
将 氧化为
氧化为 ,调节
,调节 使
使 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 ),此时溶液的
),此时溶液的 约为
约为 时
时 、
、 、
、 的
的 分别为
分别为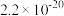 、
、 、
、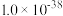 )
)
您最近一年使用:0次
解题方法
3 . 离子方程式书写:
(1)明矾可以净水:______ 。
(2)热的纯碱液可用于去油污:______ 。
(3)硫酸铝溶液和碳酸氢钠溶液可用于制泡沫灭火器:______ 。
(1)明矾可以净水:
(2)热的纯碱液可用于去油污:
(3)硫酸铝溶液和碳酸氢钠溶液可用于制泡沫灭火器:
您最近一年使用:0次
解题方法
4 . “弱”,释义为力气小,势力小,效果(由某种动因或原因所产生的结果;后果(效果)程度越浅)与“强”相对。弱电解质、盐类的水解都与“弱”相关。根据你所学过的知识,回答下列问题:
(1)在常温下, 一元酸
一元酸 溶液的
溶液的 ,回答下列问题:
,回答下列问题:
① 在水溶液中的电离平衡常数
在水溶液中的电离平衡常数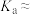
___________ 。
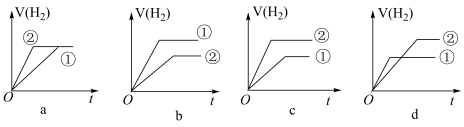
②常温下,有 相同、体积相同的盐酸和上述酸HB两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
相同、体积相同的盐酸和上述酸HB两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是___________ (填字母)。(①表示盐酸,②表示HB)。
(2) 时,向氨水中加入少量硫酸铵固体,则溶液中
时,向氨水中加入少量硫酸铵固体,则溶液中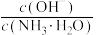 将
将___________ (填“增大”“减小”或“不变”);向氨水中加入稀硫酸至溶液的 ,此时溶液中
,此时溶液中 ,则
,则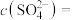
___________
(3) 可用作白色颜料和阻燃剂等。在实验室中可利用
可用作白色颜料和阻燃剂等。在实验室中可利用 的水解反应制取
的水解反应制取 。(
。( 的水解分三步进行,中间产物有
的水解分三步进行,中间产物有 等)。
等)。
①为配制 溶液,取
溶液,取 固体少许溶于
固体少许溶于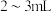 水中,有白色沉淀产生,此溶液的
水中,有白色沉淀产生,此溶液的
___________ 7(填“小于”“大于”或“等于”),配制 溶液的正确方法是
溶液的正确方法是_____
②为了得到较多的 ,操作时要将
,操作时要将 缓慢加入大量水中,反应后期还要加入少量氨水。试利用平衡移动原理说明这两项操作的作用:
缓慢加入大量水中,反应后期还要加入少量氨水。试利用平衡移动原理说明这两项操作的作用:___________ 。
(1)在常温下,
 一元酸
一元酸 溶液的
溶液的 ,回答下列问题:
,回答下列问题:①
 在水溶液中的电离平衡常数
在水溶液中的电离平衡常数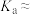
②常温下,有
 相同、体积相同的盐酸和上述酸HB两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
相同、体积相同的盐酸和上述酸HB两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
(2)
 时,向氨水中加入少量硫酸铵固体,则溶液中
时,向氨水中加入少量硫酸铵固体,则溶液中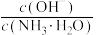 将
将 ,此时溶液中
,此时溶液中 ,则
,则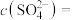
(3)
 可用作白色颜料和阻燃剂等。在实验室中可利用
可用作白色颜料和阻燃剂等。在实验室中可利用 的水解反应制取
的水解反应制取 。(
。( 的水解分三步进行,中间产物有
的水解分三步进行,中间产物有 等)。
等)。①为配制
 溶液,取
溶液,取 固体少许溶于
固体少许溶于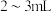 水中,有白色沉淀产生,此溶液的
水中,有白色沉淀产生,此溶液的
 溶液的正确方法是
溶液的正确方法是②为了得到较多的
 ,操作时要将
,操作时要将 缓慢加入大量水中,反应后期还要加入少量氨水。试利用平衡移动原理说明这两项操作的作用:
缓慢加入大量水中,反应后期还要加入少量氨水。试利用平衡移动原理说明这两项操作的作用:
您最近一年使用:0次
5 . 按要求填空:
(1)某元素的最外层电子排布式是4s24p5,则其元素符号为___________ 。
(2)写出以惰性电极为材料电解饱和MgCl2溶液的离子方程式___________ 。
(3)H3BO3具有一元弱酸的性质,在水中可产生正四面体结构的离子,写出H3BO3在水中的电离方程式:___________ 。
(4)50mL0.50mol/LHCl溶液与50mL0.55mol/LNaOH溶液充分反应,测得此过程放出akJ的热量,写出该过程表示中和热(数值要求化简)的热化学方程式:___________ 。
(5)将AlCl3溶液蒸干并灼烧得不到无水AlCl3,但将SOCl2(亚硫酰氯)与AlCl3·6H2O混合并加热,可获得无水AlCl3,试写出此混合加热过程的化学方程式___________ 。
(1)某元素的最外层电子排布式是4s24p5,则其元素符号为
(2)写出以惰性电极为材料电解饱和MgCl2溶液的离子方程式
(3)H3BO3具有一元弱酸的性质,在水中可产生正四面体结构的离子,写出H3BO3在水中的电离方程式:
(4)50mL0.50mol/LHCl溶液与50mL0.55mol/LNaOH溶液充分反应,测得此过程放出akJ的热量,写出该过程表示中和热(数值要求化简)的热化学方程式:
(5)将AlCl3溶液蒸干并灼烧得不到无水AlCl3,但将SOCl2(亚硫酰氯)与AlCl3·6H2O混合并加热,可获得无水AlCl3,试写出此混合加热过程的化学方程式
您最近一年使用:0次
6 . 按要求完成下题。
(1)写出H2S的电离方程式:______ 。
(2)0.1mol/LNa2CO3溶液中各离子浓度大小顺序为______ 。
(3)pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,所得溶液显______ 性。
(4)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是______ 。
(5)常温下,NaCN溶液的pH>7,原因是______ (离子反应方程式)。
(6)常温下,pH=10的CH3COONa溶液中,由水电离出的c(OH-)=______ mol/L。
(7)常温下,0.05mol/LH2SO4溶液的pH=______ 。
(1)写出H2S的电离方程式:
(2)0.1mol/LNa2CO3溶液中各离子浓度大小顺序为
(3)pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,所得溶液显
(4)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是
(5)常温下,NaCN溶液的pH>7,原因是
(6)常温下,pH=10的CH3COONa溶液中,由水电离出的c(OH-)=
(7)常温下,0.05mol/LH2SO4溶液的pH=
您最近一年使用:0次
解题方法
7 . 完成下列问题
(1)在25℃时,有pH为x(x≤6)的盐酸和pH为y(y≥8)的NaOH溶液,取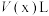 该盐酸同该NaOH溶液中和,需
该盐酸同该NaOH溶液中和,需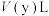 NaOH溶液。回答下列问题:
NaOH溶液。回答下列问题:
①若x+y=14,则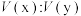
___________ 。
②若x+y=13,则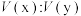
___________ 。
③若x+y>14,则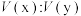
___________ (填表达式)并且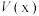
___________ 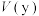 (>、=或<)
(>、=或<)
(2)把 溶液蒸干后再灼烧,最后得到的主要固体产物是
溶液蒸干后再灼烧,最后得到的主要固体产物是___________ ,其理由是(用水解方程式表示)___________ 。
(3)在一定温度下,将0.2mol的碘化氢充入1L的密闭容器中,充分反应,达到平衡后,测得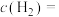
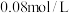 。该反应的平衡常数
。该反应的平衡常数___________ 。
(1)在25℃时,有pH为x(x≤6)的盐酸和pH为y(y≥8)的NaOH溶液,取
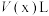 该盐酸同该NaOH溶液中和,需
该盐酸同该NaOH溶液中和,需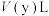 NaOH溶液。回答下列问题:
NaOH溶液。回答下列问题:①若x+y=14,则
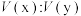
②若x+y=13,则
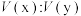
③若x+y>14,则
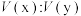
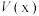
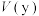 (>、=或<)
(>、=或<)(2)把
 溶液蒸干后再灼烧,最后得到的主要固体产物是
溶液蒸干后再灼烧,最后得到的主要固体产物是(3)在一定温度下,将0.2mol的碘化氢充入1L的密闭容器中,充分反应,达到平衡后,测得
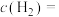
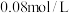 。该反应的平衡常数
。该反应的平衡常数
您最近一年使用:0次
8 . 完成下列问题。
(1)连二亚硫酸钠 ,俗称保险粉,易溶于水,常用于印染、纸张漂白等。回答下列问题:
,俗称保险粉,易溶于水,常用于印染、纸张漂白等。回答下列问题:
① 中S的化合价为
中S的化合价为_______ 。
②向锌粉的悬浮液中通入 ,制备
,制备 ,生成
,生成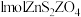 ,反应中转移的电子为
,反应中转移的电子为_______ mol。
(2)高铁酸盐具有极强的氧化性,可作水处理剂。其制备方法为低温下,在 溶液中加入
溶液中加入 浓溶液可析出
浓溶液可析出 。完成下列填空:
。完成下列填空:
①写出上述得到 的化学方程式
的化学方程式_______ 。
②实验室配制 溶液时,需加入少量稀硫酸,用离子方程式解释其原因
溶液时,需加入少量稀硫酸,用离子方程式解释其原因_______ 。
(1)连二亚硫酸钠
 ,俗称保险粉,易溶于水,常用于印染、纸张漂白等。回答下列问题:
,俗称保险粉,易溶于水,常用于印染、纸张漂白等。回答下列问题:①
 中S的化合价为
中S的化合价为②向锌粉的悬浮液中通入
 ,制备
,制备 ,生成
,生成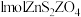 ,反应中转移的电子为
,反应中转移的电子为(2)高铁酸盐具有极强的氧化性,可作水处理剂。其制备方法为低温下,在
 溶液中加入
溶液中加入 浓溶液可析出
浓溶液可析出 。完成下列填空:
。完成下列填空:①写出上述得到
 的化学方程式
的化学方程式②实验室配制
 溶液时,需加入少量稀硫酸,用离子方程式解释其原因
溶液时,需加入少量稀硫酸,用离子方程式解释其原因
您最近一年使用:0次
9 . 写出下列所对应的离子或化学方程式
(1)写出用氯化铁溶液蚀刻印刷电路板发生反应的离子方程式:___________ 。
(2)向FeSO4溶液中滴加少量酸性KMnO4溶液,若溶液紫红色褪去,证明Fe2+具有还原性。反应原理用离子方程式表示为___________ 。
(3)写出泡沫灭火器的工作原理(AlCl3与NaHCO3反应):___________ 。
(4)写出Na2O2与CO2的反应,并标出双线桥___________ 。
(1)写出用氯化铁溶液蚀刻印刷电路板发生反应的离子方程式:
(2)向FeSO4溶液中滴加少量酸性KMnO4溶液,若溶液紫红色褪去,证明Fe2+具有还原性。反应原理用离子方程式表示为
(3)写出泡沫灭火器的工作原理(AlCl3与NaHCO3反应):
(4)写出Na2O2与CO2的反应,并标出双线桥
您最近一年使用:0次
10 . 泡沫灭火器灭火原理(离子方程式)___________ 。
您最近一年使用:0次



