名校
1 . 下列事实不能用勒夏特列原理解释的是
| A.实验室中常用排饱和食盐水的方式收集氯气 |
B.红棕色的 气体,加压后颜色先变深后变浅 气体,加压后颜色先变深后变浅 |
| C.合成氨工业中使用铁触媒作催化剂 |
| D.对熟石灰的悬浊液加热,悬浊液中固体质量增加 |
您最近一年使用:0次
2021-10-23更新
|
665次组卷
|
4卷引用:湖北省襄阳市南漳县第二中学2021-2022学年高二上学期10月考化学试题
名校
2 . 不能用平衡移动原理解释的事实是
| A.向饱和的胆矾溶液中加入表面不规则的硫酸铜晶体,一段时间后溶液质量不变,但晶体逐渐变得规则 |
| B.硫酸钡可作钡餐,而碳酸钡不可以 |
| C.合成氨时选择加压作为反应条件 |
| D.对氯化铝溶液进行蒸干并灼烧后得到氧化铝固体 |
您最近一年使用:0次
2021高三·全国·专题练习
3 . 常温下,向10mL0.1mol·L-1CuCl2溶液中滴入0.1mol·L-1的Na2S溶液,滴加过程中溶液中-lgc(Cu2+)随滴入的Na2S溶液体积的变化如图所示。下列叙述正确的是
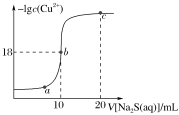

| A.Na2S溶液中:c(S2-)+c(HS-)+c(H2S)=2c(Na+) |
| B.Ksp(CuS)的数量级为10-36 |
| C.a、b、c三点溶液中,b点水的电离程度最大 |
| D.c点溶液中:2c(Cl-)=c(Na+) |
您最近一年使用:0次
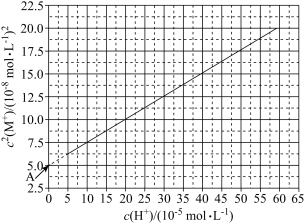
4 . HA是一元弱酸,其电离常数为Ka,难溶盐MA的溶度积为Ksp,M+不发生水解。将一定量固体MA加入水中,向溶液中加入不含A元素、M元素的酸或者碱调节pH,此过程中固体始终有剩余。实验发现,298K时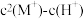 为线性关系,如下图中实线所示。回答下列问题。
为线性关系,如下图中实线所示。回答下列问题。
(1)定义: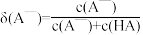 ,则
,则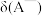 =
=___________ 。(用含Ka和c(H+)的式子表示)。
(2)不论加入酸或者碱的量如何,c(M+)与含A粒子之间的关系式为___________ 。
(3)写出c2(M+)与c(H+)之间的关系式___________ 。(用含Ka和Ksp的式子表示)。
(4)结合图象数据可得Ksp=___________ 和Ka=___________ 。
(5)图象中靠近A点的虚线表示实际很难测得,A点实际是反向延长得到的,解释为什么实际中测不到A点的数据。___________ 。注:此题改编自2021年高考选择题最后一题,同学们考后可思考若难溶盐为MA2,则是否还存在如图象的线性关系?
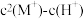 为线性关系,如下图中实线所示。回答下列问题。
为线性关系,如下图中实线所示。回答下列问题。
(1)定义:
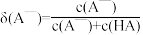 ,则
,则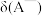 =
=(2)不论加入酸或者碱的量如何,c(M+)与含A粒子之间的关系式为
(3)写出c2(M+)与c(H+)之间的关系式
(4)结合图象数据可得Ksp=
(5)图象中靠近A点的虚线表示实际很难测得,A点实际是反向延长得到的,解释为什么实际中测不到A点的数据。
您最近一年使用:0次
名校
5 . 常温下,向 一定浓度的硝酸银溶液中逐滴加入
一定浓度的硝酸银溶液中逐滴加入 的氨水,反应过程中
的氨水,反应过程中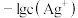 或
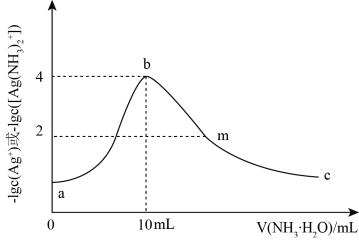
或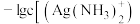 与加入氨水体积的关系如图所示。下列说法正确的是
与加入氨水体积的关系如图所示。下列说法正确的是
 一定浓度的硝酸银溶液中逐滴加入
一定浓度的硝酸银溶液中逐滴加入 的氨水,反应过程中
的氨水,反应过程中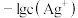 或
或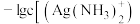 与加入氨水体积的关系如图所示。下列说法正确的是
与加入氨水体积的关系如图所示。下列说法正确的是
A.原硝酸银溶液的浓度是 |
B.反应生成氢氧化银的 的数量级为 的数量级为 |
C. 的浓度b点小于m点 的浓度b点小于m点 |
D.溶液m点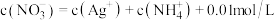 |
您最近一年使用:0次
解题方法
6 . 一定温度下,AgCl(s) Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl−)的关系如图所示。下列说法错误的是
Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl−)的关系如图所示。下列说法错误的是
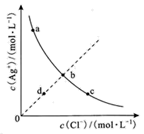
 Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl−)的关系如图所示。下列说法错误的是
Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl−)的关系如图所示。下列说法错误的是
| A.a、b、c三点对应的Kw相等 |
| B.往d点的溶液中加入AgNO3溶液,可能会变到a点 |
| C.AgCl在a点的溶解度一定比c点的大 |
| D.该温度下,AgBr的溶解平衡曲线可能与线段bd相交 |
您最近一年使用:0次
2021-10-18更新
|
379次组卷
|
3卷引用:广东省“六校联盟”2021-2022学年高三上学期第二次联考化学试题
广东省“六校联盟”2021-2022学年高三上学期第二次联考化学试题河北省衡水市第十四中学(西校区)2021-2022学年高二上学期二调考试化学试题(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)
7 . 某科研课题小组研究利用含H+、Na+、Zn2+、Mn2+、Fe2+、Fe3+、SO 的工业废电解质溶液,制备高纯的ZnO、MnO2、Fe2O3,设计实验流程如图:
的工业废电解质溶液,制备高纯的ZnO、MnO2、Fe2O3,设计实验流程如图:
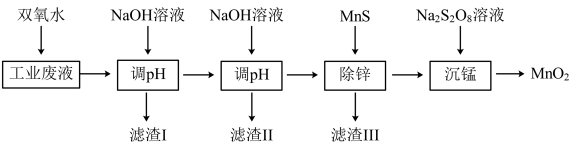
回答下列问题:
(1)加入双氧水的目的是___ 。
(2)第一次调pH使Fe3+完全沉淀,写出反应的离子方程___ 。
(3)第二次调pH前,科研小组成员分析此时的溶液,得到常温下相关数据如表(表中金属离子沉淀完全时,其浓度为1×10-5mol·L-1)。
为防止Mn2+同时沉淀造成产品不纯,最终选择将溶液的pH控制为7,则此时溶液中Zn2+的沉淀率为___ ,利用滤渣Ⅱ制备高纯的ZnO时,必然含有极其微量的___ (以化学式表示)。
(4)已知常温下,Ksp(MnS)=3.0×10-14,Ksp(ZnS)=1.5×10-24,在除锌时发生沉淀转化反应为:MnS(s)+Zn2+(aq) ZnS(s)+Mn2+(aq),其平衡常数K=
ZnS(s)+Mn2+(aq),其平衡常数K=___ 。(填数值)
(5)沉锰反应在酸性条件下完成,写出该反应的离子方程式___ 。
 的工业废电解质溶液,制备高纯的ZnO、MnO2、Fe2O3,设计实验流程如图:
的工业废电解质溶液,制备高纯的ZnO、MnO2、Fe2O3,设计实验流程如图:
回答下列问题:
(1)加入双氧水的目的是
(2)第一次调pH使Fe3+完全沉淀,写出反应的离子方程
(3)第二次调pH前,科研小组成员分析此时的溶液,得到常温下相关数据如表(表中金属离子沉淀完全时,其浓度为1×10-5mol·L-1)。
| 浓度/(mol·L-1) | 氢氧化物的Ksp | 开始沉淀的pH | 沉淀完全的pH | |
| Zn2+ | 0.12 | 1.2×10-17 | 6.0 | 8.1 |
| Mn2+ | 0.10 | 4.0×10-14 | 7.8 | 9.8 |
(4)已知常温下,Ksp(MnS)=3.0×10-14,Ksp(ZnS)=1.5×10-24,在除锌时发生沉淀转化反应为:MnS(s)+Zn2+(aq)
 ZnS(s)+Mn2+(aq),其平衡常数K=
ZnS(s)+Mn2+(aq),其平衡常数K=(5)沉锰反应在酸性条件下完成,写出该反应的离子方程式
您最近一年使用:0次
8 . Ⅰ.金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(S/mol·L-1)如图所示。
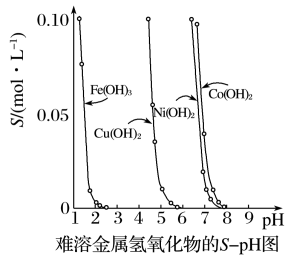
(1)pH=3时溶液中铜元素的主要存在形式是___ (写化学式)。
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为___ 。
A.3左右 B.4左右 C.2左右
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,___ (填“能”或“不能”)通过调节溶液pH的方法来除去,理由是___ 。
(4)已知一些难溶物的溶度积常数如表:
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的___ 除去它们。
A.NaOH B.FeS C.Na2S
Ⅱ.某小组同学进行如图实验探究:
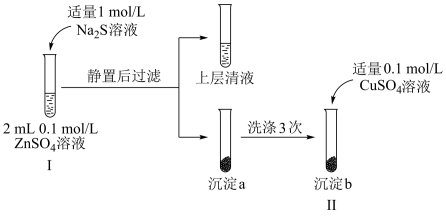
(5)预通过实验Ⅰ和实验Ⅱ证明Ksp(ZnS)<Ksp(CuS),实验Ⅰ中加入1mol•L-1Na2S的体积范围为:___ 。
(6)试管Ⅱ中观察到白色沉淀转化为黑色沉淀。请结合化学用语,从平衡移动的角度进行解释___ 。
(7)若将沉淀a洗涤3次后,加适量0.1mol/LFeSO4溶液,是否能看到白色沉淀转化为黑色沉淀,请结合计算予以说明___ 。

(1)pH=3时溶液中铜元素的主要存在形式是
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为
A.3左右 B.4左右 C.2左右
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,
(4)已知一些难溶物的溶度积常数如表:
| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-36 | 3.4×10-28 | 6.4×10-53 | 1.6×10-24 |
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的
A.NaOH B.FeS C.Na2S
Ⅱ.某小组同学进行如图实验探究:

(5)预通过实验Ⅰ和实验Ⅱ证明Ksp(ZnS)<Ksp(CuS),实验Ⅰ中加入1mol•L-1Na2S的体积范围为:
| 难溶电解质 | 颜色 | Ksp的数值(18~25℃) |
| ZnS | 白色 | 1.6×10-24 |
| CuS | 黑色 | 1.3×10-36 |
| FeS | 黑色 | 6.3×10-18 |
(6)试管Ⅱ中观察到白色沉淀转化为黑色沉淀。请结合化学用语,从平衡移动的角度进行解释
(7)若将沉淀a洗涤3次后,加适量0.1mol/LFeSO4溶液,是否能看到白色沉淀转化为黑色沉淀,请结合计算予以说明
您最近一年使用:0次
名校
解题方法
9 . Ⅰ.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过0.005mg/L。处理含镉废水可采用化学沉淀法。试回答下列问题:
(1)磷酸镉[Cd3(PO4)2]沉淀溶解平衡常数的表达式为Ksp=___________ 。
(2)一定温度下,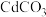 的
的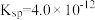 ,
, 的
的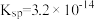 ,那么它们在水中的溶解量
,那么它们在水中的溶解量___________ 较大。
(3)向某含镉废水中加入 ,当
,当 浓度达到
浓度达到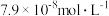 时,废水中
时,废水中 的浓度为
的浓度为___________ mol/L[已知: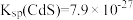 ,
,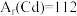 ],此时是否符合生活饮用水卫生标准?
],此时是否符合生活饮用水卫生标准?___________ (填“是”或“否”)。
Ⅱ.根据题目提供的溶度积数据进行计算并回答下列问题:
(4)已知25℃时,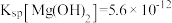 ;酸碱指示剂百里酚蓝变色的pH范围如下:
;酸碱指示剂百里酚蓝变色的pH范围如下:
25℃时,向 饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为
饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为___________ 。
(5)25℃向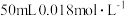 的
的 溶液中加入
溶液中加入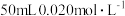 的盐酸,生成沉淀。已知该温度下,AgCl的
的盐酸,生成沉淀。已知该温度下,AgCl的 ,忽略溶液的体积变化,请计算:
,忽略溶液的体积变化,请计算:
①完全沉淀后,溶液中 =
=___________ ,
②完全沉淀后,溶液的pH=___________ 。
③如果向完全沉淀后的溶液中继续加入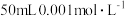 的盐酸,是否有白色沉淀生成?
的盐酸,是否有白色沉淀生成?___________ (填“是”或“否”)。
(1)磷酸镉[Cd3(PO4)2]沉淀溶解平衡常数的表达式为Ksp=
(2)一定温度下,
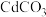 的
的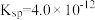 ,
, 的
的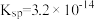 ,那么它们在水中的溶解量
,那么它们在水中的溶解量(3)向某含镉废水中加入
 ,当
,当 浓度达到
浓度达到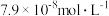 时,废水中
时,废水中 的浓度为
的浓度为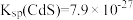 ,
,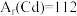 ],此时是否符合生活饮用水卫生标准?
],此时是否符合生活饮用水卫生标准?Ⅱ.根据题目提供的溶度积数据进行计算并回答下列问题:
(4)已知25℃时,
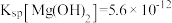 ;酸碱指示剂百里酚蓝变色的pH范围如下:
;酸碱指示剂百里酚蓝变色的pH范围如下: |  | 8.0~96 | 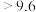 |
| 颜色 | 黄色 | 绿色 | 蓝色 |
 饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为
饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为(5)25℃向
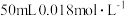 的
的 溶液中加入
溶液中加入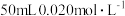 的盐酸,生成沉淀。已知该温度下,AgCl的
的盐酸,生成沉淀。已知该温度下,AgCl的 ,忽略溶液的体积变化,请计算:
,忽略溶液的体积变化,请计算:①完全沉淀后,溶液中
 =
=②完全沉淀后,溶液的pH=
③如果向完全沉淀后的溶液中继续加入
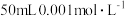 的盐酸,是否有白色沉淀生成?
的盐酸,是否有白色沉淀生成?
您最近一年使用:0次
2021-10-13更新
|
1432次组卷
|
6卷引用:河北省石家庄市第一中学2021-2022学年高二上学期10月月考化学试卷
河北省石家庄市第一中学2021-2022学年高二上学期10月月考化学试卷(已下线)必考点08 沉淀溶解平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)(已下线)3.4.1 难溶电解质的沉淀溶解平衡-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第三章 水溶液中的离子平衡-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第21讲 难溶电解质的沉淀溶解平衡(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
名校
解题方法
10 . 在 饱和溶液中加入少量的
饱和溶液中加入少量的 溶液产生
溶液产生 沉淀,若以Ksp表示
沉淀,若以Ksp表示 的溶度积常数,则平衡后溶液中
的溶度积常数,则平衡后溶液中
 饱和溶液中加入少量的
饱和溶液中加入少量的 溶液产生
溶液产生 沉淀,若以Ksp表示
沉淀,若以Ksp表示 的溶度积常数,则平衡后溶液中
的溶度积常数,则平衡后溶液中A. |
B.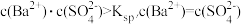 |
C. |
D.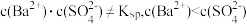 |
您最近一年使用:0次
2021-10-13更新
|
473次组卷
|
3卷引用:河北省石家庄市第一中学2021-2022学年高二上学期10月月考化学试卷
河北省石家庄市第一中学2021-2022学年高二上学期10月月考化学试卷浙江省金衢六校联盟2021-2022学年高二上学期期末联考化学试题(已下线)第33练 沉淀溶解平衡-2023年高考化学一轮复习小题多维练(全国通用)



