名校
1 . 已知: (白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
(白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
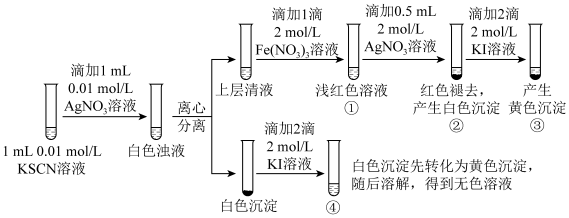
下列说法中,不正确 的是
 (白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
(白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
下列说法中,
A.①中现象能说明 与 与 生成的白色浊液中存在沉淀溶解平衡 生成的白色浊液中存在沉淀溶解平衡 |
B.②中现象产生的原因是发生了反应: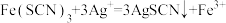 |
| C.③中产生黄色沉淀的现象能证明AgI的溶解度比AgSCN的溶解度小 |
D.④中黄色沉淀溶解的原因可能是AgI与KI溶液中的 进一步发生了反应 进一步发生了反应 |
您最近一年使用:0次
2021-11-15更新
|
697次组卷
|
3卷引用:辽宁省大连市第八中学2021-2022学年高三上学期12月月考化学试题
辽宁省大连市第八中学2021-2022学年高三上学期12月月考化学试题北京市北师大附属实验中学2021-2022学年高二上学期期中考试化学试题(已下线)第21讲 难溶电解质的沉淀溶解平衡(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
名校
解题方法
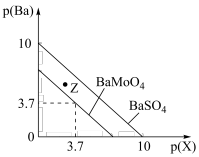
2 . 已知:BaMoO4、BaSO4均难溶于水,lg2≈0.3,离子浓度≤10-5mol/L时认为其沉淀完全。T℃时,BaMoO4、BaSO4的沉淀溶解平衡曲线如图所示,其中p(Ba)=-lgc(Ba2+),p(X)=-lgc(MoO )或-lgc(SO
)或-lgc(SO )。下列叙述正确的是
)。下列叙述正确的是
 )或-lgc(SO
)或-lgc(SO )。下列叙述正确的是
)。下列叙述正确的是
| A.T℃时,Z点对应为BaMoO4的不饱和溶液 |
| B.T℃时,向等浓度的Na2SO4和Na2MoO4的混合溶液中加入BaCl2溶液,先析出BaMoO4沉淀 |
| C.T℃时,Ksp(BaMoO4)的数量级为10-7 |
D.T℃时,BaMoO4(s)+SO  BaSO4(s)+MoO BaSO4(s)+MoO 的平衡常数K=200 的平衡常数K=200 |
您最近一年使用:0次
2021-11-14更新
|
708次组卷
|
6卷引用:重庆市朝阳中学2021-2022学年高二12月月考化学试题
3 . 下列化学用语表示正确的是
A.醋酸的电离: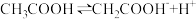 |
B.硫酸氢钠在水溶液中的电离: |
C.氯化铵的水解: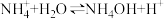 |
D.氯化银的沉淀溶解平衡: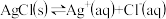 |
您最近一年使用:0次
2021-11-11更新
|
272次组卷
|
3卷引用:黑龙江省哈尔滨市宾县第二中学2021-2022学年高二上学期第二次月考化学试题
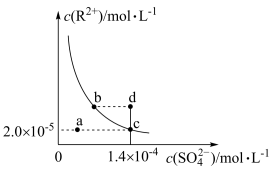
4 . 常温下某盐 在水中的溶解平衡曲线如图所示,下列说法错误的是
在水中的溶解平衡曲线如图所示,下列说法错误的是
 在水中的溶解平衡曲线如图所示,下列说法错误的是
在水中的溶解平衡曲线如图所示,下列说法错误的是
A.a点体系中存在平衡: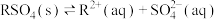 |
B.d点对应的体系中,分散质粒子直径大于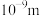 |
C.b、c两点均为 的饱和溶液 的饱和溶液 |
D.常温下 |
您最近一年使用:0次
2021-11-06更新
|
135次组卷
|
3卷引用:广东省普通高中2021-2022学年上学期高三11月阶段性质量检测化学试题
解题方法
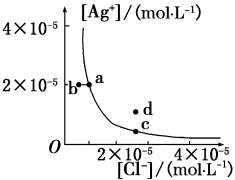
5 . 某温度时,AgCl(s) Ag+(aq)+Cl﹣(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
Ag+(aq)+Cl﹣(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
 Ag+(aq)+Cl﹣(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
Ag+(aq)+Cl﹣(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
| A.c点对应的Ksp等于a点对应的Ksp |
| B.加入AgNO3,可以使溶液由c点变到d点 |
| C.d点没有AgCl沉淀生成 |
| D.加入少量水,AgCl固体仍有剩余,平衡右移,Cl-浓度减小 |
您最近一年使用:0次
2021-11-03更新
|
440次组卷
|
3卷引用:吉林省长岭县第二中学2021-2022学年高二上学期第一次考试化学试题
名校
解题方法
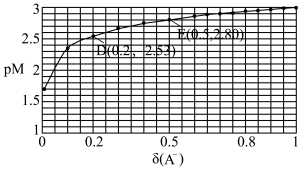
6 . HA是一元弱酸,微溶盐MA2的饱和溶液中c(M2+)随c(H+)而变化,M2+不发生水解。定义如下关系:pM=-lgc(M2+),δ(A-)= 。25℃时,实验测得pM与δ(A-)的关系如下图所示,其中D点对应的pH=5.0.已知lg2≈0.3,则下列说法正确的是
。25℃时,实验测得pM与δ(A-)的关系如下图所示,其中D点对应的pH=5.0.已知lg2≈0.3,则下列说法正确的是
 。25℃时,实验测得pM与δ(A-)的关系如下图所示,其中D点对应的pH=5.0.已知lg2≈0.3,则下列说法正确的是
。25℃时,实验测得pM与δ(A-)的关系如下图所示,其中D点对应的pH=5.0.已知lg2≈0.3,则下列说法正确的是
| A.D点存在2c(M2+)=3c(HA) |
| B.E点的pH≈5.6 |
| C.25℃时,Ksp(MA2)的数量级为10-10 |
| D.25℃时,HA的电离常数:Ka为2.5×10-5 |
您最近一年使用:0次
2021-11-01更新
|
709次组卷
|
6卷引用:河南省部分名校2021-2022学年高三上学期第一次阶段性测试理综化学试题
河南省部分名校2021-2022学年高三上学期第一次阶段性测试理综化学试题新疆岳普湖县2021-2022学年高二下学期第一次学情调研测试化学试题(已下线)专题19 沉淀溶解平衡的图像问题分析-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)第八章 水溶液中的离子反应与平衡 第54讲 水溶液中四大平衡常数的综合应用(已下线)微专题 水溶液中四大平衡常数的综合应用四川省泸州市叙永第一中学校2023-2024学年高二上学期1月期末化学试题
名校
7 . 下列化学用语的表达正确的是
A. +H2O =NH3·H2O+H+ +H2O =NH3·H2O+H+ |
B.Na2SO3+2H2O 2NaOH+ 2H2SO3 2NaOH+ 2H2SO3 |
C.NaHCO3=Na++H++ |
D.BaSO4(s) Ba 2+(aq)+ Ba 2+(aq)+ (aq) (aq) |
您最近一年使用:0次
名校
8 . 天然石灰石是工业生产中重要的原材料之一,它的主要成分是CaCO3,一般以CaO的质量分数表示钙含量,常采用高锰酸钾法测定。步骤如下:
I.称取ag研细的石灰石样品于250mL烧杯中,加过量稀盐酸溶解,水浴加热10分钟;
II.稍冷后逐滴加入氨水至溶液pH≈4,再缓慢加入适量(NH4)2C2O4溶液,继续水浴加热30分钟;
III.冷却至室温后过滤出沉淀,用另外配制的稀(NH4)2C2O4溶液洗涤沉淀三次,再用蒸馏水洗涤至洗涤液中无法检出Cl−;
IV.加入适量热的稀硫酸至沉淀中,获得的溶液用cmol·L−1KMnO4标准溶液滴定至终点。
V.平行测定三次,消耗KMnO4溶液的体积平均为VmL。
已知:H2C2O4是弱酸;CaC2O4是难溶于水的白色沉淀。
(1)I中为了加快反应速率而采取的操作有___________ 。
(2)II中加入氨水调节溶液pH的作用是___________ 。
(3)III中洗涤得到干净的沉淀。
①结合平衡移动原理,解释用稀(NH4)2C2O4溶液洗涤沉淀的目的___________ 。
②验证沉淀是否洗涤干净的操作是___________ 。
③若沉淀中的Cl−未洗涤干净,则最终测量结果___________ (填“偏大”、“偏小”或“不变”)。
(4)IV中用KMnO4标准溶液滴定。
①滴定时发生反应的离子方程式为___________ 。
②滴定至终点的现象为___________ 。
③样品中以CaO质量分数表示的钙含量为___________ (列出表达式)。
I.称取ag研细的石灰石样品于250mL烧杯中,加过量稀盐酸溶解,水浴加热10分钟;
II.稍冷后逐滴加入氨水至溶液pH≈4,再缓慢加入适量(NH4)2C2O4溶液,继续水浴加热30分钟;
III.冷却至室温后过滤出沉淀,用另外配制的稀(NH4)2C2O4溶液洗涤沉淀三次,再用蒸馏水洗涤至洗涤液中无法检出Cl−;
IV.加入适量热的稀硫酸至沉淀中,获得的溶液用cmol·L−1KMnO4标准溶液滴定至终点。
V.平行测定三次,消耗KMnO4溶液的体积平均为VmL。
已知:H2C2O4是弱酸;CaC2O4是难溶于水的白色沉淀。
(1)I中为了加快反应速率而采取的操作有
(2)II中加入氨水调节溶液pH的作用是
(3)III中洗涤得到干净的沉淀。
①结合平衡移动原理,解释用稀(NH4)2C2O4溶液洗涤沉淀的目的
②验证沉淀是否洗涤干净的操作是
③若沉淀中的Cl−未洗涤干净,则最终测量结果
(4)IV中用KMnO4标准溶液滴定。
①滴定时发生反应的离子方程式为
②滴定至终点的现象为
③样品中以CaO质量分数表示的钙含量为
您最近一年使用:0次
名校
9 . 石灰乳中存在下列平衡:Ca(OH)2(s) Ca2+(aq)+2OH-(aq);加入下列溶液,可使固体明显减少的是
Ca2+(aq)+2OH-(aq);加入下列溶液,可使固体明显减少的是
 Ca2+(aq)+2OH-(aq);加入下列溶液,可使固体明显减少的是
Ca2+(aq)+2OH-(aq);加入下列溶液,可使固体明显减少的是| A.Na2CO3溶液 | B.KCl溶液 |
| C.NaOH溶液 | D.CaCl2溶液 |
您最近一年使用:0次
2021-10-28更新
|
698次组卷
|
9卷引用:新疆喀什第二中学2021-2022学年高二11月月考化学试题
新疆喀什第二中学2021-2022学年高二11月月考化学试题(已下线)考向27 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点微专题(已下线)专题27 难溶电解质的溶解平衡(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练2015-2016学年福建省长泰县第一中学高二上学期期末化学试卷陕西省黄陵中学2018-2019学年高二(重点班)上学期期中考试化学试题(已下线)3.4.1 沉淀溶解平衡-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)(已下线)第21讲 难溶电解质的沉淀溶解平衡(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)水溶液中的离子反应与平衡——课时6沉淀溶解平衡宁夏开元学校2023-2024学年高二学年下学期开学收心测试化学试题
解题方法
10 . AlPO4的沉淀溶解平衡曲线如图所示。下列说法不正确的
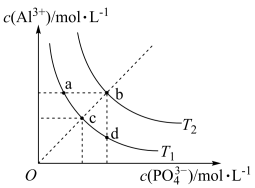

| A.T1一定大于T2 |
| B.AlPO4在b点对应的溶解度大于c点 |
| C.图中四个点的Ksp:a=c=d<b |
| D.T1温度下,在AlPO4的饱和溶液中加入AlCl3可使溶液由c点变到a点 |
您最近一年使用:0次



