名校
1 . 一种三室微生物燃料电池的工作原理如图所示,该电池能同时去除有机物、脱氮形成无害气体和水。下列说法不正确 的是
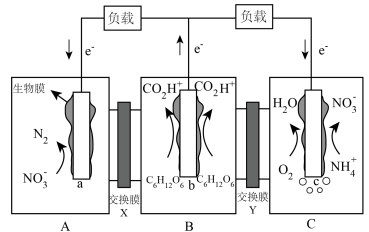

| A.X、Y交换膜均为质子交换膜 |
| B.电极室C中溶液经灭菌后通入电极室A |
C.b电极反应式: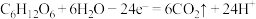 |
| D.电极室C中仅发生还原反应 |
您最近半年使用:0次
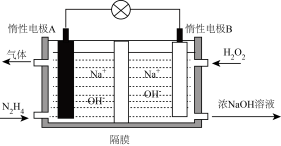
2 . 肼( )-双氧水燃料电池由于绿色环保且具有较高的能量密度而广受关注,其工作原理如图所示。下列说法错误的是
)-双氧水燃料电池由于绿色环保且具有较高的能量密度而广受关注,其工作原理如图所示。下列说法错误的是
 )-双氧水燃料电池由于绿色环保且具有较高的能量密度而广受关注,其工作原理如图所示。下列说法错误的是
)-双氧水燃料电池由于绿色环保且具有较高的能量密度而广受关注,其工作原理如图所示。下列说法错误的是
A.该电池正极反应式为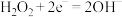 |
| B.电池工作过程中A极区溶液pH增大 |
| C.隔膜为阳离子交换膜 |
D.电池工作时,外电路通过2mol  时,A极区产生气体11.2L 时,A极区产生气体11.2L |
您最近半年使用:0次
3 . 下列有关原电池的说法正确的是
| A.活泼的金属不一定作负极 | B.电池工作时,正极失去电子 |
| C.电池工作时,负极发生还原反应 | D.电解质溶液一定不能为浓硝酸 |
您最近半年使用:0次
名校
解题方法
4 . Mg-H2O2电池可用于驱动无人驾收的潜航器。该电池以海水为电解质资液,示意图如图,该电池工作时,下列说法不正确的是
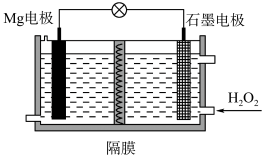

| A.Mg电极是该电池的负极 |
| B.溶液中Cl-向正极移动 |
| C.石墨电极附近溶液的pH增大 |
| D.若在石墨电极区加入一定量盐酸,则发生的电极反应式为:2H++H2O2+2e-=2H2O |
您最近半年使用:0次
名校
解题方法
5 . 锂二氧化碳电池可在常温下同时实现二氧化碳的锚定与转化,可以在深海作业、火星探测等高二氧化碳的环境中得到应用,电池总反应为:4Li+3CO2  2Li2CO3+C,下列说法错误的是
2Li2CO3+C,下列说法错误的是
 2Li2CO3+C,下列说法错误的是
2Li2CO3+C,下列说法错误的是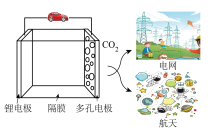
| A.该电池不能用水溶液作为电解液 |
B.放电时,正极的电极反应为: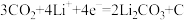 |
| C.充电时,若以铅蓄电池为电源,则锂电极应与Pb极相连接 |
| D.充电时,当生成3.36L(标准状况下) CO2,通过隔膜迁移的Li+数目为0.4NA |
您最近半年使用:0次
2023-12-11更新
|
178次组卷
|
3卷引用:福建省南平市高级中学2023-2024学年高二上学期期中考试化学试题
福建省南平市高级中学2023-2024学年高二上学期期中考试化学试题(已下线)专题07 原电池-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)宁夏开元学校2023-2024学年高二上学期期末考试化学试题
名校
解题方法
6 . 碱性银锌二次航空电池为价格昂贵的高能电池。该电池的总反应为: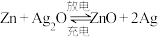 ,其电池中的基本单元示意图如下:
,其电池中的基本单元示意图如下:
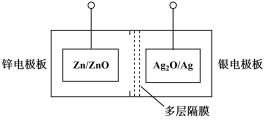
(1)该电池放电时,银电极板为电池的___________ (填“正极”或“负极”)。
(2)以KOH溶液为电解液,放电时锌电极板区域中发生的电极反应可分为两步:
反应ⅰ.锌电极板的溶解:∙∙∙∙∙∙
反应ⅱ.锌电极板上ZnO的析出:
补充反应ⅰ:___________ 。
(3)放电时,析出的ZnO会覆盖在锌电极板表面,影响电池使用效果。用浓KOH溶液可以抑制ZnO的生成,并促进锌电极板的溶解,请结合化学用语,从速率和平衡的角度说明原因:_______ 。
(4)将锌电极板制成蜂窝孔状,如图a所示,能增大锌电极板的表面积,但蜂窝孔的孔径过小,影响 进出蜂窝孔的速率,导致孔径内外
进出蜂窝孔的速率,导致孔径内外 浓度出现差异,多次充放电后会影响锌电极板的形状。图b是使用一段时间后的锌极板变形情况。
浓度出现差异,多次充放电后会影响锌电极板的形状。图b是使用一段时间后的锌极板变形情况。
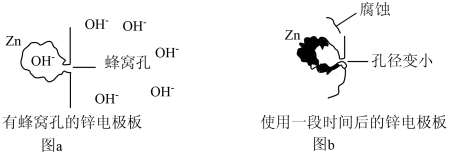
下列说法正确的是___________ (填字母序号)。
a.充电时, 向锌极板方向迁移
向锌极板方向迁移
b.孔内沉积ZnO,导电能力减弱,影响电池使用效果
c.导致该腐蚀变形的主要原因是孔外 浓度高于孔内
浓度高于孔内 浓度
浓度
d.为延长电池使用寿命,提高电池放电效果,应选用孔径恰当的锌极板
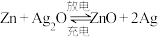 ,其电池中的基本单元示意图如下:
,其电池中的基本单元示意图如下:
(1)该电池放电时,银电极板为电池的
(2)以KOH溶液为电解液,放电时锌电极板区域中发生的电极反应可分为两步:
反应ⅰ.锌电极板的溶解:∙∙∙∙∙∙
反应ⅱ.锌电极板上ZnO的析出:

补充反应ⅰ:
(3)放电时,析出的ZnO会覆盖在锌电极板表面,影响电池使用效果。用浓KOH溶液可以抑制ZnO的生成,并促进锌电极板的溶解,请结合化学用语,从速率和平衡的角度说明原因:
(4)将锌电极板制成蜂窝孔状,如图a所示,能增大锌电极板的表面积,但蜂窝孔的孔径过小,影响
 进出蜂窝孔的速率,导致孔径内外
进出蜂窝孔的速率,导致孔径内外 浓度出现差异,多次充放电后会影响锌电极板的形状。图b是使用一段时间后的锌极板变形情况。
浓度出现差异,多次充放电后会影响锌电极板的形状。图b是使用一段时间后的锌极板变形情况。
下列说法正确的是
a.充电时,
 向锌极板方向迁移
向锌极板方向迁移b.孔内沉积ZnO,导电能力减弱,影响电池使用效果
c.导致该腐蚀变形的主要原因是孔外
 浓度高于孔内
浓度高于孔内 浓度
浓度d.为延长电池使用寿命,提高电池放电效果,应选用孔径恰当的锌极板
您最近半年使用:0次
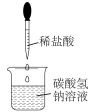
7 . 市场出售的“暖贴”中主要成分是铁粉、炭粉、木屑、少量氯化钠和水等,“暖贴”用塑料袋密封,使用时从塑料袋中取出轻轻揉搓就会释放热量,用完后袋内有大量铁锈生成。下列说法正确的是
| A.“暖贴”工作时,氯离子移向负极 |
| B.铁锈具有磁性,常用作橡胶的黑色颜料 |
| C.“暖贴”工作时的能量变化与图示能量变化相符 |
| D.工业上钠的制取是通过电解氯化钠饱和溶液的方法 |
您最近半年使用:0次
2023-12-06更新
|
53次组卷
|
2卷引用:辽宁省葫芦岛市协作校2023-2024学年高三上学期第二次考试化学试题
解题方法
8 . 近日,科学家设计一种具有石墨正极的高容量可充电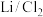 锂金属电池,原理如图所示。氯化铝(
锂金属电池,原理如图所示。氯化铝( )溶解在亚硫酰氯(
)溶解在亚硫酰氯( )中,以氟化物(
)中,以氟化物( )为添加剂作为电解质。回答下列问题:
)为添加剂作为电解质。回答下列问题:
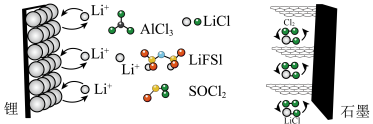
(1)放电时,能量主要转化形式是___________ 。
(2)放电时,锂离子由___________ (填“锂”或“石墨”,下同)极向___________ 极迁移,石墨极反应式为___________ 。
(3)充电时,石墨极与电源___________ (填“正”或“负”)极连接。转移 个电子时锂电极理论上净增
个电子时锂电极理论上净增___________ g锂( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(4)该装置不能使用水、醇、酸作溶剂,其理由是___________ 。
(5) 在
在 中完全燃烧放出热量为
中完全燃烧放出热量为 。写出热化学方程式:
。写出热化学方程式:___________ 。
(6)工业上制备亚硫酰氯: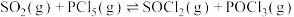
 。下列措施能提高
。下列措施能提高 平衡转化率的是___________(填字母)。
平衡转化率的是___________(填字母)。
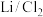 锂金属电池,原理如图所示。氯化铝(
锂金属电池,原理如图所示。氯化铝( )溶解在亚硫酰氯(
)溶解在亚硫酰氯( )中,以氟化物(
)中,以氟化物( )为添加剂作为电解质。回答下列问题:
)为添加剂作为电解质。回答下列问题: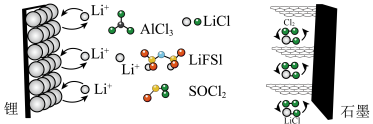
(1)放电时,能量主要转化形式是
(2)放电时,锂离子由
(3)充电时,石墨极与电源
 个电子时锂电极理论上净增
个电子时锂电极理论上净增 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。(4)该装置不能使用水、醇、酸作溶剂,其理由是
(5)
 在
在 中完全燃烧放出热量为
中完全燃烧放出热量为 。写出热化学方程式:
。写出热化学方程式:(6)工业上制备亚硫酰氯:
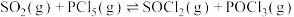
 。下列措施能提高
。下列措施能提高 平衡转化率的是___________(填字母)。
平衡转化率的是___________(填字母)。| A.升高温度 | B.增大压强 | C.加入催化剂 | D.分离 |
您最近半年使用:0次
解题方法
9 . 中国科学院将分子 引入电解质中调整充电和放电反应途径,实现了高功率可充电
引入电解质中调整充电和放电反应途径,实现了高功率可充电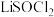 电池,工作原理如下图所示。下列有关说法错误的是
电池,工作原理如下图所示。下列有关说法错误的是
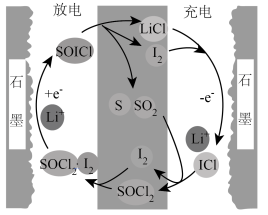
 引入电解质中调整充电和放电反应途径,实现了高功率可充电
引入电解质中调整充电和放电反应途径,实现了高功率可充电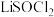 电池,工作原理如下图所示。下列有关说法错误的是
电池,工作原理如下图所示。下列有关说法错误的是
A.分子 的引入催化了电池放电和充电过程 的引入催化了电池放电和充电过程 |
| B.电池工作环境必须在无水无氧的条件下进行 |
C.充电时阴极反应式: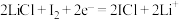 |
D.电池的放电总反应: |
您最近半年使用:0次
名校
10 . 重铬酸铵[(NH4)2Cr2O7](M=252 g·mol-1)常用作分析试剂、催化剂及媒染剂等。某化学兴趣小组对重铬酸铵的一些性质及组成进行探究。已知: + H2O
+ H2O 2
2 +2H+。回答下列问题:
+2H+。回答下列问题:
(1)在试管中加入少量重铬酸铵样品,滴加足量6 mol·L-1 NaOH溶液,振荡、微热。产生的现象是______________________ 。
(2)为探究重铬酸铵的分解产物,按下图连接好装置,在A中加入2.52 g重铬酸铵样品进行实验。

①实验过程中通入N2的主要目的是___________ 。
②实验过程中,若发现加热温度不够,如何改进?___________ 。
③C装置的作用是___________ 。加热A至恒重,观察到B中固体由白变蓝,D中酚酞溶液不变色,同时测得A中剩余固体1.52 g、B增重0.72 g,另外分解产物中还含有N2,则重铬酸铵受热分解的化学方程式为___________ 。
(3)为探究溶液酸性增强对铬(VI)盐溶液氧化性或Na2SO3溶液还原性的影响,该小组利用下图装置继续实验(已知物质氧化性与还原性强弱差异越大,电压越大)。

a.K闭合时,记录电压。
b.向U型管左侧溶液中滴加硫酸至pH=2后,电压增大了y。
c.继续向U型管右侧溶液中滴加硫酸后,无气体逸出,电压几乎不变。
①上述实验得出结论:___________ ;酸性增强,对Na2SO3溶液还原性几乎无影响。
②有同学认为:随着溶液酸性的增强,溶液中O2的氧化性增强也会使电压增大。补做实验:U型管左管中改为盛放___________ 溶液;然后向左管中滴加硫酸至pH=2后,测得电压增大了z,若z_____ y(填“>”、“<”或“=”),则证明实验结论不受影响。
 + H2O
+ H2O 2
2 +2H+。回答下列问题:
+2H+。回答下列问题:(1)在试管中加入少量重铬酸铵样品,滴加足量6 mol·L-1 NaOH溶液,振荡、微热。产生的现象是
(2)为探究重铬酸铵的分解产物,按下图连接好装置,在A中加入2.52 g重铬酸铵样品进行实验。

①实验过程中通入N2的主要目的是
②实验过程中,若发现加热温度不够,如何改进?
③C装置的作用是
(3)为探究溶液酸性增强对铬(VI)盐溶液氧化性或Na2SO3溶液还原性的影响,该小组利用下图装置继续实验(已知物质氧化性与还原性强弱差异越大,电压越大)。

a.K闭合时,记录电压。
b.向U型管左侧溶液中滴加硫酸至pH=2后,电压增大了y。
c.继续向U型管右侧溶液中滴加硫酸后,无气体逸出,电压几乎不变。
①上述实验得出结论:
②有同学认为:随着溶液酸性的增强,溶液中O2的氧化性增强也会使电压增大。补做实验:U型管左管中改为盛放
您最近半年使用:0次



