名校
解题方法
1 . 某校化学小组探究 与
与 溶液的反应,进行了如下实验(以下实验过程中溶液体积变化忽略不计):
溶液的反应,进行了如下实验(以下实验过程中溶液体积变化忽略不计):
(1)对比实验i、ii、iii,说明反应速率与___________ 有关。
(2)为了探究淡黄色固体的成分,甲同学进行实验:取实验iv试管壁上的淡黄色固体,发现其微溶于乙醇,易溶于 ,淡黄色固体是
,淡黄色固体是___________ 。
(3)根据上述实验现象,甲同学猜测一定有单质碘生成,猜测的理论依据是___________ ,但实验中溶液始终没有变蓝。
(4)利用如图装置继续实验,证实了单质碘可以生成。实验现象是___________ 。
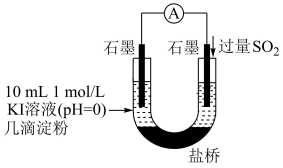
(5)对于实验i、ii、iii未能检测到单质碘,甲同学继续实验
根据(2)(4)(5)的实验现象,结合化学反应原理解释实验iv中始终未检测到单质碘的原因是___________ 。
(6)根据上述一系列实验,乙同学大胆猜测,整个反应中 起到了催化剂作用,为了证明乙同学的猜想正确,还需要的实验证据是
起到了催化剂作用,为了证明乙同学的猜想正确,还需要的实验证据是___________ 。
实验结果证实了猜想,则总反应的化学方程式是___________ 。
 与
与 溶液的反应,进行了如下实验(以下实验过程中溶液体积变化忽略不计):
溶液的反应,进行了如下实验(以下实验过程中溶液体积变化忽略不计):| 实验 | 实验操作 | 实验现象 |
| i | 取 淀粉 淀粉 溶液 溶液 ,通入 ,通入 至量 至量 | 溶液慢慢变为浅黄色 |
| ii | 取 淀粉 淀粉 溶液 溶液 ,通入 ,通入 至过量 至过量 | 溶液迅速变为黄色,略有浑浊 |
| iii | 取 淀粉 淀粉 溶液 溶液 (用盐酸酸化至 (用盐酸酸化至 ),通入 ),通入 至过量 至过量 | 溶液迅速变为黄色,有浑浊 |
| iv | 将实验iii中的黄色浊液进行离心分离 | 试管壁上附着淡黄色固体,溶液为黄色 |
(1)对比实验i、ii、iii,说明反应速率与
(2)为了探究淡黄色固体的成分,甲同学进行实验:取实验iv试管壁上的淡黄色固体,发现其微溶于乙醇,易溶于
 ,淡黄色固体是
,淡黄色固体是(3)根据上述实验现象,甲同学猜测一定有单质碘生成,猜测的理论依据是
(4)利用如图装置继续实验,证实了单质碘可以生成。实验现象是

(5)对于实验i、ii、iii未能检测到单质碘,甲同学继续实验
| 实验 | 实验操作 | 实验现象 |
| v | 将 通入蓝色的碘淀粉混合溶液中 通入蓝色的碘淀粉混合溶液中 | 溶液蓝色迅速褪去 |
| vi | 取实验iv离心后的黄色溶液少量,加入盐酸酸化的 溶液 溶液 | 生成白色沉淀 |
(6)根据上述一系列实验,乙同学大胆猜测,整个反应中
 起到了催化剂作用,为了证明乙同学的猜想正确,还需要的实验证据是
起到了催化剂作用,为了证明乙同学的猜想正确,还需要的实验证据是实验结果证实了猜想,则总反应的化学方程式是
您最近半年使用:0次
2 . 中科院科学家设计出一套利用SO2和太阳能综合制氢方案,其基本工作原理如图所示,下列说法错误的是
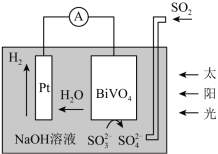

| A.该装置实现了太阳能转化为化学能 |
| B.Pt电极作正极,发生还原反应 |
| C.电子流向:Pt电极→外电路→BiVO4电极 |
D.BiVO4电极上的反应为SO -2e-+2OH-=SO -2e-+2OH-=SO +H2O +H2O |
您最近半年使用:0次
名校
解题方法
3 . Ⅰ.铁黄是一种重要的化工产品。由生产钛白粉废渣制备铁黄的过程如下。

资料:
i.钛白粉废渣成分:主要为FeSO4·H2O,含少量TiOSO4和不溶物
ii.TiOSO4+(x+1)H2O TiO2·xH2O↓+H2SO4
TiO2·xH2O↓+H2SO4
iii.0.1mol·L−1Fe2+生成Fe(OH)2,开始沉淀时pH=6.3,完全沉淀时pH=8.3
0.1mol·L−1Fe3+生成FeOOH,开始沉淀时pH=1.5,完全沉淀时pH=2.8
(一)纯化:加入过量铁粉,充分反应后,分离混合物
(二)制备晶种
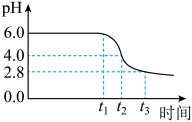
为制备高品质铁黄产品,需先制备少量铁黄晶种。过程及现象是:向一定浓度FeSO4溶液中加入氨水,产生白色沉淀,并很快变成灰绿色。滴加氨水至pH为6.0时开始通空气并记录pH变化(如下图)。
(1)①产生白色沉淀的离子方程式是___________ 。
②产生白色沉淀后的pH低于资料iii中的6.3.原因是:沉淀生成后c(Fe2+)___________ 0.1mol·L−1(填“>”“=”或“<”)。
③0-t1时段,pH几乎不变;t1-t2时段,pH明显降低。结合方程式解释原因:___________ 。
④pH≈4时制得铁黄晶种。若继续通入空气,t3后pH几乎不变,此时溶液中c(Fe2+)仍降低,但c(Fe3+)增加,且c(Fe2+)降低量大于c(Fe3+)增加量。结合总方程式说明原因:___________ 。
Ⅱ.某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
(2)浓盐酸与MnO2混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和MnO2
①电极反应式:
i.还原反应:MnO2+2e-+4H+=Mn2++2H2O
ii.氧化反应:___________ 。
②根据电极反应式,分析A中仍存在盐酸和MnO2的原因。
i.随c(H+)降低或c(Mn2+)浓度升高,MnO2氧化性减弱。
ii.随c(Cl-)降低,___________ 。
③补充实验证实了②中的分析。
a是___________ ,b是___________ 。
(3)利用c(H+)对MnO2氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与MnO2反应所需的最低c(H+)由大到小的顺序是___________ ,从原子结构角度说明理由___________ 。
(4)根据(2)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将Mn2+氧化为MnO2。经实验证实了推测,该化合物是___________ 。
(5)Ag分别与1mol·L−1的盐酸、氢溴酸和氢碘酸混合,Ag只与氢碘酸发生置换反应,试解释原因:___________ 。
(6)总结:物质氧化性和还原性变化的一般规律是___________ 。

资料:
i.钛白粉废渣成分:主要为FeSO4·H2O,含少量TiOSO4和不溶物
ii.TiOSO4+(x+1)H2O
 TiO2·xH2O↓+H2SO4
TiO2·xH2O↓+H2SO4iii.0.1mol·L−1Fe2+生成Fe(OH)2,开始沉淀时pH=6.3,完全沉淀时pH=8.3
0.1mol·L−1Fe3+生成FeOOH,开始沉淀时pH=1.5,完全沉淀时pH=2.8
(一)纯化:加入过量铁粉,充分反应后,分离混合物
(二)制备晶种
为制备高品质铁黄产品,需先制备少量铁黄晶种。过程及现象是:向一定浓度FeSO4溶液中加入氨水,产生白色沉淀,并很快变成灰绿色。滴加氨水至pH为6.0时开始通空气并记录pH变化(如下图)。

(1)①产生白色沉淀的离子方程式是
②产生白色沉淀后的pH低于资料iii中的6.3.原因是:沉淀生成后c(Fe2+)
③0-t1时段,pH几乎不变;t1-t2时段,pH明显降低。结合方程式解释原因:
④pH≈4时制得铁黄晶种。若继续通入空气,t3后pH几乎不变,此时溶液中c(Fe2+)仍降低,但c(Fe3+)增加,且c(Fe2+)降低量大于c(Fe3+)增加量。结合总方程式说明原因:
Ⅱ.某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
(2)浓盐酸与MnO2混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和MnO2
①电极反应式:
i.还原反应:MnO2+2e-+4H+=Mn2++2H2O
ii.氧化反应:
②根据电极反应式,分析A中仍存在盐酸和MnO2的原因。
i.随c(H+)降低或c(Mn2+)浓度升高,MnO2氧化性减弱。
ii.随c(Cl-)降低,
③补充实验证实了②中的分析。
| 实验操作 | 试剂 | 产物 | |
| I |  | 较浓H2SO4 | 有氯气 |
| Ⅱ | a | 有氯气 | |
| Ⅲ | a+b | 无氯气 |
(3)利用c(H+)对MnO2氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与MnO2反应所需的最低c(H+)由大到小的顺序是
(4)根据(2)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将Mn2+氧化为MnO2。经实验证实了推测,该化合物是
(5)Ag分别与1mol·L−1的盐酸、氢溴酸和氢碘酸混合,Ag只与氢碘酸发生置换反应,试解释原因:
(6)总结:物质氧化性和还原性变化的一般规律是
您最近半年使用:0次
名校
解题方法
4 . 微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法正确的是


| A.该装置是原电池,b极是负极 |
| B.该电池工作时,应选用质子交换膜 |
| C.该电池工作时,电子从a经电流表A流向b,离子从右经交换膜向左迁移 |
| D.电极a反应:(C6H10O5)n-24e-+7H2O=6CO2↑+24H+ |
您最近半年使用:0次
2023-10-27更新
|
1704次组卷
|
8卷引用:广西部分高中2024届高三第一次摸底测试化学试题
广西部分高中2024届高三第一次摸底测试化学试题广西南宁市2024届高三上学期毕业班摸底测试化学试题(已下线)寒假作业08 原电池-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)(已下线)热点14 电化学及其应用安徽省淮北市第一中学2023-2024学年高二下学期寒假自主学习质量评估化学试题(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)西藏自治区拉萨市第三高级中学2023-2024学年高三上学期第三次月考理综试题
名校
5 . 用吸附了氢气的纳米碳管等材料制作的二次电池原理如图所示,下列说法正确的是
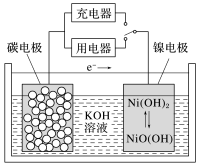

| A.充电时,阴极的电极反应为Ni(OH)2+OH-−e-=NiO(OH)+H2O |
| B.充电时,将电池的碳电极与外电源的正极相连 |
| C.放电时,OH-移向镍电极 |
| D.放电时,负极的电极反应为H2-2e-+2OH-=2H2O |
您最近半年使用:0次
名校
解题方法
6 . 某实验小组学生为探究氧化性: Br2 > Fe3+ > I2,设计下列实验方案。
【查阅资料】电极电势如下表:(已知:电极电势越高,氧化性越强)
(1)FeCl3溶液的配制:取FeCl3固体溶于___________ ,再稀释至指定浓度。配制250mL 0.1mol/L FeCl3溶液,需5.0 mol/L FeCl3溶液的体积为___________ mL,配制过程,图中不需要使用的仪器有___________ (填仪器名称)。

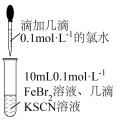
(2)利用FeBr2和氯水,设计实验证明氧化性:Br2 > Fe3+,实验如图所示,实验过程中,能证明氧化性:Br2 > Fe3+的现象是___________ 。
(3)利用0.1mol/L的FeCl3溶液和0.1mol/L的 溶液,不用任何试剂证明氧化性:Fe3+ > I2,FeCl3溶液和碘水颜色相近,设计的实验装置如图,实验过程中,电流计指针偏转,说明反应发生。
溶液,不用任何试剂证明氧化性:Fe3+ > I2,FeCl3溶液和碘水颜色相近,设计的实验装置如图,实验过程中,电流计指针偏转,说明反应发生。
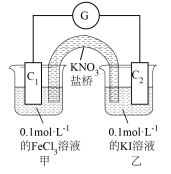
①通过外电路中电子流向:___________ (用C1、C2和→表示),可证明氧化性: 。
。
②也可通过甲池中颜色变化证明,甲池中颜色变化为___________ 。
(4)化学能可转化为电能,写出其在生活中常见的一种应用___________ 。
【查阅资料】电极电势如下表:(已知:电极电势越高,氧化性越强)
| 氧化还原电对(氧化型/还原型) | 电极反应式(氧化型+ne-=还原型) | 电极电势(E0/V) |
| Fe3+ +/ Fe2 | Fe3+ + e- = Fe2+ | 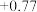 |
| I2 /I- | I2 + 2e- = 2I- | 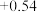 |
| Br2 /Br- | Br2 + 2e- = 2 Br- | 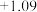 |

(2)利用FeBr2和氯水,设计实验证明氧化性:Br2 > Fe3+,实验如图所示,实验过程中,能证明氧化性:Br2 > Fe3+的现象是

(3)利用0.1mol/L的FeCl3溶液和0.1mol/L的
 溶液,不用任何试剂证明氧化性:Fe3+ > I2,FeCl3溶液和碘水颜色相近,设计的实验装置如图,实验过程中,电流计指针偏转,说明反应发生。
溶液,不用任何试剂证明氧化性:Fe3+ > I2,FeCl3溶液和碘水颜色相近,设计的实验装置如图,实验过程中,电流计指针偏转,说明反应发生。
①通过外电路中电子流向:
 。
。②也可通过甲池中颜色变化证明,甲池中颜色变化为
(4)化学能可转化为电能,写出其在生活中常见的一种应用
您最近半年使用:0次
解题方法
7 . 硅锰电池是一种新型电池,其工作原理如图所示。下列说法错误的是
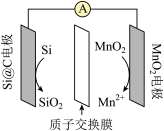

A.电池充电时, 电极连接外接电源的正极 电极连接外接电源的正极 |
B.电池工作时, 通过质子交换膜由Si@C电极区移向 通过质子交换膜由Si@C电极区移向 电极区 电极区 |
C.电池充电时,Si@C电极的电极反应式是 |
| D.放电时,导线上每通过0.2mol电子,正极区溶液的质量增加8.7g |
您最近半年使用:0次
2023-10-25更新
|
138次组卷
|
2卷引用:辽宁省名校联盟2023-2024学年高三10月联考化学试题
解题方法
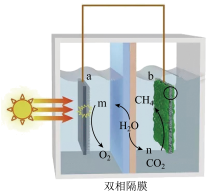
8 . 一种微生物—光电化学复合系统可高效实现固定 并生成
并生成 ,其原理如图所示,双极隔膜可向两极室分别提供
,其原理如图所示,双极隔膜可向两极室分别提供 和
和 。下列有关说法不正确的是
。下列有关说法不正确的是
 并生成
并生成 ,其原理如图所示,双极隔膜可向两极室分别提供
,其原理如图所示,双极隔膜可向两极室分别提供 和
和 。下列有关说法不正确的是
。下列有关说法不正确的是
| A.a电极为负极,发生氧化反应 |
B.m为 ,n为 ,n为 |
C.b电极的电极反应式: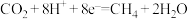 |
D.b极每生成1.6g  ,装置中共消耗10.8g ,装置中共消耗10.8g  |
您最近半年使用:0次
名校
9 . 中国明确提出2030年“碳达峰”与2060年“碳中和”目标。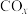 选择性甲烷化是有望实现“双碳目标”具有良好应用前景的处理方法。富氢气氛下,
选择性甲烷化是有望实现“双碳目标”具有良好应用前景的处理方法。富氢气氛下, 、
、 均可与
均可与 发生甲烷化反应:
发生甲烷化反应:
Ⅰ.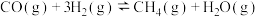
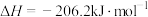
Ⅱ.

回答下列问题:
(1)已知
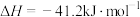 ,则
,则
_______ 。
(2)请从平衡移动的角度,提出三种可行的操作提高反应Ⅰ中 的转化率
的转化率_______ 、_______ 、_______ 。
(3)400℃时,选用镍基催化剂,向 密闭容器中通入
密闭容器中通入 、
、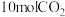 和
和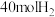 进行反应,平衡后测得
进行反应,平衡后测得 ,
,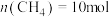 。
。
① 的平衡转化率为
的平衡转化率为_______ 。
②反应Ⅱ平衡常数K的数值最接近下列哪个数值_______ (填字母)。
A.20 B.2 C.0.2 D.0.02
(4)其他条件相同,反应Ⅱ使用两种不同催化剂,反应相同的时间,测得 的转化率随温度变化的影响如图所示。
的转化率随温度变化的影响如图所示。
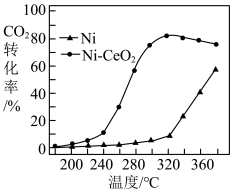
①请解释使用 催化剂时,随着温度的升高,为何
催化剂时,随着温度的升高,为何 转化率先升高后降低
转化率先升高后降低_____ ?
②根据图像分析,下列说法错误的是_______ (填字母)。
A.在200~360℃范围内, 的催化效果比
的催化效果比 更好
更好
B.可以通过改变催化剂种类的方式调控 平衡转化率
平衡转化率
C.在240℃附近,可以通过延长反应时间的方式提高 的转化率
的转化率
(5) 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示:
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示:
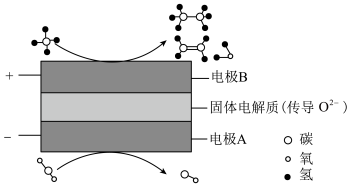
①阴极上的反应式为_______ 。
②阳极上生成乙烯 和乙烷
和乙烷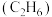 的反应式分别为
的反应式分别为_______ 和_______ 。
③若生成的乙烯 和乙烷
和乙烷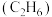 的体积比为
的体积比为 ,则消耗的
,则消耗的 和
和 的体积比为
的体积比为_______ 。
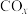 选择性甲烷化是有望实现“双碳目标”具有良好应用前景的处理方法。富氢气氛下,
选择性甲烷化是有望实现“双碳目标”具有良好应用前景的处理方法。富氢气氛下, 、
、 均可与
均可与 发生甲烷化反应:
发生甲烷化反应:Ⅰ.
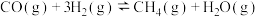
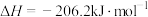
Ⅱ.


回答下列问题:
(1)已知

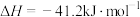 ,则
,则
(2)请从平衡移动的角度,提出三种可行的操作提高反应Ⅰ中
 的转化率
的转化率(3)400℃时,选用镍基催化剂,向
 密闭容器中通入
密闭容器中通入 、
、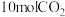 和
和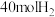 进行反应,平衡后测得
进行反应,平衡后测得 ,
,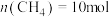 。
。①
 的平衡转化率为
的平衡转化率为②反应Ⅱ平衡常数K的数值最接近下列哪个数值
A.20 B.2 C.0.2 D.0.02
(4)其他条件相同,反应Ⅱ使用两种不同催化剂,反应相同的时间,测得
 的转化率随温度变化的影响如图所示。
的转化率随温度变化的影响如图所示。
①请解释使用
 催化剂时,随着温度的升高,为何
催化剂时,随着温度的升高,为何 转化率先升高后降低
转化率先升高后降低②根据图像分析,下列说法错误的是
A.在200~360℃范围内,
 的催化效果比
的催化效果比 更好
更好B.可以通过改变催化剂种类的方式调控
 平衡转化率
平衡转化率C.在240℃附近,可以通过延长反应时间的方式提高
 的转化率
的转化率(5)
 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示:
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示:
①阴极上的反应式为
②阳极上生成乙烯
 和乙烷
和乙烷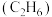 的反应式分别为
的反应式分别为③若生成的乙烯
 和乙烷
和乙烷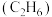 的体积比为
的体积比为 ,则消耗的
,则消耗的 和
和 的体积比为
的体积比为
您最近半年使用:0次
名校
解题方法
10 . 科研人员最近发明了一种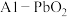 电池,通过X和Y两种离子交换膜将电解质溶液隔开,形成M、R、N三个电解质溶液区域,电解质分别为
电池,通过X和Y两种离子交换膜将电解质溶液隔开,形成M、R、N三个电解质溶液区域,电解质分别为 、
、 、
、 ,结构示意图如上(已知a>b)。该电池放电时,下列说法错误的是
,结构示意图如上(已知a>b)。该电池放电时,下列说法错误的是
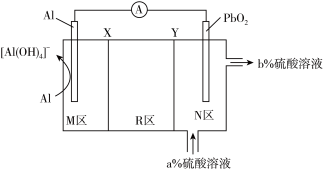
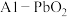 电池,通过X和Y两种离子交换膜将电解质溶液隔开,形成M、R、N三个电解质溶液区域,电解质分别为
电池,通过X和Y两种离子交换膜将电解质溶液隔开,形成M、R、N三个电解质溶液区域,电解质分别为 、
、 、
、 ,结构示意图如上(已知a>b)。该电池放电时,下列说法错误的是
,结构示意图如上(已知a>b)。该电池放电时,下列说法错误的是
A. 通过X移向M区 通过X移向M区 |
| B.R区电解质溶液浓度逐渐增大 |
C.N区电极反应为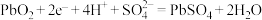 |
| D.每消耗1.8gAl,N区电解质溶液减少16g |
您最近半年使用:0次



