名校
解题方法
1 . 已知 A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素。E是第四周期的p区元素且最外层只有2对成对电子,F元素的基态原子第四能层只有一个电子,其它能层均已充满电子。
(1)基态E原子的价电子排布图_______________ 。
(2)B、C、D三元素第一电离能由大到小的顺序为________ (用元素符号表示)。
(3)BD 中心原子杂化轨道的类型为
中心原子杂化轨道的类型为________ 杂化;CA 的空间构型为
的空间构型为__________ (用文字描述)。
(4)1mol BC-中含有π键的数目为______ NA。
(5)D、E元素最简单氢化物的稳定性______ >______ (填化学式),理由是____ 。
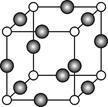
(6)C、F两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是_____ ,C原子的配位数是_____ 。若相邻C原子和F原子间的距离为a cm,阿伏加德罗常数为NA,则该晶体的密度为______ g/cm3(用含a、NA的符号表示)。
(1)基态E原子的价电子排布图
(2)B、C、D三元素第一电离能由大到小的顺序为
(3)BD
 中心原子杂化轨道的类型为
中心原子杂化轨道的类型为 的空间构型为
的空间构型为(4)1mol BC-中含有π键的数目为
(5)D、E元素最简单氢化物的稳定性
(6)C、F两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是

您最近一年使用:0次
2019-01-30更新
|
240次组卷
|
5卷引用:云南省民族中学2017届高三适应性考试(六)理综化学试题
2 . 现有原子序数小于20的A,B,C,D,E,F6种元素,它们的原子序数依次增大,已知B元素是地壳中含量最多的元素;A和C的价电子数相同,B和D的价电子数也相同,且A和C两元素原子核外电子数之和是B,D两元素原子核内质子数之和的1/2;C,D,E三种元素的基态原子具有相同的电子层数,且E原子的p轨道上电子数比D原子的p轨道上多一个电子;6种元素的基态原子中,F原子的电子层数最多且和A处于同一主族。回答下列问题。
(1)用电子式表示C和E形成化合物的过程________________ 。
(2)写出基态F原子核外电子排布式__________________ 。
(3)写出A2D的电子式________ ,其分子中________ (填“含”或“不含”)σ键,________ (填“含”或“不含”)π键。
(4)A,B,C共同形成的化合物化学式为________ ,其中化学键的类型有________ 。
(1)用电子式表示C和E形成化合物的过程
(2)写出基态F原子核外电子排布式
(3)写出A2D的电子式
(4)A,B,C共同形成的化合物化学式为
您最近一年使用:0次
2018-12-13更新
|
187次组卷
|
3卷引用:云南省昭通市彝良县第一中学2018-2019学年高二上学期12月考试化学试题
名校
解题方法
3 . 今有A、B、C、D四种元素,已知A元素是地壳中含量最多的元素;B元素为金属元素,它的原子核外K、L层上电子数之和等于M、N层电子数之和;C元素是第三周期第一电离能最小的元素;D元素在第三周期中电负性最大。
(1)试推断A、B、C、D四种元素的符号:A________ 、B________ 、C________ 、D________ 。
(2)写出A元素原子的核外电子排布式:____________ ;写出B元素原子核外电子排布的价电子构型:__________ ;用电子排布图表示C原子的核外电子排布情况:_______________ 。
(3)比较四种元素的第一电离能和电负性的大小:第一电离能____________ ;电负性____________ 。
(1)试推断A、B、C、D四种元素的符号:A
(2)写出A元素原子的核外电子排布式:
(3)比较四种元素的第一电离能和电负性的大小:第一电离能
您最近一年使用:0次
2018-12-04更新
|
495次组卷
|
10卷引用:云南省澄江二中2018-2019学年高二上学期期中考试化学试题
云南省澄江二中2018-2019学年高二上学期期中考试化学试题云南省盐津县第二中学2018-2019学年高二上学期12月份考试化学试题云南省玉溪市新平三中2019-2020学年高二上学期12月份月考化学试题云南省凤庆县第一中学2019-2020学年高二12月月考化学试题四川省凉山木里中学2017-2018学年高二上学期期中考试化学试卷新疆兵团八师一四三团一中2018-2019学年高二下学期期中考试化学试题鲁科版2019选择性必修2第1章 原子结构与元素性质 第1章学科素养提升(人教版2019)选择性必修2第一章 原子结构与性质 学科素养提升湖南省长沙市明达中学2021-2022学年高二上学期期末考试化学试题海南省儋州川绵中学2021-2022学年高二下学期第一次月考化学试题
4 . 氨硼烷是一种有效、安全的固体储氢材料.氨硼烷的结构和乙烷相似,如图.
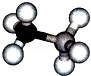
(1)氨硼烷的晶体类型为__ .
(2)氮和硼比较,电负性大的元素为__ (填元素符号).
(3)氨硼烷分子中氮原子、硼原子的杂化轨道类型分别为__ 和__ .
(4)氨硼烷__ (填“能”或“不能”)溶于水,其原因是__ .
(5)以NaBH4为硼源、某配合物为氨源可用于制备氨硼烷.为测定该配合物的结构,取2.32g配合物进行如下实验:用重量法分析金属元素,测得镍元素的质量为0.59g;在碱性条件下加热蒸出NH3,用滴定法测出其物质的量为0.06mol;滴加过量硝酸银溶液,有白色沉淀生成,加热,沉淀没有增加;用摩尔法分析含量,测得氯元素质量为0.71g.
该配合物中镍离子的基态电子排布式为__ .该配合物的化学式为 。

(1)氨硼烷的晶体类型为
(2)氮和硼比较,电负性大的元素为
(3)氨硼烷分子中氮原子、硼原子的杂化轨道类型分别为
(4)氨硼烷
(5)以NaBH4为硼源、某配合物为氨源可用于制备氨硼烷.为测定该配合物的结构,取2.32g配合物进行如下实验:用重量法分析金属元素,测得镍元素的质量为0.59g;在碱性条件下加热蒸出NH3,用滴定法测出其物质的量为0.06mol;滴加过量硝酸银溶液,有白色沉淀生成,加热,沉淀没有增加;用摩尔法分析含量,测得氯元素质量为0.71g.
该配合物中镍离子的基态电子排布式为
您最近一年使用:0次
2018-11-27更新
|
240次组卷
|
2卷引用:云南省泸水五中2018-2019学年高二上学期期中考试化学试题
5 . 氧是地壳中含量最多的元素。
(1)氧元素基态原子核外未成对电子数为________ 个。
(2)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为________ 。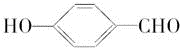 的沸点比
的沸点比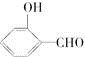 高,原因是
高,原因是__________________________ 。
(3)H+可与H2O形成H3O+,H3O+中O原子采用________ 杂化。H3O+中H—O—H键角比H2O中H—O—H键角大,原因为_____________________________________ 。
(1)氧元素基态原子核外未成对电子数为
(2)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为
 的沸点比
的沸点比 高,原因是
高,原因是(3)H+可与H2O形成H3O+,H3O+中O原子采用
您最近一年使用:0次
名校
6 . 已知A、B、C、D、E、F是周期表前四周期的元素,原子序数依次增大。A的基态原子2p能级上有2个单电子;C是地壳中含量最多的元素;E的单质常温常压下为黄绿色气体,化学性质十分活泼,具有毒性;F位于ds区,最外能层有单电子,是热和电最佳导体之一;D与F不同周期,但最外能层电子数相等。
(1)写出基态C原子的电子排布式:____________ 。
(2)A、B、C三种元素第一电离能最大的是____________ 。(用元素符号表示),其原因是____________ 。
(3)B、C两元素形成的化合物B2C的分子空间构型为____________ 。与B2C互为等电子体的粒子的化学式为____________ 。(填一种)。
(4)D、E形成的一种离子化合物,在晶胞结构图中黑球表示E的位置,白球表示D的位置,已知该晶胞的边长为ncm,阿伏伽德罗常数为NA,求晶胞的密度ρ=_______ g/cm3(用含n、NA的计算式表示)。
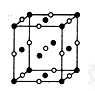
(5)由F原子形成的晶胞结构如图,F原子的半径为r,列式表示F原子在晶胞中的空间利用率:__________________ (不要求计算结果)。

(1)写出基态C原子的电子排布式:
(2)A、B、C三种元素第一电离能最大的是
(3)B、C两元素形成的化合物B2C的分子空间构型为
(4)D、E形成的一种离子化合物,在晶胞结构图中黑球表示E的位置,白球表示D的位置,已知该晶胞的边长为ncm,阿伏伽德罗常数为NA,求晶胞的密度ρ=

(5)由F原子形成的晶胞结构如图,F原子的半径为r,列式表示F原子在晶胞中的空间利用率:

您最近一年使用:0次
2016高二·全国·课时练习
7 . 已知A,B,C,D、E都是周期表中前四周期的元素,且原子序数依次增大,其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题(答题时,A,B,C,D,E用所对应的元素符号表示):
(1)比E核外电子数少5的元素的原子核外电子排布式是_________ ,A,B,C,D的第一电离能由小到大的顺序为_______ 。
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是________________ 。

(3)A的氢化物属于______ (填“极性”或“非极性”)分子,D的低价氧化物分子的空间构型是_______ 。
(4)A,E形成的某种化合物的晶胞结构如图所示,则其化学式为______ (每个球均表示1个原子)。
(1)比E核外电子数少5的元素的原子核外电子排布式是
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是

(3)A的氢化物属于
(4)A,E形成的某种化合物的晶胞结构如图所示,则其化学式为
您最近一年使用:0次
2017-01-18更新
|
215次组卷
|
4卷引用:云南省武定县第一中学2018-2019学年高二上学期12月份考试化学试题
名校
8 . 有四种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)A原子的核外电子排布式:____________________________________________________ 。
(2)B元素在周期表中的位置:______________________________________________________ ;
离子半径:B________ (填“大于”或“小于”)A。
(3)C原子的电子排布图是_________ ,其原子核外有____ 个未成对电子,能量最高的电子为____ 轨道上的电子,其轨道呈______ 形。
(4)D-的结构示意图是________ 。
(5)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为___________ 。与D的氢化物的水化物反应的化学方程式为__________________ 。
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生成过程中常用的消毒杀菌剂 |
请根据表中信息填写:
(1)A原子的核外电子排布式:
(2)B元素在周期表中的位置:
离子半径:B
(3)C原子的电子排布图是
(4)D-的结构示意图是
(5)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为
您最近一年使用:0次
2016-12-09更新
|
129次组卷
|
5卷引用:云南省双柏县第一中学2018-2019学年高二上学期期中考试化学试题
11-12高二上·福建厦门·期中
名校
9 . A、B、C、D四种元素,已知A元素是地壳中含量最多的元素;B元素为金属元素,它的原子核外K、L层上电子数之和等于M、N层电子数之和;C元素是第三周期第一电离能最小的元素;D元素在第三周期中第一电离能最大。下列有关叙述错误的是
| A.四种元素A、B、C、D分别为O、Ca、Na、Ar |
| B.元素A、B、C两两组成的化合物可为CaO、CaO2、Na2O、Na2O2等 |
| C.元素A、C简单离子的半径大小关系为A<C |
| D.元素B、C电负性大小关系为B>C |
您最近一年使用:0次
2016-12-09更新
|
520次组卷
|
12卷引用:云南省玉溪市易门中学2017-2018学年高二上学期期中考试化学试题
云南省玉溪市易门中学2017-2018学年高二上学期期中考试化学试题云南省凤庆县第一中学2019-2020学年高二12月月考化学试题云南省玉溪市易门县一中2021-2022学年高二下学期3月月考化学试题(已下线)2011-2012学年福建省厦门一中高二上学期期中考试化学试卷(已下线)2013-2014学年福建省厦门一中高二上学期期中考试化学试卷2016-2017学年宁夏银川市第二中学高二下学期第一次月考化学试卷河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1(已下线)专题11.1 原子结构与性质(练)-《2020年高考一轮复习讲练测》(已下线)第35讲 原子结构与性质(精练)-2021年高考化学一轮复习讲练测甘肃省静宁县第一中学2020-2021学年高二上学期期末考试化学(实验班)试题(已下线)模块同步卷02 原子结构与元素的性质-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)吉林省长春市实验中学2020-2021学年度高二下学期阶段考试化学试题
10 . 【化学选修3:物质结构与性质】A、B、C、D、E五种元素的原子序数依次增大,其中非金属元素A的基态原子中成对电子数是未成时电子数的两倍,C元素在地壳中含量最高,D的单质是短周期中熔点最低的金属,E的合金是我国使用最早的合金。
(1)E元素的基态原子电子排布式为__________________ 。
(2)A的某种氢化物A2H2分子中含有___ 个σ键和____ 个π键。
(3)A 的含氧酸根离子AO3n-的空间构型是___________ 。
(4)B的最简单的氢化物的沸点比A 的最简单的氢化物的沸点高得多,其原因是_____ 。
(5)E的最高价氧化物对应的水化物溶解于氨水中生成的复杂化合物的化学式是______ 。
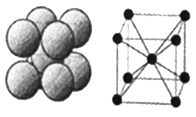
(6)下图是D单质的晶体堆积方式,这种堆积方式的晶胞中原子的配位数为____ ,若该原子的半径为rpm ,此晶体的密度ρ=______ g/cm3(用含r的代数式表示,阿伏伽德罗常数用NA表示)。
(1)E元素的基态原子电子排布式为
(2)A的某种氢化物A2H2分子中含有
(3)A 的含氧酸根离子AO3n-的空间构型是
(4)B的最简单的氢化物的沸点比A 的最简单的氢化物的沸点高得多,其原因是
(5)E的最高价氧化物对应的水化物溶解于氨水中生成的复杂化合物的化学式是
(6)下图是D单质的晶体堆积方式,这种堆积方式的晶胞中原子的配位数为

您最近一年使用:0次
2017-02-24更新
|
855次组卷
|
4卷引用:云南省红河州弥勒市中小学2018-2019学年高二下学期期末考试化学试题



