名校
解题方法
1 . 硼氢化钠(NaBH4)具有很强的还原性,被称为“万能还原剂”,NaBH4在催化剂钌(44Ru)表面与水反应的历程如图所示:
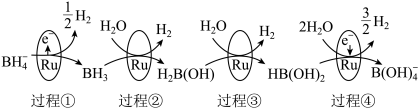
| A.元素钌(44Ru)位于d区 |
| B.BH3分子的空间结构和VSEPR模型不同 |
| C.过程④中产生1molH2,转移电子物质的量为2mol |
| D.硼氢化钠中硼元素的化合价为+3价,反应过程中硼元素的化合价始终保持不变 |
您最近一年使用:0次
2023-03-16更新
|
342次组卷
|
3卷引用:山东省德州市第一中学2022-2023学年高二下学期3月月考化学试题
2 . X、Y、Z、W是同周期主族元素,四种元素均是短周期元素,W元素形成的某种单质具有强氧化性,可用于杀菌消毒。四种元素与锂组成的盐是一种新型锂离子电池的电解质,结构如图所示,下列说法正确的是
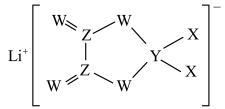

| A.组成这种新型电解质的所有元素均处于元素周期表p区 |
| B.Z元素的含氧酸不可能使酸性高锰酸钾溶液褪色 |
| C.最简单氢化物的沸点: X>W |
| D.同周期中第一电离能比W元素小的有4种元素 |
您最近一年使用:0次
名校
解题方法
3 . 短周期主族元素X、Y、Z、W在周期表中位置如图,下列表述正确的是
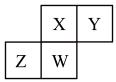

| A.Y最高正价可能为+6价 |
| B.W有可能周期数等于其族序数 |
| C.Z的最高价氧化物有可能与Y的最高价氧化物对应的水化物反应 |
| D.若X为氧元素,则离子半径顺序:r(W2-)>r(Y-)>r(X2-)>r(Z3-) |
您最近一年使用:0次
2023-02-16更新
|
791次组卷
|
2卷引用:广东省深圳市高级中学2022-2023学年高一上学期期末考试化学试题
2023高三·全国·专题练习
解题方法
4 . 元素周期表中的数量应用
(1)甲、乙是元素周期表中同一周期的第ⅡA族和第ⅦA族元素,原子序数分别为m、n,则m、n的关系为_______ 。
(2)甲、乙是元素周期表中同一主族相邻周期的两种元素(其中甲在上一周期),若甲的原子序数为x,则乙的原子序数可能是_______ 。
(3)若A、B是相邻周期同主族元素(A在B的上一周期),A、B所在周期分别有m种和n种元素,A的原子序数为x,B的原子序数为y,则x、y的关系为_______ 。
(4)下列各表为元素周期表中的一部分,表中数字为原子序数,其中M的原子序数为37的是_______。
(1)甲、乙是元素周期表中同一周期的第ⅡA族和第ⅦA族元素,原子序数分别为m、n,则m、n的关系为
(2)甲、乙是元素周期表中同一主族相邻周期的两种元素(其中甲在上一周期),若甲的原子序数为x,则乙的原子序数可能是
(3)若A、B是相邻周期同主族元素(A在B的上一周期),A、B所在周期分别有m种和n种元素,A的原子序数为x,B的原子序数为y,则x、y的关系为
(4)下列各表为元素周期表中的一部分,表中数字为原子序数,其中M的原子序数为37的是_______。
A. | B.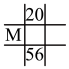 | C.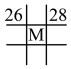 | D.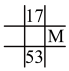 |
您最近一年使用:0次
名校
5 . 几种主族元素在周期表中的位置如下:
根据上表回答下列问题:
(1)画出⑩的原子结构示意图:_______ 。
(2)④和⑨两种元素形成的化合物的电子式是_______ 。
(3)②、⑦、⑧三种元素离子半径由大到小的顺序是_______ (用离子符号表示)。
(4)由⑥、⑨组成的化合物分子中,⑥、⑨原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物和一种碱性气体,试写出该反应的化学方程式:_______ 。
(5)对于元素②与④,能说明②的金属性比④强的是_______(填标号)。
(6)由①、③、⑦组成的化合物中含有的化学键有_______ 。
(7)在含有①、④、⑤简单阳离子的 溶液中,逐滴滴加
溶液中,逐滴滴加 的
的 溶液到过量,生成沉淀的质量与加入的
溶液到过量,生成沉淀的质量与加入的 溶液的体积关系如图所示。由图中数据分析计算:
溶液的体积关系如图所示。由图中数据分析计算:
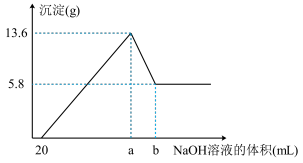
i.沉淀减少时发生的离子方程式:_______ 。
ii.a点的数值为_______  。
。
| 族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ② | ④ | ⑤ | ⑧ | ⑨ | |||
| 4 | ③ | ⑩ | ||||||
(1)画出⑩的原子结构示意图:
(2)④和⑨两种元素形成的化合物的电子式是
(3)②、⑦、⑧三种元素离子半径由大到小的顺序是
(4)由⑥、⑨组成的化合物分子中,⑥、⑨原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物和一种碱性气体,试写出该反应的化学方程式:
(5)对于元素②与④,能说明②的金属性比④强的是_______(填标号)。
A.②与 反应比④与 反应比④与 反应剧烈 反应剧烈 |
| B.②单质的熔、沸点比④的低 |
| C.②的最高价氧化物对应的水化物的碱性比④的最高价氧化物对应的水化物的碱性强 |
| D.与非金属单质反应时,②原子失电子数目比④原子失电子数目少 |
(7)在含有①、④、⑤简单阳离子的
 溶液中,逐滴滴加
溶液中,逐滴滴加 的
的 溶液到过量,生成沉淀的质量与加入的
溶液到过量,生成沉淀的质量与加入的 溶液的体积关系如图所示。由图中数据分析计算:
溶液的体积关系如图所示。由图中数据分析计算:
i.沉淀减少时发生的离子方程式:
ii.a点的数值为
 。
。
您最近一年使用:0次
名校
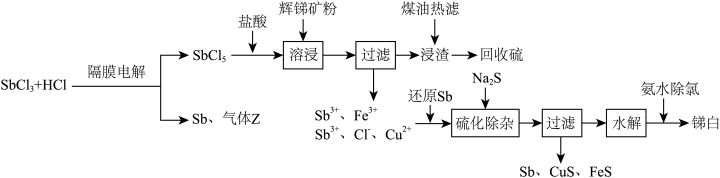
6 . 三氧化二锑,又称锑白,在工业上作阻燃剂、填充剂等,用途广泛。一种利用辉锑矿粉(含 及少量
及少量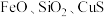 )制取锑白的工艺流程如图:
)制取锑白的工艺流程如图:
已知:①常温下,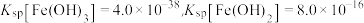 ,
, 。
。
②锑的常见价态为+3、+5价,其中 具有强氧化性,在溶液中能发生较剧烈的水解生成
具有强氧化性,在溶液中能发生较剧烈的水解生成 。
。
(1)锑元素的原子序数为51,位于元素周期表第___________ 周期第___________ 族。
(2)溶浸时发生的主要反应的离子方程式为___________ 。
(3)加入还原Sb还原高价金属离子,能够提高产物锑白的纯度,原因是___________ 。
(4) 水解会生成多种物质,较为稳定的是SbOCl,写出SbOCl在稀氨水中最终生成锑白的化学方程式:
水解会生成多种物质,较为稳定的是SbOCl,写出SbOCl在稀氨水中最终生成锑白的化学方程式:___________ ,锑白洗涤后便可干燥保存,检验洗净的试剂为___________ 。
(5)隔膜电解时,气体Z的分子式为___________ ;为平衡两极电荷,应使用___________ 交换膜(填“阴离子”“阳离子”或“质子”),理由是___________ 。
 及少量
及少量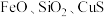 )制取锑白的工艺流程如图:
)制取锑白的工艺流程如图:
已知:①常温下,
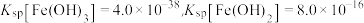 ,
, 。
。②锑的常见价态为+3、+5价,其中
 具有强氧化性,在溶液中能发生较剧烈的水解生成
具有强氧化性,在溶液中能发生较剧烈的水解生成 。
。(1)锑元素的原子序数为51,位于元素周期表第
(2)溶浸时发生的主要反应的离子方程式为
(3)加入还原Sb还原高价金属离子,能够提高产物锑白的纯度,原因是
(4)
 水解会生成多种物质,较为稳定的是SbOCl,写出SbOCl在稀氨水中最终生成锑白的化学方程式:
水解会生成多种物质,较为稳定的是SbOCl,写出SbOCl在稀氨水中最终生成锑白的化学方程式:(5)隔膜电解时,气体Z的分子式为
您最近一年使用:0次
2023-02-03更新
|
423次组卷
|
2卷引用:江苏省扬州中学2022-2023学年高三下学期开学摸底考试化学试题
解题方法
7 . 下表列出了A~M 13种元素在周期表中的位置:
(1)这些元素中,金属性最强的元素是_______ (填元素符号,下同),非金属性最强的是_______ 。
(2)写出H元素的最高价氧化物与F元素最高价氧化物对应水化物反应的离子方程式_______ 。
(3)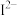 、
、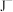 、
、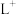 、
、 等微粒中,半径最大的是
等微粒中,半径最大的是_______ ,最小的是_______ 。
(4)A与D形成的化合物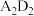 是
是_______ 化合物,其电子式为_______ 。
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I | J | K | ||
| 4 | L | M |
(2)写出H元素的最高价氧化物与F元素最高价氧化物对应水化物反应的离子方程式
(3)
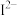 、
、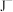 、
、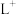 、
、 等微粒中,半径最大的是
等微粒中,半径最大的是(4)A与D形成的化合物
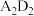 是
是
您最近一年使用:0次
名校
解题方法
8 . 近年来我国航天事业成果显著,其制造材料中包含了铝、镁、锌、钛、锰、铜、镍、铬、硅、氮、氧等多种元素。回答下列问题:
(1)铬元素属于周期表中_______ 区的元素,其基态原子核外电子空间运动状态有_______ 种,
(2)钛能形成多种配合物,如Ti(CO)6、[Ti(H2O)6]Cl3、[Ti(NH3)6]Cl3等。其配合物的配位数均为_______ ,其中配位原子的电负性由小到大的顺序是_______ (写元素符号),[Ti(NH3)6]Cl3中∠H-N-H_______ (填“大于”、“小于”或“等于”)单个氨气分子中∠H-N-H,原因是_______ 。
(3)Ni与Ca处于同一周期,且核外最外层电子构型相同,但金属Ni的熔点和沸点均比金属Ca的高,其原因为_______ 。
(4)已知锰的某种氧化物的晶胞如图所示,其中锰离子的化合价为_______ ,其配位数为_______ 。已知晶胞参数为a pm,设阿伏加德罗常数的值为NA,晶胞密度
_______  。(列出计算式即可)
。(列出计算式即可)

(1)铬元素属于周期表中
(2)钛能形成多种配合物,如Ti(CO)6、[Ti(H2O)6]Cl3、[Ti(NH3)6]Cl3等。其配合物的配位数均为
(3)Ni与Ca处于同一周期,且核外最外层电子构型相同,但金属Ni的熔点和沸点均比金属Ca的高,其原因为
(4)已知锰的某种氧化物的晶胞如图所示,其中锰离子的化合价为

 。(列出计算式即可)
。(列出计算式即可) 
您最近一年使用:0次
名校
解题方法
9 . 短周期元素W、X、Y、Z、Q,原子序数依次增大,W原子没有中子,X元素为地壳中含量最多的元素,Y、Z、Q同周期,且Y、Z、Q最外层电子数之和为14,Y与W同主族,下列结论不正确的是
| A.原子半径大小顺序为Y>Z>Q>X>W |
| B.W、X、Y形成的化合物中只有共价键 |
| C.X、Y可以形成的原子个数比1:1或1:2的化合物 |
| D.最高价氧化物对应的水化物酸性Z﹤Q |
您最近一年使用:0次
2023-01-12更新
|
1063次组卷
|
4卷引用:江苏省南京市第五高级中学2022-2023学年高一上学期学情自测卷化学试题
江苏省南京市第五高级中学2022-2023学年高一上学期学情自测卷化学试题 山东省青岛第五十八中学2022-2023学年高一下学期3月月考化学试题山东省青岛第十九中学2022-2023学年高一4月月考化学试题(已下线)专题09 原子结构 元素周期律和周期表-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(江苏专用)
10 . 随着新能源汽车销量的猛增,动力电池退役高峰将至,磷酸铁锂 是目前使用最多的动力电池材料,因此回收磷酸铁锂具有重要意义。一种从废旧磷酸铁锂正极片(
是目前使用最多的动力电池材料,因此回收磷酸铁锂具有重要意义。一种从废旧磷酸铁锂正极片( 、导电石墨、铝箔)中回收锂的工艺流程如下:
、导电石墨、铝箔)中回收锂的工艺流程如下:
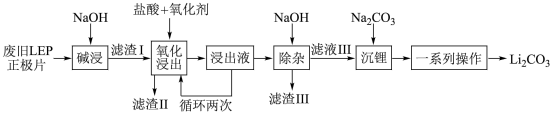
已知:i.废旧磷酸铁锂正极片中的化学物质均不溶于水也不与水反应。
ii. 在水中的溶解度随温度升高而降低,但煮沸时与水发生反应。
在水中的溶解度随温度升高而降低,但煮沸时与水发生反应。
回答下列问题:
(1) 中密度最小的金属元素在周期表中的位置是
中密度最小的金属元素在周期表中的位置是_______ 。
(2)“氧化浸出”时,保持其他条件不变,不同氧化剂对锂的浸出实验结果如下表,实际生产中氧化剂选用 ,不选用
,不选用 的原因是
的原因是_______ 。在“氧化浸出”时,适当的升温可加快反应速率,但一般不采取高温法,其原因是_______ 。 “氧化浸出”时生成了难溶的 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(3)“浸出液”循环两次的目的是_______ 。
(4)“滤渣II”经纯化可得 ,流程中生成的
,流程中生成的 、
、 在高温条件下与
在高温条件下与 煅烧可得
煅烧可得 ,实现再生利用,其化学方程式为
,实现再生利用,其化学方程式为_______ 。
(5)“一系列操作”具体包括_______ 、洗涤、干燥。
 是目前使用最多的动力电池材料,因此回收磷酸铁锂具有重要意义。一种从废旧磷酸铁锂正极片(
是目前使用最多的动力电池材料,因此回收磷酸铁锂具有重要意义。一种从废旧磷酸铁锂正极片( 、导电石墨、铝箔)中回收锂的工艺流程如下:
、导电石墨、铝箔)中回收锂的工艺流程如下:
已知:i.废旧磷酸铁锂正极片中的化学物质均不溶于水也不与水反应。
ii.
 在水中的溶解度随温度升高而降低,但煮沸时与水发生反应。
在水中的溶解度随温度升高而降低,但煮沸时与水发生反应。回答下列问题:
(1)
 中密度最小的金属元素在周期表中的位置是
中密度最小的金属元素在周期表中的位置是(2)“氧化浸出”时,保持其他条件不变,不同氧化剂对锂的浸出实验结果如下表,实际生产中氧化剂选用
 ,不选用
,不选用 的原因是
的原因是 ,该反应的化学方程式为
,该反应的化学方程式为| 序号 | 锂含量/% | 氧化剂 |  | 浸出液 浓度 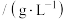 | 浸出渣中 含量/% |
| 1 | 3.7 |  | 3.5 | 9.02 | 0.10 |
| 2 | 3.7 |  | 3.5 | 9.05 | 0.08 |
| 3 | 3.7 |  | 3.5 | 7.05 | 0.93 |
| 4 | 3.7 |  | 3.5 | 8.24 | 0.43 |
(4)“滤渣II”经纯化可得
 ,流程中生成的
,流程中生成的 、
、 在高温条件下与
在高温条件下与 煅烧可得
煅烧可得 ,实现再生利用,其化学方程式为
,实现再生利用,其化学方程式为(5)“一系列操作”具体包括
您最近一年使用:0次



