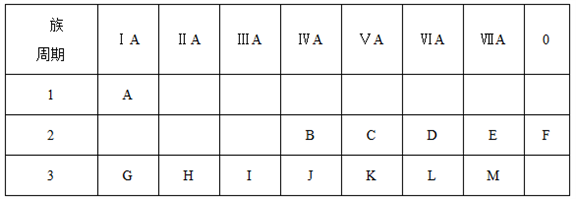
1 . 下表是元素周期表中的一部分,根据A~M在周期表中的位置,回答下列问题:
(1)表中元素,化学性质最不活泼的是_______ ,氧化性最强的单质是________ ,还原性最强的单质是____ 。(写元素符号或化学式)
(2)表中元素的最高价氧化物对应的水化物中,碱性最强的化合物的化学式为________ ,酸性最强的化合物的化学式为___________ ,呈两性的化合物的化学式为___________ 。
(3)A分别与B、C、D、E、J、K、L、M形成的化合物中最稳定的是_______ (写化学式)。
(4)写出D、G、L对应的离子半径由大到小的顺序________ (用离子符号表示)。
(1)表中元素,化学性质最不活泼的是
(2)表中元素的最高价氧化物对应的水化物中,碱性最强的化合物的化学式为
(3)A分别与B、C、D、E、J、K、L、M形成的化合物中最稳定的是
(4)写出D、G、L对应的离子半径由大到小的顺序
您最近一年使用:0次
12-13高一下·广东东莞·期中
名校
解题方法
2 . 下表是周期表中的一部分,根据A-I在周期表中的位置,第(1)~ (4)小题用元素符号或化学式回答,(5)~(8)小题按题目要求回答。
(1)表中元素,化学性质最不活泼的是_______ ,只有负价而无正价的是________ ,氧化性最强的单质是______ ,还原性最强的单质是________ 。
(2)最高价氧化物的水化物碱性最强的是___ ,酸性最强的是____ ,呈两性的是 _______ 。
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的______________ ,
(4)在B、C、E、F、G、H中,原子半径最大的是_________ ,
(5)A和D组成化合物的电子式_____________________ ,
(6)A和E组成化合物的化学式_____________________ ,
(7)用电子式表示B和H组成化合物的形成过程______________________________ ,
(8)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式___________________________________________ 。
| 族 周期 | I A | Ⅱ A | Ⅲ A | Ⅳ A | Ⅴ A | Ⅵ A | Ⅶ A | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(2)最高价氧化物的水化物碱性最强的是
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的
(4)在B、C、E、F、G、H中,原子半径最大的是
(5)A和D组成化合物的电子式
(6)A和E组成化合物的化学式
(7)用电子式表示B和H组成化合物的形成过程
(8)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式
您最近一年使用:0次
2016-12-09更新
|
1049次组卷
|
3卷引用:2012-2013学年广东省东莞市第七高级中学高一下学期期中考试化学试卷
(已下线)2012-2013学年广东省东莞市第七高级中学高一下学期期中考试化学试卷宁夏青铜峡市高级中学2017-2018学年高一下学期期中考试化学试题河北省石家庄市元氏县第四中学2019-2020学年高一下学期期中考试化学试题
名校
3 . 下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)元素①的原子结构示意图是______ 。
(2)从元素原子得失电子的角度看,元素⑤具有_______ (填“氧化性”或“还原性”)。
(3)元素②形成的单质气体含有_______ (填“极性”或“非极性”)共价键。
(4)元素③,⑨与H原子以原子个数比为1:1:1形成的化合物的电子式为______ 。
(5)第三周期中元素的最高价氧化物对应水化物中碱性最强的是_______ (填化学式,下同),最高价氧化物对应的水化物具有两性的物质是_______ ,这两种物质反应的离子方程式为_______ 。
(6)元素③,⑤,⑨形成简单离子的半径由大到小的顺序是______ (填离子符号)。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
二 | ① | ② | ③ | ④ | ||||
三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)从元素原子得失电子的角度看,元素⑤具有
(3)元素②形成的单质气体含有
(4)元素③,⑨与H原子以原子个数比为1:1:1形成的化合物的电子式为
(5)第三周期中元素的最高价氧化物对应水化物中碱性最强的是
(6)元素③,⑤,⑨形成简单离子的半径由大到小的顺序是
您最近一年使用:0次
名校
4 . 下图为元素周期表的一部分,请参照① ⑨在表中的位置,回答下列问题:
⑨在表中的位置,回答下列问题:
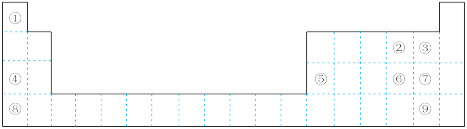
(1)最高价氧化物对应水化物碱性最强的是_______ (填化学式),氢化物热稳定性最强的是_______ (填电子式)。
(2)②③④的原子半径从大到小的顺序是_______ (填元素符号)。④⑤⑧的阳离子中氧化性最强的是_______ (填离子符号)。
(3)元素⑥的非金属性比⑦_______ (填“强”或“弱”),请从原子结构的角度解释:_______ 。
(4)现在含有元素硒( )的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多
)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多 个电子层,硒在周期表中的位置为
个电子层,硒在周期表中的位置为_______ ,则下列叙述中正确的是_______ 。
A.原子序数为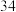
B.气态氢化物的稳定性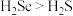
C. 不能与氢氧化钠反应
不能与氢氧化钠反应
D. 既有氧化性又有还原性
既有氧化性又有还原性
(5)①和④可形成 型离子化合物,该离子化合物的电子式为
型离子化合物,该离子化合物的电子式为_______ ,其与水反应放出气体的化学方程式为_______ 。
 ⑨在表中的位置,回答下列问题:
⑨在表中的位置,回答下列问题:
(1)最高价氧化物对应水化物碱性最强的是
(2)②③④的原子半径从大到小的顺序是
(3)元素⑥的非金属性比⑦
(4)现在含有元素硒(
 )的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多
)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多 个电子层,硒在周期表中的位置为
个电子层,硒在周期表中的位置为A.原子序数为
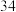
B.气态氢化物的稳定性
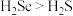
C.
 不能与氢氧化钠反应
不能与氢氧化钠反应D.
 既有氧化性又有还原性
既有氧化性又有还原性(5)①和④可形成
 型离子化合物,该离子化合物的电子式为
型离子化合物,该离子化合物的电子式为
您最近一年使用:0次
2023-02-05更新
|
278次组卷
|
2卷引用:湖南省郴州市苏仙区多校2022-2023学年高一上学期期末线上联考化学试题
名校
解题方法
5 . 填空题
(一)某同学欲验证 与
与 的金属性强弱,设计实验如下:
的金属性强弱,设计实验如下:
依据上述实验设计,回答下列问题:
(1)铝元素在周期表中的位置为第______ 周期______ 族;
(2)上述实验试管 中的实验现象为
中的实验现象为_________________________ ;
(3)写出试管 中白色沉淀溶解的离子反应方程式
中白色沉淀溶解的离子反应方程式______________________ ;
(4)上述实验现象证明碱性:
______  (填“>”“<”或“=”)
(填“>”“<”或“=”)
(二)某同学欲验证 、
、 、
、 的氧化性强弱,实验操作如下:
的氧化性强弱,实验操作如下:
Ⅰ.向盛有 和
和 混合液的试管
混合液的试管 中通入少量氯气,振荡观察;
中通入少量氯气,振荡观察;
Ⅱ.向盛有淀粉 混合液的试管
混合液的试管 中加入少量
中加入少量 溶液,振荡观察;
溶液,振荡观察;
(5) 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为____________
(6)试管 中通入少量氯气后的实验现象是
中通入少量氯气后的实验现象是______________________________
(7)写出试管 中发生的离子反应
中发生的离子反应______________________________
(一)某同学欲验证
 与
与 的金属性强弱,设计实验如下:
的金属性强弱,设计实验如下:实验操作 | 实验现象 | 反应或结论 |
Ⅰ.向试管 | ① |
|
Ⅱ.向试管 | 试管中先出现白色沉淀,后白色沉淀溶解 | ② |
(1)铝元素在周期表中的位置为第
(2)上述实验试管
 中的实验现象为
中的实验现象为(3)写出试管
 中白色沉淀溶解的离子反应方程式
中白色沉淀溶解的离子反应方程式(4)上述实验现象证明碱性:

 (填“>”“<”或“=”)
(填“>”“<”或“=”) (二)某同学欲验证
 、
、 、
、 的氧化性强弱,实验操作如下:
的氧化性强弱,实验操作如下:Ⅰ.向盛有
 和
和 混合液的试管
混合液的试管 中通入少量氯气,振荡观察;
中通入少量氯气,振荡观察;Ⅱ.向盛有淀粉
 混合液的试管
混合液的试管 中加入少量
中加入少量 溶液,振荡观察;
溶液,振荡观察;(5)
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(6)试管
 中通入少量氯气后的实验现象是
中通入少量氯气后的实验现象是(7)写出试管
 中发生的离子反应
中发生的离子反应
您最近一年使用:0次
名校
解题方法
6 . 下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)元素②的原子结构示意图是___________ ,形成化合物种类最多的元素是___________ 。(填元素符号)
(2)元素⑨在周期表中所处位置___________ ,从元素原子得失电子的角度看,元素⑨具有___________ (填“氧化性”或“还原性”)。
(3)元素③与元素⑤形成原子个数比为1:1的化合物的电子式为___________ ,该化合物中存在的化学键类型有___________ 、___________ 。
(4)第三周期元素除⑩外原子半径最大的是___________ (填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是___________ (填化学式,下同),具有两性的是___________ ,这两种物质反应的离子方程式为___________ 。
(5)元素④、⑤、⑥形成简单离子的半径由大到小的顺序是___________ 。(填离子符号)
 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)元素⑨在周期表中所处位置
(3)元素③与元素⑤形成原子个数比为1:1的化合物的电子式为
(4)第三周期元素除⑩外原子半径最大的是
(5)元素④、⑤、⑥形成简单离子的半径由大到小的顺序是
您最近一年使用:0次
名校
7 . 据南方日报报道,广东省珠江第二大水系北江流域因当地矿业的开发,造成附近河底沉积物中铊含量严重超标,致使当地人“靠江不饮北江水”。铊(Tl)是某超导体材料的组成元素之一,Tl3+与Ag在酸性介质中发生反应Tl3++2Ag=Tl++2Ag+。
(1)铊(Tl)的原子序数为81,铊在元素周期表中位于第____ 周期第______ 族。
(2)铊与下列某种元素位于同一主族,该元素是________ 。
A. 硼 B. 氮 C. 碳 D. 氟
(3)下列推断正确的是______ (填序号)。
A. 单质的还原性:Tl>Al B. 原子半径:Al>Tl C. 碱性:Al(OH)3>Tl(OH)3
D. 氧化性:Tl3+>Ag+E. Tl+最外层只有1个电子 F. Tl能形成+3价和+1价的化合物
(4)X元素是与铝属于对角线关系的第二周期元素,二者的单质化学性质相似。X单质与浓NaOH溶液反应的化学方程式是________ 。
(1)铊(Tl)的原子序数为81,铊在元素周期表中位于第
(2)铊与下列某种元素位于同一主族,该元素是
A. 硼 B. 氮 C. 碳 D. 氟
(3)下列推断正确的是
A. 单质的还原性:Tl>Al B. 原子半径:Al>Tl C. 碱性:Al(OH)3>Tl(OH)3
D. 氧化性:Tl3+>Ag+E. Tl+最外层只有1个电子 F. Tl能形成+3价和+1价的化合物
(4)X元素是与铝属于对角线关系的第二周期元素,二者的单质化学性质相似。X单质与浓NaOH溶液反应的化学方程式是
您最近一年使用:0次
10-11高一下·广东·期中
8 . 下表是元素周期表中的一部分,根据A—I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是_________ ,氧化性最强的单质是_________ ,还原性最强的单质是_________ ;
(2)最高价氧化物的水化物碱性最强的是__________ ,酸性最强的是_________ ,呈两性的是___________ ;
(3)E单质的结构式为_________ , D元素最高价氧化物的电子式为___________ ;
(4)写出B与C两元素最高价氧化物的水化物之间反应的离子方程式___________ 。
族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | A | |||||||
2 | D | E | G | I | ||||
3 | B | C | F | H |
(1)表中元素,化学性质最不活泼的是
(2)最高价氧化物的水化物碱性最强的是
(3)E单质的结构式为
(4)写出B与C两元素最高价氧化物的水化物之间反应的离子方程式
您最近一年使用:0次
解题方法
9 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)据汞的原子结构示意图 ,汞在第
,汞在第___ 周期。
(2)NH3、H2O、H2S分别为氮、氧、硫3种元素对应的氢化物,其中沸点最高的是____ ,其中心原子杂化轨道类型:___ 。
(3)下列有关性质的比较能用元素周期律解释的是__ (填字母,下同)。
a.酸性:HCl>H2SO3
b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2
d.热稳定性:Na2CO3>NaHCO3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是___ 。
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。
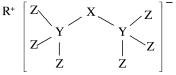
①R的元素符号为___ 。
②X的氢化物的电子式:___ 。
③写出Y的最高价氧化物的一种用途__ 。
(1)据汞的原子结构示意图
 ,汞在第
,汞在第(2)NH3、H2O、H2S分别为氮、氧、硫3种元素对应的氢化物,其中沸点最高的是
(3)下列有关性质的比较能用元素周期律解释的是
a.酸性:HCl>H2SO3
b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2
d.热稳定性:Na2CO3>NaHCO3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①R的元素符号为
②X的氢化物的电子式:
③写出Y的最高价氧化物的一种用途
您最近一年使用:0次
名校
解题方法
10 . 近年来连续出现的铊中毒事件,给各科研单位及学校危险药品的管理敲响了警钟。铊的相关信息卡片如图所示:

(1)铊的原子序数为81,铊在元素周期表中位于第________ 周期第________ 族。
(2)若设铊的质量数为A,则铊原子中中子数和质子数之差为____________ 。
(3)下列推断正确的是________ 。
A.单质的还原性:Tl>Al B.原子半径:Al>Tl
C.碱性:Al(OH)3>Tl(OH)3 D.氧化性:Tl3+>Al3+
(4)铊(Tl)是某超导材料的组成元素之一。Tl3+与Ag在酸性介质中发生反应:
Tl3++2Ag===Tl++2Ag+。下列推断正确的是________ 。
A.Tl+最外层有1个电子 B.Tl能形成+3价和+1价的化合物
C.Tl3+的氧化性比Ag+弱 D.Tl+的还原性比Ag强

(1)铊的原子序数为81,铊在元素周期表中位于第
(2)若设铊的质量数为A,则铊原子中中子数和质子数之差为
(3)下列推断正确的是
A.单质的还原性:Tl>Al B.原子半径:Al>Tl
C.碱性:Al(OH)3>Tl(OH)3 D.氧化性:Tl3+>Al3+
(4)铊(Tl)是某超导材料的组成元素之一。Tl3+与Ag在酸性介质中发生反应:
Tl3++2Ag===Tl++2Ag+。下列推断正确的是
A.Tl+最外层有1个电子 B.Tl能形成+3价和+1价的化合物
C.Tl3+的氧化性比Ag+弱 D.Tl+的还原性比Ag强
您最近一年使用:0次

 溶液,再逐滴滴入
溶液,再逐滴滴入 溶液至过量,边滴边振荡
溶液至过量,边滴边振荡 溶液,再逐滴滴入
溶液,再逐滴滴入

