名校
解题方法
1 . 中国科学家成功合成了世界上首个“五氮负离子”的盐——(N5)6(H3O)3(NH4)4Cl。该固体盐中存在的化学键类型有___________ 。1mol“五氮负离子”中所含的电子数为___________ mol。
您最近一年使用:0次
2 . 请按照要求填写:
(1)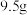 某二价金属氯化物
某二价金属氯化物 中含有
中含有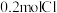 ,则
,则 的摩尔质量是
的摩尔质量是___________ 。
(2)除去镁粉中的铝粉,所选试剂为___________ ,相关的离子反应方程式为___________ 。
(3)配平离子方程式:___________ 。
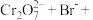 ___________=___________
___________=___________ ___________
___________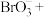 ___________
___________
(4)2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂 的一种制备方法如下。
的一种制备方法如下。___________ ;
② 的结构式是
的结构式是___________ ;
③反应Ⅰ的离子方程式是___________ 。
(1)
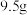 某二价金属氯化物
某二价金属氯化物 中含有
中含有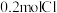 ,则
,则 的摩尔质量是
的摩尔质量是(2)除去镁粉中的铝粉,所选试剂为
(3)配平离子方程式:
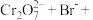 ___________=___________
___________=___________ ___________
___________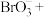 ___________
___________
(4)2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂
 的一种制备方法如下。
的一种制备方法如下。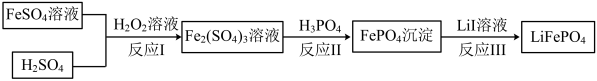
②
 的结构式是
的结构式是③反应Ⅰ的离子方程式是
您最近一年使用:0次
解题方法
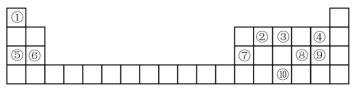
3 . 下表为元素周期表的一部分,请参照元素①-⑩在表中的位置,回答下列问题:___________ ,⑦原子结构示意图为___________ 。
(2)⑤、⑥、⑦的简单离子半径由大到小的顺序为___________ (用原子符号和“>”表示)。
(3)④⑧⑨的气态氢化物中,最稳定的是___________ (用化学式表示),最高价氧化物对应水化物中,酸性最强的是___________ (用化学式表示)。
(4)由①③⑨组成的盐化学式为___________ ,其中含有的化学键类型是___________
(2)⑤、⑥、⑦的简单离子半径由大到小的顺序为
(3)④⑧⑨的气态氢化物中,最稳定的是
(4)由①③⑨组成的盐化学式为
您最近一年使用:0次
解题方法
4 . 下列化学用语、图示与表达均正确的是
| A.离子化合物中可能有共价键 | B.HCl的电子式: |
| C.次氯酸的结构式:H-Cl-O | D. 的结构示意图 的结构示意图 |
您最近一年使用:0次
名校
5 . 下列说法正确的是
A.HCl属于共价化合物,溶于水能电离出 和 和 |
| B.NaOH是离子化合物,该物质中只含离子键 |
| C.HI气体受热分解的过程中,只需克服分子间作用力 |
| D.炭黑具有各向异性,碳原子在三维空间里呈周期性有序排列 |
您最近一年使用:0次
解题方法
6 . 下列物质中既含离子键又含共价键的是
| A.SO3 | B.Na | C.NaOH | D.NaCl |
您最近一年使用:0次
7 . 下列只含共价键的化合物是
| A.HClO4 | B.NaCl | C.KOH | D.MgCl2 |
您最近一年使用:0次
8 . W、X、Y、Z、R为原子序数依次增大的短周期主族元素,五种元素组成的某化合物可用于治疗肝昏迷及其他精神疾病,该化合物的结构简式如图所示。下列说法正确的是
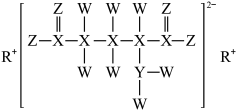
| A.简单氢化物的沸点:X>Y>Z |
| B.原子半径:R>X>Y>Z>W |
| C.R分别与Z和W形成的化合物中化学键类型完全相同 |
| D.X、Y、Z分别与W形成的化合物均是极性分子 |
您最近一年使用:0次
解题方法
9 . 下列说法错误的是
| A.Cl2不属于共价化合物 | B.离子化合物中可能有共价键 |
| C.共价化合物中可能有离子键 | D.离子键只能存在于离子化合物中 |
您最近一年使用:0次
名校
解题方法
10 . 卤化钠(NaX)和四卤化钛(TiX4)的熔点如图所示。下列判断不正确的是
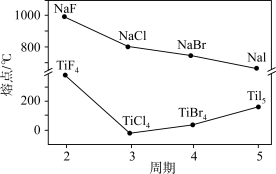
| A.NaX随X-半径增大,离子键减弱 |
| B.四氯化钛中存在共价键和分子间作用力 |
| C.TiF4的熔点反常升高是由于氢键的作用 |
| D.由图可看出F的电负性强于Cl、Br、I |
您最近一年使用:0次



