名校
解题方法
1 . 中国科学家提出了“液态阳光”概念,利用太阳能将CO2和H2O转化为液态醇类燃料,其物质和能量转化路径如图所示,下列说法错误的是

| A.CO2属于共价化合物 |
| B.该过程中能量转化的形式有:太阳能→化学能→电能 |
| C.太阳能属于不可再生能源 |
| D.液态阳光技术为化石燃料枯竭的未来提供了一种可能的能源解决方案 |
您最近一年使用:0次
名校
2 . 随原子序数递增,八种短周期元素(用字母 等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。
等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。
(1)f在周期表中的位置是_______ 。
(2) 、
、 两种元素的原子可构成一种碱性物质,该物质的电子式是
两种元素的原子可构成一种碱性物质,该物质的电子式是_______ 。
(3)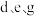 三者简单离子的半径由大到小顺序是(用离子符号表示):
三者简单离子的半径由大到小顺序是(用离子符号表示):_______ 。
(4)写出一个能证明 非金属性强弱的化学方程式:
非金属性强弱的化学方程式:_______ 。
(5)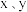 最简单化合物的空间构型为
最简单化合物的空间构型为_______ 。
(6)下列判断不正确的是_______。
 等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。
等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。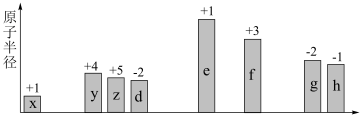
(1)f在周期表中的位置是
(2)
 、
、 两种元素的原子可构成一种碱性物质,该物质的电子式是
两种元素的原子可构成一种碱性物质,该物质的电子式是(3)
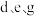 三者简单离子的半径由大到小顺序是(用离子符号表示):
三者简单离子的半径由大到小顺序是(用离子符号表示):(4)写出一个能证明
 非金属性强弱的化学方程式:
非金属性强弱的化学方程式:(5)
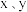 最简单化合物的空间构型为
最简单化合物的空间构型为(6)下列判断不正确的是_______。
A. 和 和 可以形成 可以形成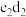 型化合物,正、负离子物质的量之比为 型化合物,正、负离子物质的量之比为 |
B.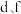 组成的化合物具有两性 组成的化合物具有两性 |
C. 的最高价氧化物对应水化物与 的最高价氧化物对应水化物与 的氢化物反应生成产物中既含有离子键又含有共价键 的氢化物反应生成产物中既含有离子键又含有共价键 |
D. 与 与 同主族,相差两个周期 同主族,相差两个周期 |
您最近一年使用:0次
名校
解题方法
3 . 乙烯催化氧化的过程如下图(部分相关离子未画出),下列描述不正确的是
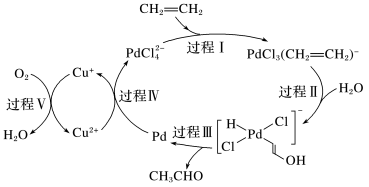
| A.该转化过程中Pd的价态发生了变化 |
| B.该转化过程中,有非极性键的断裂与极性键的形成 |
| C.Cu+为该反应的催化剂 |
D.乙烯催化氧化反应的化学方程式为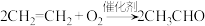 |
您最近一年使用:0次
4 . 下列物质中含有极性键的盐是
A. | B. | C. | D.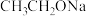 |
您最近一年使用:0次
名校
5 . 元素周期表反映元素之间的内在联系,是研究物质性质的重要工具。如图是元素周期表的一部分,请回答下列问题:
(1)元素③、④、⑧的简单离子半径由大到小 的排序为______ (填离子符号)。
(2)⑤和⑧组成的化合物的电子式为______ 。
化合物X由③和④元素单质高温下反应生成,其含有的化学键为______ (填化学键类型)
(3)⑥的氧化物和②的最高价氧化物对应的水化物反应的离子方程式为______ 。
(4)用一个化学方程式说明非金属性⑧>⑦(不可使用 )
)______ 。
周期 | IA | 0 | |||||||
1 | IIA | … | IIIA | IVA | VA | VIA | VIIA | ||
2 | ① | ② | ③ | ||||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)⑤和⑧组成的化合物的电子式为
化合物X由③和④元素单质高温下反应生成,其含有的化学键为
(3)⑥的氧化物和②的最高价氧化物对应的水化物反应的离子方程式为
(4)用一个化学方程式说明非金属性⑧>⑦(不可使用
 )
)
您最近一年使用:0次
6 . 离子液体是指由体积较大的阴、阳离子组成,并且在室温或接近室温下呈液态的盐,也称为低温熔融盐。有许多优点,例如难挥发,有良好的导电性,可作溶剂、电解质、催化剂等。1-正丁基-3-甲基咪唑六氟磷酸盐是一种离子液体,结构简式如图,下列关于它的叙述正确的是
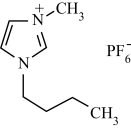 或
或
A.该新型化合物含有的C、N、P元素均为 杂化 杂化 |
| B.1-正丁基-3-甲基咪唑六氟磷酸盐属于含共价键的离子化合物 |
| C.电负性:F>N>H>C |
| D.该新型化合物的组成元素全部位于元素周期表p区 |
您最近一年使用:0次
名校
解题方法
7 . 元素周期表与元素周期律在化学学习研究中有很重要的作用。下表是元素周期表的一部分
(1)④和②组成的一种化合物颜色为淡黄色,请写出该化合物的电子式_______ ,该化合物含有的化学键类型有_______ 。
(2)请写出元素①的简单氢化物的结构式_______ 。
(3)元素①、②、⑦简单氢化物的稳定性最强的是_______ (用化学式表示) 。
(4)元素①、②、⑧简单氢化物的沸点最高的是_______ (用化学式表示) 。
(5)元素③、⑤、⑨的简单离子半径由大到小的顺序(用离子符号表示)_______ 。
(6)写出元素①最高价氧化物对应水化物稀溶液与铜应的化学方程式_______ 。
(7)元素非金属性强弱比较有很多方法,其中比较⑧和⑨的非金属性强弱的研究方案中不可行的是:_______(填序号)。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | |||||||
| 2 | ① | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)请写出元素①的简单氢化物的结构式
(3)元素①、②、⑦简单氢化物的稳定性最强的是
(4)元素①、②、⑧简单氢化物的沸点最高的是
(5)元素③、⑤、⑨的简单离子半径由大到小的顺序(用离子符号表示)
(6)写出元素①最高价氧化物对应水化物稀溶液与铜应的化学方程式
(7)元素非金属性强弱比较有很多方法,其中比较⑧和⑨的非金属性强弱的研究方案中不可行的是:_______(填序号)。
| A.比较两种单质的颜色 | B.比较两种单质与 化合的难易程度 化合的难易程度 |
| C.依据两元素在周期表中的位置 | D.比较氧化物对应水化物的酸性 |
您最近一年使用:0次
名校
解题方法
8 . 下列关于晶体的说法不正确的是
①含有离子的晶体一定是离子晶体
②分子晶体若采取面心密堆积方式,其配位数是12
③含有共价键的晶体一定是共价晶体
④分子晶体的熔点一定比金属晶体的低
⑤MgO远比NaCl的熔点高
⑥共价键的强弱决定分子晶体熔、沸点的高低
①含有离子的晶体一定是离子晶体
②分子晶体若采取面心密堆积方式,其配位数是12
③含有共价键的晶体一定是共价晶体
④分子晶体的熔点一定比金属晶体的低
⑤MgO远比NaCl的熔点高
⑥共价键的强弱决定分子晶体熔、沸点的高低
| A.①③④⑥ | B.①②③⑤ | C.①②④ | D.②③④⑥ |
您最近一年使用:0次
名校
9 . 下列物质中既具有共价键又具有离子键的是
| A.NaCl | B.CaCl2 | C.NO2 | D.KNO3 |
您最近一年使用:0次
名校
10 . X、Y、Z、U、V、W是原子序数依次增大的短周期主族元素。X存在一种核素原子核中没有中子,化合物 的电子总数为18,Z元素的最外层电子数是内层电子数的3倍,X与U同主族,Z与W同主族,V与Z形成的化合物具有两性。以下说法中错误的是
的电子总数为18,Z元素的最外层电子数是内层电子数的3倍,X与U同主族,Z与W同主族,V与Z形成的化合物具有两性。以下说法中错误的是
 的电子总数为18,Z元素的最外层电子数是内层电子数的3倍,X与U同主族,Z与W同主族,V与Z形成的化合物具有两性。以下说法中错误的是
的电子总数为18,Z元素的最外层电子数是内层电子数的3倍,X与U同主族,Z与W同主族,V与Z形成的化合物具有两性。以下说法中错误的是| A.离子半径:W>Z>V |
| B.简单气态氢化物热稳定性:Z>Y |
| C.Z与U元素形成的化合物中阴阳离子个数比均为1∶2 |
| D.X、Y、Z三种元素形成的化合物一定是共价化合物 |
您最近一年使用:0次



