解题方法
1 . 下列各项叙述中,正确的是
| A.电负性:S>As>Se | B.键角:H2O<NH3<CH4 |
| C.沸点:HF>HCl>HBr>HI | D.离子还原性:S2->I->Br->Cl- |
您最近一年使用:0次
2 . 下列说法正确的是
| A.化学键既存在于相邻原子之间,又存在于相邻分子之间 |
| B.HF、HCl、HBr、HI的热稳定性依次减弱 |
| C.电负性越大,非金属性越强,第一电离能也越大 |
| D.碳碳双键的键能是碳碳单键键能的2倍 |
您最近一年使用:0次
2020-05-11更新
|
112次组卷
|
2卷引用:天津市河北区2020届高三总复习质量检测(一)(一模)化学试题
3 . 氢、氮、氯、铜是元素周期表中前四周期元素。回答下列问题:
(1)铜在元素周期表中的位置__ ,写出NH3的电子式__ 。
(2)氯与硫相比,非金属性较强的是__ (用元素符号表示),下列事实能证明这一结论的是__ 。(填序号)。
a.常温下氯的单质呈气态,硫的单质呈固态
b.稳定性:HCl>H2S
c.酸性:HClO4>H2SO4
d.氯的电负性大于硫的电负性
(3)含氮化合物(CH3)3N与盐酸反应,离子方程式为:(CH3)3N+H+=[(CH3)3NH]+,该反应过程中新生成的化学键为___ (填序号)。
a.离子键 b.配位键 c.氢键 d.非极性共价键
若化合物(CH3)3N能溶于水,其可能的原因是___ 。
(4)Cu与H元素形成某种晶体的结构如图所示,则该晶体的化学式为__ ,若该晶体的密度为ρ g•cm-3,阿伏加 德罗常数的值为NA,则该晶胞的棱长为__ nm(用含ρ和NA的式子表示,已知1nm=10-7cm)。

(1)铜在元素周期表中的位置
(2)氯与硫相比,非金属性较强的是
a.常温下氯的单质呈气态,硫的单质呈固态
b.稳定性:HCl>H2S
c.酸性:HClO4>H2SO4
d.氯的电负性大于硫的电负性
(3)含氮化合物(CH3)3N与盐酸反应,离子方程式为:(CH3)3N+H+=[(CH3)3NH]+,该反应过程中新生成的化学键为
a.离子键 b.配位键 c.氢键 d.非极性共价键
若化合物(CH3)3N能溶于水,其可能的原因是
(4)Cu与H元素形成某种晶体的结构如图所示,则该晶体的化学式为

您最近一年使用:0次
解题方法
4 . A、B、C、D是四种短周期元素,E是过渡元素,A、B、C同周期,C、D同主族,A的原子结构示意图为: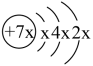 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2。回答下列问题:
(1)用元素符号 表示C所在周期(除稀有气体元素外)电负性最大的元素是___________ 。
(2)写出E的元素符号___________ 。
(3)C元素的氢化物分子中C原子的杂化方式为___________ 。
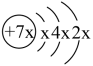 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2。回答下列问题:(1)用
(2)写出E的元素符号
(3)C元素的氢化物分子中C原子的杂化方式为
您最近一年使用:0次
解题方法
5 . 回答下列问题:
(1)某基态原子的价层电子的轨道表示式为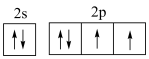
①s电子的电子云轮廓图是______________ 形
②有______________ 种空间运动状态不同的电子
③最外层有______________ 个电子
④有______________ 种能量不同的电子
(2)四种元素基态原子的电子排布式如下:①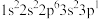 ;②
;② ;③
;③ ;④
;④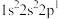
①第一电离能:①______________ ②(填“>”、“=”或“<”)
②电负性:③______________ ④(填“>”、“=”或“<”)
(1)某基态原子的价层电子的轨道表示式为

①s电子的电子云轮廓图是
②有
③最外层有
④有
(2)四种元素基态原子的电子排布式如下:①
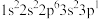 ;②
;② ;③
;③ ;④
;④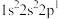
①第一电离能:①
②电负性:③
您最近一年使用:0次
解题方法
6 . H、C、N、O、S、C1是非常重要的非金属元素,广泛存在于自然界。回答下列问题:
(1)H、C、O元素电负性由大到小的顺序为___________ 。
(2) 分子中
分子中 的杂化方式为
的杂化方式为___________ 杂化。
(3)基态硫原子的价层电子排布式___________ 。
(4)硫单质的一种结构为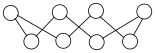 ,该物质
,该物质___________ (填“可溶”或“难溶”)于水。
(5)沸点:
___________  (填“>”或“<”),原因:
(填“>”或“<”),原因:___________ 。
(6)已知 的键能为
的键能为 的键能为
的键能为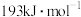 ,则
,则 分子中
分子中 键键能为
键键能为___________  。
。
(7) 是一种大气污染物,液氯储存区贴有的说明卡如下(部分):
是一种大气污染物,液氯储存区贴有的说明卡如下(部分):
①用离子方程式表示“泄漏处理”中 溶液的作用
溶液的作用___________ 。
②除掉 中的
中的 通过饱和食盐水,这种操作方法是
通过饱和食盐水,这种操作方法是___________ 法。
(1)H、C、O元素电负性由大到小的顺序为
(2)
 分子中
分子中 的杂化方式为
的杂化方式为(3)基态硫原子的价层电子排布式
(4)硫单质的一种结构为
 ,该物质
,该物质(5)沸点:

 (填“>”或“<”),原因:
(填“>”或“<”),原因:(6)已知
 的键能为
的键能为 的键能为
的键能为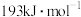 ,则
,则 分子中
分子中 键键能为
键键能为 。
。(7)
 是一种大气污染物,液氯储存区贴有的说明卡如下(部分):
是一种大气污染物,液氯储存区贴有的说明卡如下(部分):| 危险性 |  |
| 储运要求 | 远离金属粉末、氮、烃类、醇类物质;设置氯气检测仪 |
| 泄漏处理 | 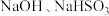 溶液吸收 溶液吸收 |
| 包装 | 钢瓶 |
 溶液的作用
溶液的作用②除掉
 中的
中的 通过饱和食盐水,这种操作方法是
通过饱和食盐水,这种操作方法是
您最近一年使用:0次
解题方法
7 . 下列说法或解释错误的是
| A.C、N、O的电负性逐渐增大,其最简单氢化物分子中键角逐渐减小 |
B.可燃冰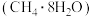 中甲烷分子与水分子间不会形成氢键 中甲烷分子与水分子间不会形成氢键 |
C.漂白粉溶液在空气中失效: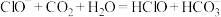 |
D.铜片在 和稀硫酸混合液中溶解: 和稀硫酸混合液中溶解: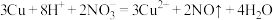 |
您最近一年使用:0次



