解题方法
1 . 恩格列净是治疗2型糖尿病的一种原料药,其关键中间体(F)的合成路线如下:
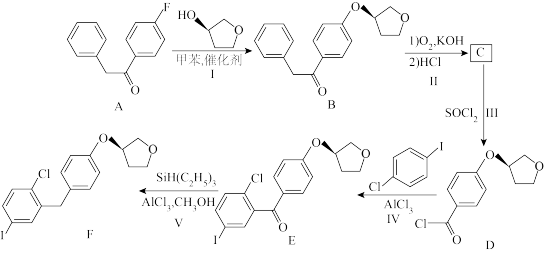
已知: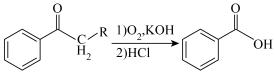 +RCOOH
+RCOOH
回答下列问题:
(1)B分子含有的官能团名称为
(2)反应Ⅰ在
(3)反应Ⅱ生成两种有机物,一种为C,另一种产物的结构简式为
(4)
 易水解:
易水解: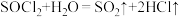 。反应Ⅲ的化学方程式为
。反应Ⅲ的化学方程式为(5)V的反应类型为
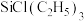 ,若反应中Si的化合价不变,则
,若反应中Si的化合价不变,则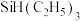 中三种元素按电负性由大到小排列为
中三种元素按电负性由大到小排列为(6)芳香族化合物G是C的同分异构体,请写出符合下列条件的G的结构简式
①能与 溶液反应产生气体
溶液反应产生气体
②核磁共振氢谱有四组峰且峰面积比为6∶3∶2∶1。
您最近一年使用:0次
名校
解题方法
2 . 运用物质结构与性质的相关知识,回答下列问题:
(1) 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是_______ 。基态 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有_____ 个伸展方向,原子轨道呈______ 形。
(2) 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为________ , 价电子轨道表示式为
价电子轨道表示式为________ 。
(3) 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。
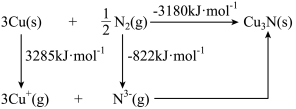
通过图中数据________ (填“能”或“不能”)计算出 原子的第一电离能,
原子的第一电离能, 的晶格能为
的晶格能为________  。
。
(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。
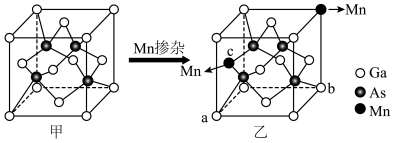
①GaAs晶胞中距离Ga原子最近As原子的个数为________ 。
②掺杂 之后,晶体中
之后,晶体中 的原子个数比为
的原子个数比为________ (化为最简整数比)。
(1)
 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有(2)
 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为 价电子轨道表示式为
价电子轨道表示式为(3)
 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。
通过图中数据
 原子的第一电离能,
原子的第一电离能, 的晶格能为
的晶格能为 。
。(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。

①GaAs晶胞中距离Ga原子最近As原子的个数为
②掺杂
 之后,晶体中
之后,晶体中 的原子个数比为
的原子个数比为
您最近一年使用:0次
名校
解题方法
3 . 酞菁和酞菁钴可制得光动力学中的光敏剂,分子结构如图,其中酞菁分子中所有原子共平面,下列说法正确的是
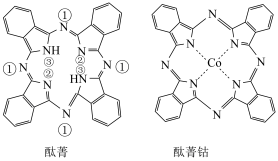
| A.酞菁钴中钴的化合价为+4 |
| B.直径为1.5×10–9 m的酞菁钴分子能透过半透膜 |
| C.酞菁钴中元素的电负性由大到小的顺序为N>C>H>Co |
| D.标注①②的N原子的杂化方式是sp2,③的N原子的杂化方式是sp3 |
您最近一年使用:0次
2024-03-13更新
|
481次组卷
|
2卷引用:福建省厦门第一中学2023-2024学年高三下学期2月第一次月考化学试卷
名校
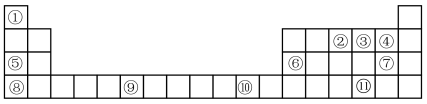
4 . 表格为门捷列夫元素周期表的一部分,其中的编号代表对应的元素。用元素符号回答下列问题:
(1)基态F原子有___________ 种运动状态的电子。
(2)元素③⑪电负性较大的是___________ ;Se的原子结构示意图为___________ 。
(3)元素铬的基态原子的价电子排布图为:___________ 。
(4)Cu基态原子中,能量最高的电子占据的原子轨道的形状为___________ 。
(5)该表格中电负性最大的元素与第一电离能最小的元素形成的化合物的电子式为________ 。
(6)②③的简单气态氢化物中较稳定的是___________ (填化学式),元素⑥⑦的最高价氧化物的水化物相互反应的离子方程式为___________ 。
(1)基态F原子有
(2)元素③⑪电负性较大的是
(3)元素铬的基态原子的价电子排布图为:
(4)Cu基态原子中,能量最高的电子占据的原子轨道的形状为
(5)该表格中电负性最大的元素与第一电离能最小的元素形成的化合物的电子式为
(6)②③的简单气态氢化物中较稳定的是
您最近一年使用:0次
2023-09-16更新
|
254次组卷
|
2卷引用:福建省龙岩市连城县第一中学2022-2023学年高二下学期3月月考化学试题
5 . 实验室用邻二氮菲(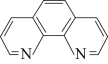 )与
)与 形成的红色配合离子(图1)测定
形成的红色配合离子(图1)测定 的浓度。回答下列问题:
的浓度。回答下列问题:

(1)Fe元素在周期表中的位置为__________ ,该配合物中心离子的配位数为__________ 。
(2)该配合离子所含元素的电负性最大的是__________ ,C原子的杂化方式为__________ 。
(3)该配合离子存在的化学键类型有__________ 。
a.离子键 b.配位键 c.极性键 d.非极性键 e.金属键 f.氢键
(4)从结构角度分析, 易被氧化成
易被氧化成 的原因是
的原因是__________ 。
(5)合成氨反应中铁催化剂表面吸附氮原子,图2为氮原子在铁的晶面上的单层附着局部示意图,图中铁原子与氮原子的个数比为__________ 。
(6)铁晶体中的原子堆积方式如图3所示, 表示阿伏加德罗常数的值,晶胞参数为
表示阿伏加德罗常数的值,晶胞参数为 ,若晶胞密度为
,若晶胞密度为 ,则
,则
__________ (列出表达式)。
 )与
)与 形成的红色配合离子(图1)测定
形成的红色配合离子(图1)测定 的浓度。回答下列问题:
的浓度。回答下列问题:
(1)Fe元素在周期表中的位置为
(2)该配合离子所含元素的电负性最大的是
(3)该配合离子存在的化学键类型有
a.离子键 b.配位键 c.极性键 d.非极性键 e.金属键 f.氢键
(4)从结构角度分析,
 易被氧化成
易被氧化成 的原因是
的原因是(5)合成氨反应中铁催化剂表面吸附氮原子,图2为氮原子在铁的晶面上的单层附着局部示意图,图中铁原子与氮原子的个数比为
(6)铁晶体中的原子堆积方式如图3所示,
 表示阿伏加德罗常数的值,晶胞参数为
表示阿伏加德罗常数的值,晶胞参数为 ,若晶胞密度为
,若晶胞密度为 ,则
,则
您最近一年使用:0次
6 . 短周期元素W、X、Y、Z原子序数依次递增,X、Z同主族,W、Y同主族。由上述元素组成的物质甲~已转化关系如图,乙、丙、丁、戊都是二元化合物,丁的焰色反应为黄色,己为淡黄色单质。下列说法错误的是
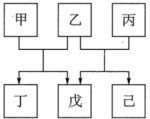

| A.只有甲的水溶液为碱性 | B.键角:丙>戊 |
| C.沸点:己>乙 | D.电负性: |
您最近一年使用:0次
名校
解题方法
7 . 下列类比或推理合理的是
| 选项 | 已知 | 方法 | 结论 |
| A | 钠保存在煤油中 | 类比 | 锂保存在煤油中 |
| B |  是离子化合物 是离子化合物 | 类比 |  是离子化合物 是离子化合物 |
| C | 非金属性: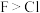 | 推理 | 沸点: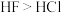 |
| D |  是正盐 是正盐 | 推理 |  是一元酸 是一元酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-11更新
|
449次组卷
|
3卷引用:福建省泉州第五中学2023届高三一模化学试题
名校
解题方法
8 . 中国科学家首次在月球上发现新矿物,将其命名为“嫦娥石”,“嫦娥石”中包含了Fe、Cu、Ti、Cr、Ni、Mo、N、O等多种元素。
(1)鉴定月球土壤的元素组成,可采用的方法是___________ 。
A.光谱分析 B.X-射线衍射分析
(2)在第二周期中,第一电离能比N高的主族元素是___________ 。氮原子的电子排布图表示的状态中,能量由低到高的顺序是___________ (填序号)。
A.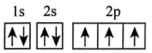 B.
B.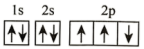
C.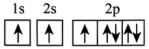 D.
D.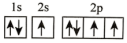
(3)已知有关氮、磷的单键和三键的键能( )如下表:
)如下表:
从能量角度看,氮以 、而白磷以
、而白磷以 (结构式可表示为
(结构式可表示为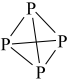 )形式存在的原因是
)形式存在的原因是___________ 。
(4)已知 分子的键角约为107°,而同主族磷的氢化物
分子的键角约为107°,而同主族磷的氢化物 分子的键角约为94°,试用价层电子对互斥模型解释
分子的键角约为94°,试用价层电子对互斥模型解释 的键角比
的键角比 的键角大的原因:
的键角大的原因:___________
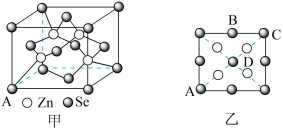
(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,已知晶胞边长为apm,乙图为甲图的俯视图,若原子坐标A为(0,0,0),B为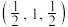 ,则D原子坐标为
,则D原子坐标为___________ ;若该晶胞密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为_________________ 。
(1)鉴定月球土壤的元素组成,可采用的方法是
A.光谱分析 B.X-射线衍射分析
(2)在第二周期中,第一电离能比N高的主族元素是
A.
 B.
B.
C.
 D.
D.
(3)已知有关氮、磷的单键和三键的键能(
 )如下表:
)如下表:| N-N |  | P-P |  |
| 193 | 946 | 197 | 489 |
从能量角度看,氮以
 、而白磷以
、而白磷以 (结构式可表示为
(结构式可表示为 )形式存在的原因是
)形式存在的原因是(4)已知
 分子的键角约为107°,而同主族磷的氢化物
分子的键角约为107°,而同主族磷的氢化物 分子的键角约为94°,试用价层电子对互斥模型解释
分子的键角约为94°,试用价层电子对互斥模型解释 的键角比
的键角比 的键角大的原因:
的键角大的原因:(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,已知晶胞边长为apm,乙图为甲图的俯视图,若原子坐标A为(0,0,0),B为
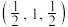 ,则D原子坐标为
,则D原子坐标为 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为
您最近一年使用:0次
9 . 回答下列问题:
(1)下列现象与原子核外电子跃迁有关的是___________ (填序号)。
a.焰火 b.LED灯光 c.金属导电
(2)在周期表中,与Li的化学性质最相似的邻族元素是___________ 。
(3)硼、钛等元素的化合物具有广泛的应用价值。
①B原子中存在未成对电子的能级电子云在空间有___________ 种伸展方向。
② (硼氢化钛)可由
(硼氢化钛)可由 和
和 反应制得。基态钛原子的价层电子轨道表示式为
反应制得。基态钛原子的价层电子轨道表示式为___________ 。电负性大小顺序为H___________ B(填“>”或“<”)。
(4)氮单质及其化合物在研究和生产中有着广泛的应用。
①亚硝酰氯(NOCl)是一种红褐色液体,每个原子最外层都达到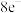 结构,则其电子式为
结构,则其电子式为___________ ,其水解会生成两种酸,写出水解的化学方程式___________ 。
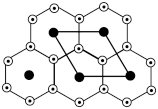
②氮化锂晶体中存在锂、氮原子共同组成的锂、氮层,锂原子以石墨晶体中的碳原子方式排布,N原子处在六元环的中心,同层中锂、氮的原子个数比为___________ ;
(1)下列现象与原子核外电子跃迁有关的是
a.焰火 b.LED灯光 c.金属导电
(2)在周期表中,与Li的化学性质最相似的邻族元素是
(3)硼、钛等元素的化合物具有广泛的应用价值。
①B原子中存在未成对电子的能级电子云在空间有
②
 (硼氢化钛)可由
(硼氢化钛)可由 和
和 反应制得。基态钛原子的价层电子轨道表示式为
反应制得。基态钛原子的价层电子轨道表示式为(4)氮单质及其化合物在研究和生产中有着广泛的应用。
①亚硝酰氯(NOCl)是一种红褐色液体,每个原子最外层都达到
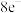 结构,则其电子式为
结构,则其电子式为②氮化锂晶体中存在锂、氮原子共同组成的锂、氮层,锂原子以石墨晶体中的碳原子方式排布,N原子处在六元环的中心,同层中锂、氮的原子个数比为

您最近一年使用:0次
名校
解题方法
10 . 下列有关合成药物胃复安的说法不正确的是
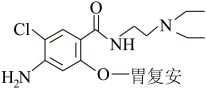
| A.分子中碳原子有2种杂化类型 |
| B.该分子组成元素的电负性由大到小的顺序为:O>N>C>H |
| C.该分子组成元素第一电离能最大的是O |
| D.分子中所有氮原子上都有一对孤电子对 |
您最近一年使用:0次
2023-03-16更新
|
248次组卷
|
2卷引用:福建省龙岩第一中学2022-2023学年高二下学期第一次月考化学试题



