解题方法
1 . 1932年美国化学家鲍林首先提出了电负性的概念。电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:
请仔细分析,回答下列有关问题:
(1)预测周期表中电负性最大的元素应为_______ ;估计钙元素的电负性的取值范围:_______ <X<_______ 。
(2)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为_______ 。
(3)请你预测Br与I元素的X数值的大小关系:X(Br)_______ X(I)。
(4)某有机化合物分子中含有S—N键,你认为该共用电子对偏向于_______ 原子(填元素符号)。
(5)根据表中的所给数据分析: 同主族内的不同元素的X值变化的规律是_______ ;
(6)化合物NaH能与水反应产生氢气,所以可用做生氢剂,写出该反应的化学方程式:_______ 。
(7)下列表述中,不能证明氯的非金属性比硫强的是_______ 。
A.气态氢化物的稳定性:HCl>H2S
B.两元素的电负性:S<Cl
C.最高价含氧酸的酸性:HClO4>H2SO4
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应:Cl2+H2S=2HCl+S↓
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
(1)预测周期表中电负性最大的元素应为
(2)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为
(3)请你预测Br与I元素的X数值的大小关系:X(Br)
(4)某有机化合物分子中含有S—N键,你认为该共用电子对偏向于
(5)根据表中的所给数据分析: 同主族内的不同元素的X值变化的规律是
(6)化合物NaH能与水反应产生氢气,所以可用做生氢剂,写出该反应的化学方程式:
(7)下列表述中,不能证明氯的非金属性比硫强的是
A.气态氢化物的稳定性:HCl>H2S
B.两元素的电负性:S<Cl
C.最高价含氧酸的酸性:HClO4>H2SO4
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应:Cl2+H2S=2HCl+S↓
您最近一年使用:0次
2 . 下列曲线表示卤族元素某种性质随核电荷数递增的变化趋势,其中正确的是
A.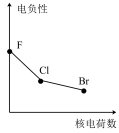 | B.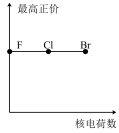 | C.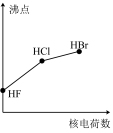 | D.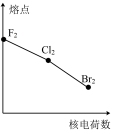 |
您最近一年使用:0次
2022-08-25更新
|
539次组卷
|
39卷引用:【全国百强校】福建省莆田第一中学2018-2019学年高二下学期期中考试化学试题
【全国百强校】福建省莆田第一中学2018-2019学年高二下学期期中考试化学试题福建省莆田第一中学2020-2021学年高二下学期期中考试化学试题2014-2015学年浙江省台州中学高二下第一次统练化学试卷2015-2016学年山西省大同一中高二下3月月考化学试卷2015-2016学年山西大学附中高二5月模块诊断化学试卷2016-2017学年山东省滨州市高二下学期第一次阶段性测试化学试卷安徽省淮北市第一中学2016-2017学年高二下学期期中考试化学试题山西省临汾第一中学等五校2017-2018学年高二上学期期末联考化学试题山西省大同市第三中学2017-2018学年高二下学期4月月考化学试题吉林省延边市第二中学2017-2018学年高二下学期第一次月考化学试题山东师范大学附属中学2017-2018学年高二下学期期中考试(理)化学试题山东省师范大学附属中学2017-2018学年高二下学期第七次学分认定考试(期中)(理)化学试题【全国百强校】山西省大同市第一中学2017-2018学年高二5月月考化学试题【全国校级联考】新疆昌吉市教育共同体四校2017-2018学年高二下学期期末联考化学试题宁夏回族自治区银川市长庆高级中学2018-2019学年高二下学期第二次月考化学试题新疆石河子第二中学2018-2019学年高二下学期期末考试化学试题宁夏银川一中2018-2019学年高二下学期期末考试化学试题河南省洛阳市2019-2020学年高二上学期期末考试化学试题陕西省西安市西安高新第一中学2018-2019学年高二下学期期末考试化学试题江苏省东台创新高级中学2019-2020学年高二下学期4月份月检测化学试题山东潍坊高密一中2020-2021学年高二上学期12月化学月考试题陕西省宝鸡市长岭中学2021-2022学年高二下学期期中考试化学试题专题2 原子结构与元素性质 第二单元 元素性质的递变规律 第2课时 元素第一电离能和电负性的周期性变化江苏省盐城市田家炳中学2021-2022学年高二下学期期中考试化学试题浙江省浦江中学、长兴中学、余杭高中2021-2022学年高二下学期三校联考(3月)化学试题新疆伊犁州新源县2021-2022学年高二下学期期末考试化学试题安徽省 淮北师范大学附属实验中学2022-2023学年高二下学期第一次月考化学试题湖北省武汉重点中学5G联合体2022-2023学年高二下学期期中考试化学试题2.2.2元素第一电离能和电负性的周期性变化 课后江苏省无锡市匡园双语学校2022-2023学年高二下学期第一次月考化学试卷【全国百强校】天津市第一中学2017-2018学年高一下学期期中考试化学试题四川省眉山市2018-2019学年高一下学期期末教学质量检测化学试题江苏省如东高级中学2019-2020学年高一下学期第二次阶段测试化学试题北京市朝阳区2020届高三5月适应性模拟化学试卷人教版(2019)高一必修第一册 第四章 物质结构 元素周期律 章末综合检测卷(已下线)专题4.1.4 卤族元素(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)甘肃省张掖市第二中学 2021-2022学年高一下学期3月月考化学试题山东师范大学附属中学2021-2022学年高一下学期第一次月考化学试题北京市中关村中学2023-2024学年高三上学期开学考试化学试卷
名校
3 . 纯碱( )是重要的基础化工原料,我国化学家侯德榜在1943年提出了著名侯氏制碱法。原理为:将
)是重要的基础化工原料,我国化学家侯德榜在1943年提出了著名侯氏制碱法。原理为:将 通入氨化的饱和食盐水中析出
通入氨化的饱和食盐水中析出 晶体,将得到的
晶体,将得到的 晶体加热分解生成
晶体加热分解生成 。下列有关
。下列有关 、
、 、
、 和
和 的说法正确的是
的说法正确的是
 )是重要的基础化工原料,我国化学家侯德榜在1943年提出了著名侯氏制碱法。原理为:将
)是重要的基础化工原料,我国化学家侯德榜在1943年提出了著名侯氏制碱法。原理为:将 通入氨化的饱和食盐水中析出
通入氨化的饱和食盐水中析出 晶体,将得到的
晶体,将得到的 晶体加热分解生成
晶体加热分解生成 。下列有关
。下列有关 、
、 、
、 和
和 的说法正确的是
的说法正确的是A.电负性: | B.沸点: |
C.键角: | D. 为极性分子,CO2为非极性分子 为极性分子,CO2为非极性分子 |
您最近一年使用:0次
2022-07-07更新
|
302次组卷
|
3卷引用:福建省福州屏东中学2023-2024学年高二下学期期中考试化学试题
解题方法
4 . 建盏由建阳坯土、天然矿物釉烧制,含有SiO2、Al2O3、Fe2O3、FeO、CaO、TiO2等化学成分。
(1)现代化学可利用_______ 特征谱线来鉴定建盏中的元素。
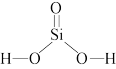
(2)建盏胎釉中含SiO2是硅酸的酸酐。硅酸结构式如图所示,硅原子的杂化方式_______ 。
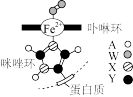
(3)Fe2+与蛋白质链上咪唑环通过配位键连接形成的物质结构如图所示。A、W、X、Y为短周期前10号主族元素。四种元素的电负性由大到小的顺序为_______ (用元素符号表示)。
(4)元素Fe在周期表中的位置为_______ ;其第三电离能(I3)为2957 KJ· mol-1、第四电离能(I4)为5290 KJ· mol-1,I4远大于I3的原因为_______ 。
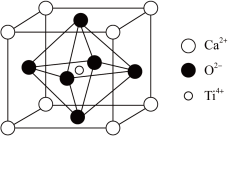
(5)建盏胎釉矿石中的钙钛矿晶胞如图所示,Ti4+处于6个O2-组成的_______ 空隙中,在钙钛矿晶胞结构的另一种表示中,Ti4+处于各顶角位置,则O2-处于_______ 位置(选填“面心”“体心”或“棱心”)。已知晶胞密度为 ρ g∙cm-3,则两个O2-离子间的最短距离为_______ nm(阿伏加德罗常数的值为NA,列出表达式)。
(1)现代化学可利用
(2)建盏胎釉中含SiO2是硅酸的酸酐。硅酸结构式如图所示,硅原子的杂化方式

(3)Fe2+与蛋白质链上咪唑环通过配位键连接形成的物质结构如图所示。A、W、X、Y为短周期前10号主族元素。四种元素的电负性由大到小的顺序为

(4)元素Fe在周期表中的位置为
(5)建盏胎釉矿石中的钙钛矿晶胞如图所示,Ti4+处于6个O2-组成的

您最近一年使用:0次
解题方法
5 . 已知①~⑦号元素在周期表中的位置如图。请回答下列问题:
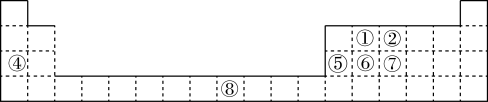
(1)基态③原子核外有____ 种空间运动状态不同的电子,其中能量最高的电子所在原子轨道的电子云轮廓图为____ 形。
(2)①、④、⑥三种元素的电负性由大到小的顺序为____ (用元素符号表示)。
(3)⑧位于元素周期表中____ (填“s、p、d或ds”)区,与⑧位于同一周期且含有相同未成对电子数的元素为____ (填元素符号)。
(4)①和⑤可形成一种黄色晶体,熔点2200℃,熔融态不导电。该晶体的类型为____ 。
(5)⑦号元素的五氯化物是共价化合物,其分子的空间结构为三角双锥形,依靠sp3d杂化形成。②和⑦同主族,但不存在②号元素的五氯化物,从原子结构的角度分析其原因是____ 。

(1)基态③原子核外有
(2)①、④、⑥三种元素的电负性由大到小的顺序为
(3)⑧位于元素周期表中
(4)①和⑤可形成一种黄色晶体,熔点2200℃,熔融态不导电。该晶体的类型为
(5)⑦号元素的五氯化物是共价化合物,其分子的空间结构为三角双锥形,依靠sp3d杂化形成。②和⑦同主族,但不存在②号元素的五氯化物,从原子结构的角度分析其原因是
您最近一年使用:0次
解题方法
6 . 化合物A是一种新型锅炉水除氧剂,其结构式如图所示: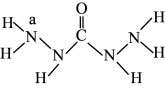 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.碳、氮元素的电负性比较是 |
B.氮原子与碳原子分别为 杂化与 杂化与 杂化 杂化 |
C.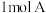 分子中所含 分子中所含 键、 键、 键的数目之比为10∶1 键的数目之比为10∶1 |
| D.编号为a的氮原子和与其成键的另外三个原子在同一平面内 |
您最近一年使用:0次
7 . 按要求回答下列问题:
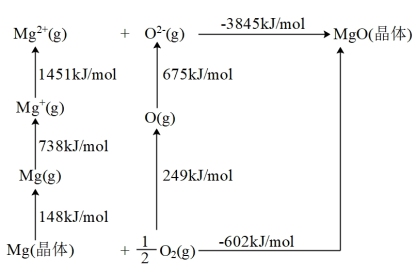
(1)MgO的Born-Haber循环如图所示。O=O键键能为_______ kJ·mol-1,Mg原子的第一电离能为_______ kJ·mol-1。
(2)已知共价键的键能:Cl-Cl:243 kJ·mol-1,Si-Si:176 kJ·mol-1,Si-Cl:360 kJ·mol-1,则反应Si(s)+2Cl2(g)=SiCl4(g) △H=_______ kJ·mol-1
(3)元素的化合价与元素的电负性、原子所处的具体的化学环境紧密相关。如:有机化合物CH3I发生水解时的反应为:CHЗI+H2O→CHЗOH+HI,已知有机化合物CFЗI中I为+1价,请写出CF3I发生水解反应的化学方程式:_______ 。
(1)MgO的Born-Haber循环如图所示。O=O键键能为

(2)已知共价键的键能:Cl-Cl:243 kJ·mol-1,Si-Si:176 kJ·mol-1,Si-Cl:360 kJ·mol-1,则反应Si(s)+2Cl2(g)=SiCl4(g) △H=
(3)元素的化合价与元素的电负性、原子所处的具体的化学环境紧密相关。如:有机化合物CH3I发生水解时的反应为:CHЗI+H2O→CHЗOH+HI,已知有机化合物CFЗI中I为+1价,请写出CF3I发生水解反应的化学方程式:
您最近一年使用:0次
解题方法
8 . O、S、Cl、Fe、Cu五种元素的单质及其化合物在工农业生产和生活中有着广泛的应用。请回答下列问题:
(1)基态Fe原子价电子的轨道表示式为_______ 。
(2)O、S、Cl的电负性由大到小的顺序是_______ (填元素符号)。
(3)O、S的最简单氢化物中键角较大的是_______ (填化学式),原因是_______ 。
(4) 的空间结构为
的空间结构为_______ 。
(5)O、Cu组成的一种化合物的晶胞结构示意图如下。
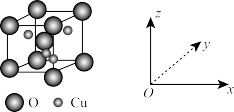
则该化合物的化学式为_______ 。
(1)基态Fe原子价电子的轨道表示式为
(2)O、S、Cl的电负性由大到小的顺序是
(3)O、S的最简单氢化物中键角较大的是
(4)
 的空间结构为
的空间结构为(5)O、Cu组成的一种化合物的晶胞结构示意图如下。

则该化合物的化学式为
您最近一年使用:0次
解题方法
9 . 第三代半导体中,碳化硅(SiC)和氮化镓(GaN)是核心半导体。它们具有更宽的禁带宽度、更高的导热率、更高的抗辐射能力、更大的电子饱和漂移速率等特性。
(1)基态Ga原子的价电子排布式为_______ 。
(2)晶体硅、碳化硅、金刚石三种晶体的熔点由高到低的顺序为_______ 。
(3)氮化镓不存在于自然界中,只能通过人工合成来制备,反应为 。
。
①GaCl3熔点为77.9℃,其晶体类型为_______ 。GaF3的熔点为1000℃,则将GaF3熔化时,被破坏的作用力是_______ 。
②上述反应涉及的元素中,电负性最小的是_______ (填元素符号,下同),第一电离能最大的是_______ 。
(1)基态Ga原子的价电子排布式为
(2)晶体硅、碳化硅、金刚石三种晶体的熔点由高到低的顺序为
(3)氮化镓不存在于自然界中,只能通过人工合成来制备,反应为
 。
。①GaCl3熔点为77.9℃,其晶体类型为
②上述反应涉及的元素中,电负性最小的是
您最近一年使用:0次
10 . 下列各项叙述中,正确的是
| A.d区中,族序数最大、原子序数最小的元素,它+3价离子比+2价离子稳定 |
| B.最外层电子数为ns2的原子,其价电子数也为2 |
| C.第一电离能越大,元素的电负性也越大 |
| D.“电子云”中的小黑点是电子在核外某空间内出现过的痕迹 |
您最近一年使用:0次
2022-04-25更新
|
129次组卷
|
2卷引用:福建省福州市八县(市)一中2021-2022学年高二下学期期中联考化学试题



