名校
解题方法
1 . 主族元素N、F、Si、As、Se、Cl等的某些化合物对工农业生产意义重大,回答下列问题:
(1)Si3N4陶瓷是世界上最坚硬的物质之一,具有高强度、低密度、耐高温等性质,其属于_______ 晶体;SiCl4中Si采取的杂化类型为_______ 。
(2)O、F、Cl电负性由大到小的顺序为_______ ;OF2分子的空间构型为_______ ;OF2的熔、沸点低于Cl2O,原因是_______ 。
(3)Se元素基态原子的原子核外电子排布式为_______ ;As的第一电离能比Se的第一电离能大的原因为_______ 。
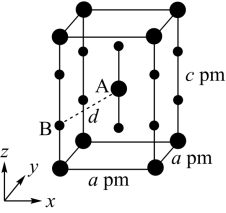
(4)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有_______ 个XeF2分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为( ,
, ,
, )。已知Xe-F键长为rpm,则B点原子的分数坐标为
)。已知Xe-F键长为rpm,则B点原子的分数坐标为_______ ;晶胞中A、B间距离d=_______ pm。
(1)Si3N4陶瓷是世界上最坚硬的物质之一,具有高强度、低密度、耐高温等性质,其属于
(2)O、F、Cl电负性由大到小的顺序为
(3)Se元素基态原子的原子核外电子排布式为
(4)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有
 ,
, ,
, )。已知Xe-F键长为rpm,则B点原子的分数坐标为
)。已知Xe-F键长为rpm,则B点原子的分数坐标为
您最近一年使用:0次
2022-05-02更新
|
863次组卷
|
7卷引用:陕西省汉中市2022届高三教学质量第二次检测考试理科综合能力测试化学试题
陕西省汉中市2022届高三教学质量第二次检测考试理科综合能力测试化学试题(已下线)专项17 物质结构与性质综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)(已下线)专题18物质结构与性质(选修)-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题17物质结构与性质(综合题)-2022年高考真题+模拟题汇编(全国卷)(已下线)专题18物质结构与性质(选修)-五年(2018~2022)高考真题汇编(全国卷)四川省绵阳南山中学2022-2023学年高三上学期入学考试理综化学试题山东省枣庄市第三中学2022-2023学年高三上学期期中考试化学试题
2 . 我国科学家预测全固态氟离子电池(CsPb1-xKxF3-x)可能替代锂离子电池。回答下列问题:
(1)基态K原子核外电子云轮廓图呈球形的能级上占据电子总数为_______ 。基态氟离子的电子排布式为_______ 。
(2)常见的含氟分子有HF、SiF4、OF2.其中,属于非极性分子的有_______ (填化学式),氟的电负性大于氯,但是HF的酸性比HCl的弱,其主要原因是_______ (提示:从分子间作用力角度分析)。
(3)我国科学家研究发现,在锂/氟化石墨电池中添加BF3,会提高能量转化效率。放电时,发生反应为LiF(s)+BF3(g)=LiBF4(aq),BF 的空间结构为
的空间结构为_______ ,上述反应中B原子的杂化类型变化为_______ 。
(4)CsF、KF的熔点分别为682℃、858℃,其熔点差异的主要原因是_______ 。
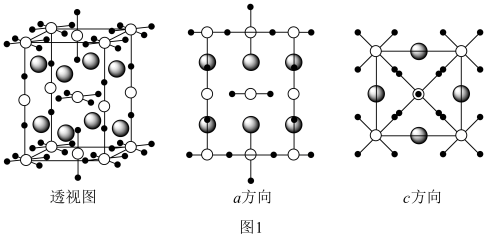
(5)铯、金、氯组成一种晶体,已知金元素有+1、+3价,它的晶胞如图1所示。大灰球为Cs,小黑球为Cl,其余球为Au。该晶体的化学式为_______ ,其中金原子有2种不同的化学环境,形成2种不同的离子,它们是_______ 和_______ 。
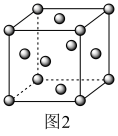
(6)铅单质的面心立方最密晶胞如图2所示。它的晶胞空隙率为_______ (用含π的式子表示;提示:晶胞空隙率=1-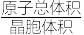 )。
)。
(1)基态K原子核外电子云轮廓图呈球形的能级上占据电子总数为
(2)常见的含氟分子有HF、SiF4、OF2.其中,属于非极性分子的有
(3)我国科学家研究发现,在锂/氟化石墨电池中添加BF3,会提高能量转化效率。放电时,发生反应为LiF(s)+BF3(g)=LiBF4(aq),BF
 的空间结构为
的空间结构为(4)CsF、KF的熔点分别为682℃、858℃,其熔点差异的主要原因是
(5)铯、金、氯组成一种晶体,已知金元素有+1、+3价,它的晶胞如图1所示。大灰球为Cs,小黑球为Cl,其余球为Au。该晶体的化学式为

(6)铅单质的面心立方最密晶胞如图2所示。它的晶胞空隙率为
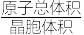 )。
)。
您最近一年使用:0次
名校
3 . 铝离子电池能量密度高、成本低且安全性高,是有前景的下一代储能电池。铝离子电池一般采用离子液体作为电解质,几种离子液体的结构如下。
(1)基态铝原子的核外电子排布式为___________ 。
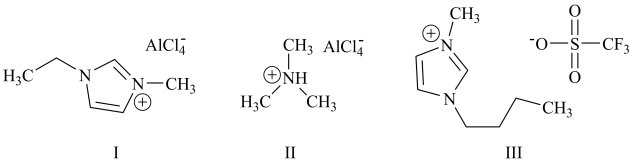
(2)基态氮原子的价层电子排布图为___________(填编号)。
(3)化合物I中碳原子的杂化轨道类型为___________ ,化合物II中阳离子的空间构型为___________ 。
(4)化合物III中O、F、S电负性由大到小的顺序为___________ 。
(5)传统的有机溶剂大多易挥发,而离子液体有相对难挥发的优点,原因是___________ 。
(6)铝离子电池的其中一种正极材料为AlMn2O4,其晶胞中铝原子的骨架如图所示。___________ 。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,如图中原子1的坐标为( ,
, ,
, ),原子2的坐标为(
),原子2的坐标为( ,
, ,
, ),则原子3的坐标为
),则原子3的坐标为_____ 。
③已知该晶体属于立方晶系,晶胞参数为apm,阿伏加德罗常数的值为NA,则晶体的密度为______ g·cm-3(列出计算式)。
(1)基态铝原子的核外电子排布式为
(2)基态氮原子的价层电子排布图为___________(填编号)。
A.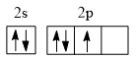 | B.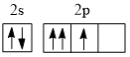 | C.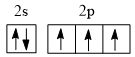 | D.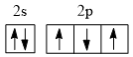 |
(4)化合物III中O、F、S电负性由大到小的顺序为
(5)传统的有机溶剂大多易挥发,而离子液体有相对难挥发的优点,原因是
(6)铝离子电池的其中一种正极材料为AlMn2O4,其晶胞中铝原子的骨架如图所示。
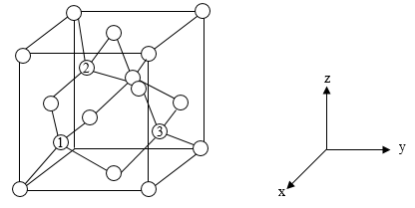
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,如图中原子1的坐标为(
 ,
, ,
, ),原子2的坐标为(
),原子2的坐标为( ,
, ,
, ),则原子3的坐标为
),则原子3的坐标为③已知该晶体属于立方晶系,晶胞参数为apm,阿伏加德罗常数的值为NA,则晶体的密度为
您最近一年使用:0次
2022-03-17更新
|
2774次组卷
|
10卷引用:广东省广州市2022届高三一模考试化学试题
广东省广州市2022届高三一模考试化学试题(已下线)必刷卷01-2022年高考化学考前信息必刷卷(全国乙卷)江西省新余市2022届高三第二次模拟考试理综化学试题吉林省长春市吉林省实验中学2022届高三最后一次模拟考试理综化学试题广东省广州市2021-2022学年高三下学期一模考试化学试题2024届四川省兴文第二中学校高三上学期一诊模拟考试理综试题(已下线)回归教材重难点11 物质结构与性质(选考)-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)广东省广州市2022届高三一模考试(结构与性质)(已下线)热点25 物质结构与性质综合题广东省广州市第六中学2023-2024学年高二下学期期中考试化学试题
4 . 中国较早时期就有炼铜、炼锌技术的记录,铜、锌元素也是人体必需的微量元素之一。回答下列问题:
(1)基态Cu原子核外的最高能层符号是___ ,基态Zn价电子排布式为___ 。
(2)硫酸铜溶于氨水形成[Cu(NH3)4]SO4溶液,组成[Cu(NH3)4]SO4的元素中,除Cu外其余元素的电负性由大到小排序为___ 。
(3)向[Cu(NH3)4]SO4溶液中逐滴滴加NaOH溶液,未出现浑浊,其原因是___ 。
(4)ZnO与ZnS结构相似,ZnO的熔点为1975℃,ZnS的熔点约为1700℃。ZnO熔点比ZnS高的原因是___ 。
(5)[Zn(CN)4]2-发生反应:4HCHO+[Zn(CN)4]2-+4H++4H2O=[Zn(H2O)4]2++4HOCH2CN
①HOCH2CN分子中碳原子轨道的杂化类型是___ 。
②与H2O分子互为等电子体的阴离子为___ 。
③[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为___ 。
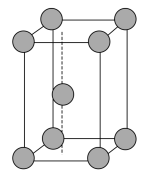
(6)金属锌晶体的晶胞如图所示,若锌原子的半径为rnm,则金属锌晶体的空间利用率是___ (用含π的代数式表示)。
(1)基态Cu原子核外的最高能层符号是
(2)硫酸铜溶于氨水形成[Cu(NH3)4]SO4溶液,组成[Cu(NH3)4]SO4的元素中,除Cu外其余元素的电负性由大到小排序为
(3)向[Cu(NH3)4]SO4溶液中逐滴滴加NaOH溶液,未出现浑浊,其原因是
(4)ZnO与ZnS结构相似,ZnO的熔点为1975℃,ZnS的熔点约为1700℃。ZnO熔点比ZnS高的原因是
(5)[Zn(CN)4]2-发生反应:4HCHO+[Zn(CN)4]2-+4H++4H2O=[Zn(H2O)4]2++4HOCH2CN
①HOCH2CN分子中碳原子轨道的杂化类型是
②与H2O分子互为等电子体的阴离子为
③[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为
(6)金属锌晶体的晶胞如图所示,若锌原子的半径为rnm,则金属锌晶体的空间利用率是

您最近一年使用:0次
解题方法
5 . 磷及其化合物在工农业生产中都有重要作用。
(1)磷原子核外电子排布式为_______ 。
(2)羟基磷灰石[Ca5(PO4)3OH]是牙齿中的重要矿物质,其中羟基(-OH)中氧原子的杂化方式为_______ , 的空间构型为
的空间构型为_______ ,该化合物中所含元素电负性最大的是_______ 。
(3)磷化硼为立方晶系晶体,该晶胞中原子的分数坐标为:
B:(0,0,0);( ,
, ,0);(
,0);( ,0,
,0, );(0,
);(0, ,
, )……
)……
P:( ,
, ,
, );(
);( ,
, ,
, );(
);( ,
, ,
, );(
);( ,
, ,
, )……
)……
①请在图中画出磷化硼晶胞的俯视图_______ 。
②与每个磷原子紧邻的硼原子有_______ 个,与每个硼原子紧邻的硼原子有_______ 个。
(4)磷钇矿可提取稀土元素钇(Y),某磷钇矿的结构如图所示。该磷钇矿的化学式为_______ ,与 互为等电子体的阴离子有
互为等电子体的阴离子有_______ (写出一种离子符号)。已知晶胞参数a=0.69nm,c=0.60nm,阿伏加德罗常数的值为NA,则该磷钇矿的密度为_______ g·cm-3(列出计算式)。

(1)磷原子核外电子排布式为
(2)羟基磷灰石[Ca5(PO4)3OH]是牙齿中的重要矿物质,其中羟基(-OH)中氧原子的杂化方式为
 的空间构型为
的空间构型为(3)磷化硼为立方晶系晶体,该晶胞中原子的分数坐标为:
B:(0,0,0);(
 ,
, ,0);(
,0);( ,0,
,0, );(0,
);(0, ,
, )……
)……P:(
 ,
, ,
, );(
);( ,
, ,
, );(
);( ,
, ,
, );(
);( ,
, ,
, )……
)……①请在图中画出磷化硼晶胞的俯视图

②与每个磷原子紧邻的硼原子有
(4)磷钇矿可提取稀土元素钇(Y),某磷钇矿的结构如图所示。该磷钇矿的化学式为
 互为等电子体的阴离子有
互为等电子体的阴离子有
您最近一年使用:0次
2021-07-13更新
|
404次组卷
|
3卷引用:青海省西宁市大通回族土族自治县2021届高三下学期高考二模化学试题
青海省西宁市大通回族土族自治县2021届高三下学期高考二模化学试题湖南省长沙市宁乡市2022届高三下学期5月模拟考试化学试题(已下线)专题35 磷、砷及其化合物-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
真题
解题方法
6 . 硅、锗(Ge)及其化合物广泛应用于光电材料领域。回答下列问题:
(1)基态硅原子最外层的电子排布图为_______ ,晶体硅和碳化硅熔点较高的是_______ (填化学式);
(2)硅和卤素单质反应可以得到 ,
, 的熔沸点如下表:
的熔沸点如下表:
①0℃时, 、
、 、
、 、
、 呈液态的是
呈液态的是____ (填化学式),沸点依次升高的原因是_____ ,气态 分子的空间构型是
分子的空间构型是_______ ;
② 与N-甲基咪唑
与N-甲基咪唑 反应可以得到
反应可以得到 ,其结构如图所示:
,其结构如图所示:

N-甲基咪唑分子中碳原子的杂化轨道类型为_______ ,H、C、N的电负性由大到小的顺序为_______ ,1个 中含有
中含有_______ 个 键;
键;
(3)下图是 、
、 、
、 三种元素形成的某化合物的晶胞示意图。
三种元素形成的某化合物的晶胞示意图。
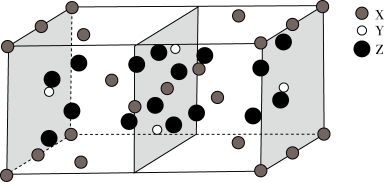
①已知化合物中 和
和 的原子个数比为1:4,图中Z表示
的原子个数比为1:4,图中Z表示_______ 原子(填元素符号),该化合物的化学式为_______ ;
②已知该晶胞的晶胞参数分别为anm、bnm、cnm, ,则该晶体的密度
,则该晶体的密度
_______  (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,用含a、b、c、
,用含a、b、c、 的代数式表示)。
的代数式表示)。
(1)基态硅原子最外层的电子排布图为
(2)硅和卤素单质反应可以得到
 ,
, 的熔沸点如下表:
的熔沸点如下表: |  |  |  | |
| 熔点/K | 183.0 | 203.2 | 278.6 | 393.7 |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
 、
、 、
、 、
、 呈液态的是
呈液态的是 分子的空间构型是
分子的空间构型是②
 与N-甲基咪唑
与N-甲基咪唑 反应可以得到
反应可以得到 ,其结构如图所示:
,其结构如图所示:
N-甲基咪唑分子中碳原子的杂化轨道类型为
 中含有
中含有 键;
键;(3)下图是
 、
、 、
、 三种元素形成的某化合物的晶胞示意图。
三种元素形成的某化合物的晶胞示意图。
①已知化合物中
 和
和 的原子个数比为1:4,图中Z表示
的原子个数比为1:4,图中Z表示②已知该晶胞的晶胞参数分别为anm、bnm、cnm,
 ,则该晶体的密度
,则该晶体的密度
 (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,用含a、b、c、
,用含a、b、c、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2021-06-09更新
|
8961次组卷
|
14卷引用:2021年湖南省高考化学试卷变式题11-19
2021年湖南省高考化学试卷变式题11-192021年新高考湖南化学高考真题(已下线)专题14 物质结构与性质-备战2022年高考化学学霸纠错(全国通用)(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题19 物质结构与性质-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题13 物质结构与性质—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)回归教材重难点11 物质结构与性质-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)押新高考卷15题 物质结构与性质综合题-备战2022年高考化学临考题号押题(新高考通版)(已下线)专题18 物质结构与性质(综合题)-三年(2020-2022)高考真题分项汇编山东省菏泽市单县第二中学2021-2022学年高二3月月考化学试题(已下线)第五章 物质结构与性质 元素周期律 第32讲 物质结构与性质综合题研究(已下线)专题20 结构与性质(已下线)专题20 结构与性质(已下线)专题16 物质结构与性质综合题-2023年高考化学真题题源解密(全国通用)
7 . C、S、Cr、Cu及其化合物在化工、材料等方面应用十分广泛。回答下列问题:
(1)二甲基亚砜(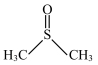 )所含元素的电负性由大到小的顺序为
)所含元素的电负性由大到小的顺序为_______ 。所含碳原子和硫原子的杂化类型分别为_______ 、_______ 。
(2)25℃时,顺-丁烯二酸( )和反-丁烯二酸(
)和反-丁烯二酸(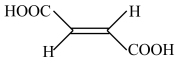 )的电离平衡常数如下表。
)的电离平衡常数如下表。
结合氢键,分析顺-丁烯二酸的K1明显大于反-丁烯二酸的原因是_______ 。
(3)元素Cr位于元素周期表中_______ 区,其基态原子次外层电子数目为_______ 个,其基态原子价层电子的空间运动状态有_______ 种。
(4)某晶体晶胞结构如图所示,其中Cu均匀分散在立方体内,NA为阿伏加德罗常数的值。

①该化合物中铜粒子的价电子排布式为_______ ,a、b氧粒子的坐标参数依次为(0,0,0)、( ,
, ,
, ),则d点粒子的坐标参数为
),则d点粒子的坐标参数为_______ 。
②若a、b间的距离=xcm,计算该晶胞的密度_______ g/cm3(写表达式)。
(1)二甲基亚砜(
 )所含元素的电负性由大到小的顺序为
)所含元素的电负性由大到小的顺序为(2)25℃时,顺-丁烯二酸(
 )和反-丁烯二酸(
)和反-丁烯二酸( )的电离平衡常数如下表。
)的电离平衡常数如下表。| 物质 | 电离平衡常数 | |
| 顺-丁烯二酸 | K1=1.17×10-2 | K2=2.6×10-7 |
| 反-丁烯二酸 | K1=9.3×10-4 | K2=2.9×10-5 |
(3)元素Cr位于元素周期表中
(4)某晶体晶胞结构如图所示,其中Cu均匀分散在立方体内,NA为阿伏加德罗常数的值。

①该化合物中铜粒子的价电子排布式为
 ,
, ,
, ),则d点粒子的坐标参数为
),则d点粒子的坐标参数为②若a、b间的距离=xcm,计算该晶胞的密度
您最近一年使用:0次
解题方法
8 . 2020年某科研团队经多次实验发现一种新型漂白剂(结构见下图),可用于漂白蚕丝等织品,其组成元素均为短周期元素,W、X对应的简单离子核外电子排布相同,且W、Y、Z的最外层电子数之和等于X的最外层电子数,下列说法错误的是


| A.四种元素中X的电负性最大 |
| B.该物质中含有2mol配位键 |
| C.Y的最高价氧化物的水化物是一元弱酸 |
| D.离子半径:Z+˂W2+<X2- |
您最近一年使用:0次
解题方法
9 . 卤族元素是重要的非金属元素,用途广泛。回答下列问题:
(1)卤族元素位于元素周期表___________ 区,其中电负性最大的是___________ (填元素符号)。
(2)基态氟原子核外有___________ 种运动状态不同的电子,其中含有单电子的轨道形状为___________ 。
(3)溴元素对应的含氧酸 HBrO4酸性比 HBrO3酸性___________ (填“强”或“弱”),原因是___________ 。
(4)化合物 I3 AsF6为离子化合物,其中阳离子(I )中心原子的杂化方式为
)中心原子的杂化方式为___________ 。该晶体中不含有的化学键类型为___________ (填选项字母)。
a.配位键 b.金属键 c.极性键 d.非极性键
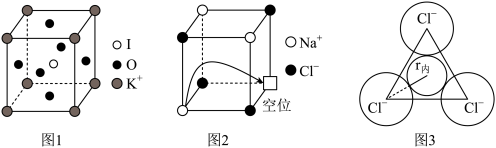
(5)由钾、氧、碘三种元素构成的晶体晶胞结构如图1所示。则该晶体的化学式为___________ ,晶胞中位置与 K+紧邻的 O 的个数为___________ 。
(6)有“点缺陷”的 NaCl 晶体可导电,其结构如图 2 所示。有人认为:高温下有“点缺陷”的 NaCl 晶体能导电,是因为 Na+经过一个由 3 个 Cl-组成的最小三角形窗孔(如图 3 所示),迁移到另一空位而造成的。已知立方体边长 a=282pm,粒子半径 r(Na+)=115pm,r(Cl-)=167pm,计算内切圆半径 r内的值并判断该观点是否正确___________ 。(已知: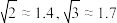 )
)
(1)卤族元素位于元素周期表
(2)基态氟原子核外有
(3)溴元素对应的含氧酸 HBrO4酸性比 HBrO3酸性
(4)化合物 I3 AsF6为离子化合物,其中阳离子(I
 )中心原子的杂化方式为
)中心原子的杂化方式为a.配位键 b.金属键 c.极性键 d.非极性键
(5)由钾、氧、碘三种元素构成的晶体晶胞结构如图1所示。则该晶体的化学式为

(6)有“点缺陷”的 NaCl 晶体可导电,其结构如图 2 所示。有人认为:高温下有“点缺陷”的 NaCl 晶体能导电,是因为 Na+经过一个由 3 个 Cl-组成的最小三角形窗孔(如图 3 所示),迁移到另一空位而造成的。已知立方体边长 a=282pm,粒子半径 r(Na+)=115pm,r(Cl-)=167pm,计算内切圆半径 r内的值并判断该观点是否正确
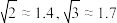 )
)
您最近一年使用:0次
解题方法
10 . Ⅰ.SiC、BN、GaAs 等是人工合成半导体的材料,具有高频、大功率和抗辐射等优点。请回答:
(1)Ga的第一电离能失去的是___________ 能级的电子。
(2)B、C、N的电负性由大到小排列为___________ 。
Ⅱ.卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(3)拟卤素(CN)2、(SCN)2与卤素单质结构相似、性质相近,分子中所有原子都满足8 电子结构。(SCN)2对应的酸有两种,测得硫氰酸(H—S—C≡N )的沸点低于异硫氰酸(H-N=C=S),其原因是___________ 。
(4)卤化物 RbICl2 在加热时会分解为晶格能相对较大的卤化物 A 和卤素互化物或卤素单质,A 的化学式为___________ ;I 属于多卤素阳离子,其空间构型为
属于多卤素阳离子,其空间构型为___________ 。
(5)卤素互化物如IBr、ICl等与卤素单质结构和性质相似。Cl2、IBr、ICl沸点由高到低的顺序为___________ 。
(6)请推测①HClO4、②HIO4、③H5IO6[可写成(HO)5IO]三种物质的酸性由强到弱的顺序为___________ (填序号)。
III.金属铁是生活中最常见的金属,其晶胞为体心立方堆积。
(7)其晶胞的俯视图为____ (填字母序号)。
(8)若铁的密度为a g/cm3,则铁晶胞中最近的两个铁原子的核间距离是____ pm(列表达式即可)。
(1)Ga的第一电离能失去的是
(2)B、C、N的电负性由大到小排列为
Ⅱ.卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(3)拟卤素(CN)2、(SCN)2与卤素单质结构相似、性质相近,分子中所有原子都满足8 电子结构。(SCN)2对应的酸有两种,测得硫氰酸(H—S—C≡N )的沸点低于异硫氰酸(H-N=C=S),其原因是
(4)卤化物 RbICl2 在加热时会分解为晶格能相对较大的卤化物 A 和卤素互化物或卤素单质,A 的化学式为
 属于多卤素阳离子,其空间构型为
属于多卤素阳离子,其空间构型为(5)卤素互化物如IBr、ICl等与卤素单质结构和性质相似。Cl2、IBr、ICl沸点由高到低的顺序为
(6)请推测①HClO4、②HIO4、③H5IO6[可写成(HO)5IO]三种物质的酸性由强到弱的顺序为
III.金属铁是生活中最常见的金属,其晶胞为体心立方堆积。
(7)其晶胞的俯视图为____ (填字母序号)。
A. | B. | C.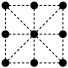 | D. |
您最近一年使用:0次
2021-05-07更新
|
479次组卷
|
3卷引用:吉林省吉林市普通中学2021届高三下学期第四次调研测试理综化学试题
吉林省吉林市普通中学2021届高三下学期第四次调研测试理综化学试题河南省名校联盟2022届高三下学期第一次模拟理科综合化学试题(已下线)押全国卷理综第35题 物质结构与性质-备战2021年高考化学临考题号押题



