名校
解题方法
1 . 原子序数小于等于36的Q、W、X、Y、Z五种元素,其中Q是形成化合物种类最多的元素,W和Y的基态原子2p能级所含成单电子数均为2,Z的基态原子核外含有13种运动状态不同的电子。回答下列问题(涉及元素时用对应的元素符号表示):
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是______ 。
(2)1molQWX与1molWQ2Y所含σ键的比值为______ 。
(3)根据等电子体理论可以预测WXY-的空间构型为______ 。
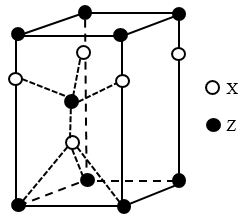
(4)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为______ 。
(5)实验室合成一种由W和X两种元素形成的化合物,该化合物具有空间网状结构,其中每个W原子与4个X原子形成共价键,每个X原子与3个W原子形成共价键。
①该化合物的化学式为。______ 。
②该化合物所属晶体类型为______ 晶体,预测其熔点应______ 金刚石(填“高于”或“低于”)。
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是
(2)1molQWX与1molWQ2Y所含σ键的比值为
(3)根据等电子体理论可以预测WXY-的空间构型为
(4)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为

(5)实验室合成一种由W和X两种元素形成的化合物,该化合物具有空间网状结构,其中每个W原子与4个X原子形成共价键,每个X原子与3个W原子形成共价键。
①该化合物的化学式为。
②该化合物所属晶体类型为
您最近一年使用:0次
2021-03-14更新
|
325次组卷
|
3卷引用:江苏省如皋中学2020届高三阶段检测化学试题
名校
解题方法
2 . 下表为长式周期表的一部分其中的编号代表对应的元素。
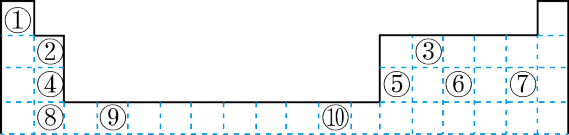
请回答下列问题:
(1)表中属于 ds 区的元素是___________ (填元素符号)它的基态原子的价电子排布式为___________ 。
(2)表中元素①的 6 个原子与元素③的 6 个原子形成的某种平面环状分子其分子式为___________ ,其中元素③的基态原子的电子排布图为_______ ;①和⑥形成的一种常见四原子分子的化学式为_______ ,该分子的立体构型为______ 。
(3)某元素原子的价电子排布式为 nsnnpn+1,该元素原子的电子层上未成对电子数为___________ ;该元素与元素①形成的最简单分子 X 的电子式为___________ 。
(4)元素⑤的电负性___________ ④元素的电负性(选填>、=、<下同);元素⑥的第一电离能___________ 原子序数为 16 的元素的第一电离能。
(5)用电子式表示元素④和⑦组成的化合物的形成过程___________ 。

请回答下列问题:
(1)表中属于 ds 区的元素是
(2)表中元素①的 6 个原子与元素③的 6 个原子形成的某种平面环状分子其分子式为
(3)某元素原子的价电子排布式为 nsnnpn+1,该元素原子的电子层上未成对电子数为
(4)元素⑤的电负性
(5)用电子式表示元素④和⑦组成的化合物的形成过程
您最近一年使用:0次
名校
解题方法
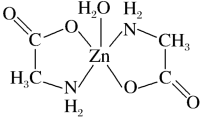
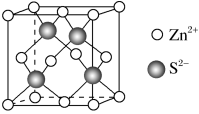
3 . 一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图。 的价电子排布式为
的价电子排布式为_______ ;一水合甘氨酸锌中所涉及的非金属元素电负性由大到小的顺序是_______ 。
(2)甘氨酸(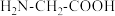 )中N的杂化轨道类型为
)中N的杂化轨道类型为_______ ;甘氨酸易溶于水,试从结构角度解释_______ 。
(3)一水合甘氨酸锌中 的配位数为
的配位数为_______ 。 填入
填入 组成
组成_______ 空隙中;
②由①能否判断出 、
、 相切?
相切?_______ (填“能”或“否”);
③已知晶体密度为 ,
, 半径为a pm,若要使
半径为a pm,若要使 、
、 相切,则
相切,则 半径为
半径为_______ pm(写计算表达式)。
 的价电子排布式为
的价电子排布式为(2)甘氨酸(
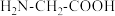 )中N的杂化轨道类型为
)中N的杂化轨道类型为(3)一水合甘氨酸锌中
 的配位数为
的配位数为(4) 是
是 的另一种配合物,IMI的结构为
的另一种配合物,IMI的结构为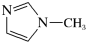 ,常温下IMI的某种衍生物与甘氨酸形成的离子化合物
,常温下IMI的某种衍生物与甘氨酸形成的离子化合物 为液态而非固态。原因是
为液态而非固态。原因是
 填入
填入 组成
组成②由①能否判断出
 、
、 相切?
相切?③已知晶体密度为
 ,
, 半径为a pm,若要使
半径为a pm,若要使 、
、 相切,则
相切,则 半径为
半径为
您最近一年使用:0次
2021-01-03更新
|
379次组卷
|
6卷引用:四川省成都市2020届高三第一次诊断性检测理综化学试题
名校
解题方法
4 . 一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图所示:
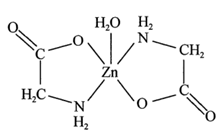
(1)基态 核外价电子排布图为
核外价电子排布图为___________ ;一水合甘氨酸锌中所涉及的非金属元素电负性由大到小的排列顺序为___________ 。
(2)甘氨酸(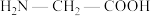 )的羧基中C原子的杂化轨道类型为
)的羧基中C原子的杂化轨道类型为___________ ;甘氨酸易溶于水,试从结构角度解释:___________ 。
(3)以氧化锌矿物为原料,提取锌的过程中涉及反应: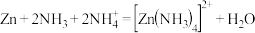 。与
。与 互为等电子体的阴离子为
互为等电子体的阴离子为___________ (写出1种即可);
(4).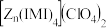 是
是 的另一种配合物,
的另一种配合物, 的结构为
的结构为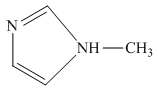 ,则
,则 中含有
中含有___________ 个 键;常温下
键;常温下 的某种衍生物与甘氨酸形成的离子化合物
的某种衍生物与甘氨酸形成的离子化合物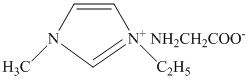 为液态而非固态,其原因是
为液态而非固态,其原因是___________ 。
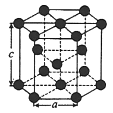
(5)金属 晶体中的原子堆积方式如图所示,这种堆积方式称为
晶体中的原子堆积方式如图所示,这种堆积方式称为___________ ;六棱柱底边边长为 ,高为
,高为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 的密度为
的密度为___________  (列出算式即可)。
(列出算式即可)。

(1)基态
 核外价电子排布图为
核外价电子排布图为(2)甘氨酸(
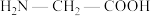 )的羧基中C原子的杂化轨道类型为
)的羧基中C原子的杂化轨道类型为(3)以氧化锌矿物为原料,提取锌的过程中涉及反应:
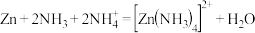 。与
。与 互为等电子体的阴离子为
互为等电子体的阴离子为(4).
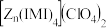 是
是 的另一种配合物,
的另一种配合物, 的结构为
的结构为 ,则
,则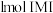 中含有
中含有 键;常温下
键;常温下 的某种衍生物与甘氨酸形成的离子化合物
的某种衍生物与甘氨酸形成的离子化合物 为液态而非固态,其原因是
为液态而非固态,其原因是(5)金属
 晶体中的原子堆积方式如图所示,这种堆积方式称为
晶体中的原子堆积方式如图所示,这种堆积方式称为 ,高为
,高为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 的密度为
的密度为 (列出算式即可)。
(列出算式即可)。
您最近一年使用:0次
名校
解题方法
5 . 镁、铝、铁、铜及其化合物在生产生活中具有广泛的应用。
(1)基态铝原子核外电子占据的最高能级符号为____ ,该能级原子轨道数为____ ,电子云轮廓图为_____ ;基态铁原子价层电子未成对电子数为_____ 。
(2)第一电离能镁_____ 铝(填>、<、=)
(3)CuSO4·5H2O俗名胆矾矾,可用于配制农药和游泳池消毒,其组成可表示为[Cu(H2O)4]SO4·H2O。晶体中含有的化学键类型为_______
a.离子键 b.共价键 c.配位键 d.氢键 e.金属键
(4)FeSO4·7H2O俗称绿矾,在空气中加热分解可能得到Fe2O3、H2O、SO2、SO3等,其中CuO的熔点为1026℃。
①H2O分子中氧原子的杂化类型是______ ,分子的立体构型是_____ 。组成绿矾的元素中电负性最大的元素是______ ,
②CuO的晶体类型是_____ 。
③SO2与SO3中,属于非极性分子的是______ ,SO2在溶剂水与溶剂CCl4中,相同温度能溶解更多SO2的溶剂是________
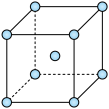
④铁的晶胞结构如图,若晶胞参数为acm,阿伏加德罗常数值为NA,则晶体的密度为___________ g/cm3。
(1)基态铝原子核外电子占据的最高能级符号为
(2)第一电离能镁
(3)CuSO4·5H2O俗名胆矾矾,可用于配制农药和游泳池消毒,其组成可表示为[Cu(H2O)4]SO4·H2O。晶体中含有的化学键类型为
a.离子键 b.共价键 c.配位键 d.氢键 e.金属键
(4)FeSO4·7H2O俗称绿矾,在空气中加热分解可能得到Fe2O3、H2O、SO2、SO3等,其中CuO的熔点为1026℃。
①H2O分子中氧原子的杂化类型是
②CuO的晶体类型是
③SO2与SO3中,属于非极性分子的是
④铁的晶胞结构如图,若晶胞参数为acm,阿伏加德罗常数值为NA,则晶体的密度为

您最近一年使用:0次
名校
解题方法
6 . C、Si在元素周期表中属于同主族元素,其常见的氧化物分别为CO2、SiO2。请回答下列问题:
(1)锗与碳、硅同主族,写出锗原子基态时的核外电子排布式:____________ 。
(2)C、O、Si三种元素的电负性由大到小的顺序为____________ (用元素符号表示)。
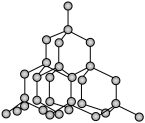
(3)二氧化硅结构跟硅晶体结构相似,即二氧化硅的结构相当于在硅晶体结构中每个硅与硅的化学键之间插入一个O原子。观察下图中硅晶体的结构,分析二氧化硅的空间网状结构中,Si、O原子形成的最小环上O原子的数目为____________ ;晶体硅中硅原子与共价键的数目比为____________ 。
(4)下图是二氧化碳的晶胞模型,从晶体类型来看,CO2属于_______ 晶体。图中显示出的二氧化碳分子数有________ 个,实际上一个二氧化碳晶胞中含有_______ 个二氧化碳分子。标准状况下2.24 L的CO2分子中含有的π键的数目为______ 。
(5)在二氧化碳晶胞中,最近的两个二氧化碳分子间的距离为a nm,NA为阿伏加 德罗常数的值,则晶体密度为____________ g·cm-3。
(1)锗与碳、硅同主族,写出锗原子基态时的核外电子排布式:
(2)C、O、Si三种元素的电负性由大到小的顺序为
(3)二氧化硅结构跟硅晶体结构相似,即二氧化硅的结构相当于在硅晶体结构中每个硅与硅的化学键之间插入一个O原子。观察下图中硅晶体的结构,分析二氧化硅的空间网状结构中,Si、O原子形成的最小环上O原子的数目为
(4)下图是二氧化碳的晶胞模型,从晶体类型来看,CO2属于
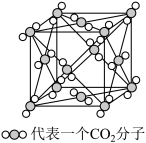
(5)在二氧化碳晶胞中,最近的两个二氧化碳分子间的距离为a nm,NA为阿伏加 德罗常数的值,则晶体密度为
您最近一年使用:0次
2020-09-22更新
|
342次组卷
|
3卷引用:辽宁省朝阳市建平县2021届高三9月联考化学试题
名校
解题方法
7 . 硼及其化合物广泛应用于高新材料领域,请回答下列有关问题:
(1)NaBH4是一种重要的储氢载体,其中涉及元素的电负性由大到小的顺序为______ 。
(2)硼氮苯被称为无机苯,其结构如图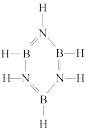 ,分子中氮原子的杂化方式是
,分子中氮原子的杂化方式是___________ 。已知硼氮苯分子在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“大π键”,该“大π键”可表示为__________ (用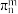 表示,其中n表示参与形成大π键的原子数,m表示形成大π键的电子数)。
表示,其中n表示参与形成大π键的原子数,m表示形成大π键的电子数)。
(3)硼酸(H3BO3)为白色片状晶体,有与石墨相似的层状结构,则硼酸晶体中存在的作用力有共价键、_______ 。
(4)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,主要结构有立方氮化硼(如图1)和六方氮化硼(如图2),前者类似于金刚石,后者与石墨相似。
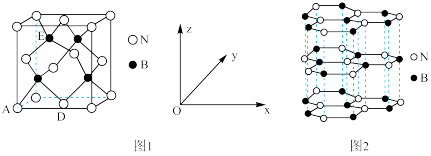
①晶胞中的原子坐标参数可表示晶胞内部各原子的相对位置。图1中原子坐标参数A为(0,0,0),D为( ,
, ,0),则E原子的坐标参数为
,0),则E原子的坐标参数为___________ 。X-射线衍射实验测得立方氮化硼晶胞边长为a pm,则立方氮化硼晶体中N与B的原子半径之和为________ pm(用含a的式子表示)。
②已知六方氮化硼同层中B-N距离为145 pm,层与层之间距离为333 pm,则晶体密度的计算式为_________ g·cm-3。(已知正六边形面积为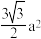 ,a为边长,NA表示阿伏加 德罗常数)
,a为边长,NA表示阿伏加 德罗常数)
(1)NaBH4是一种重要的储氢载体,其中涉及元素的电负性由大到小的顺序为
(2)硼氮苯被称为无机苯,其结构如图
 ,分子中氮原子的杂化方式是
,分子中氮原子的杂化方式是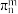 表示,其中n表示参与形成大π键的原子数,m表示形成大π键的电子数)。
表示,其中n表示参与形成大π键的原子数,m表示形成大π键的电子数)。(3)硼酸(H3BO3)为白色片状晶体,有与石墨相似的层状结构,则硼酸晶体中存在的作用力有共价键、
(4)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,主要结构有立方氮化硼(如图1)和六方氮化硼(如图2),前者类似于金刚石,后者与石墨相似。

①晶胞中的原子坐标参数可表示晶胞内部各原子的相对位置。图1中原子坐标参数A为(0,0,0),D为(
 ,
, ,0),则E原子的坐标参数为
,0),则E原子的坐标参数为②已知六方氮化硼同层中B-N距离为145 pm,层与层之间距离为333 pm,则晶体密度的计算式为
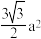 ,a为边长,NA表示阿伏加 德罗常数)
,a为边长,NA表示阿伏加 德罗常数)
您最近一年使用:0次
2020-08-03更新
|
287次组卷
|
3卷引用:山东省菏泽市2019-2020学年高二下学期期中考试化学试题(B)
名校
解题方法
8 . 复合氢化物可作为储氢和固体电解质材料,在能源与材料领域得到了广泛而深入的研究。
(1)复合氢化物升温加热可逐步分解放出氢气,理论上单位质量的下列复合氢化物其储氢能力由高到低的顺序是_______________ (填标号)。
A.Mg(NH2)2 B.NaNH2 C.H3N-BH3 D.NaAlH4 E.Li3AlH6
(2)在Mg(NH2)2和NaNH2中均存在NH ,NH
,NH 的空间构型为
的空间构型为____________ ,中心原子的杂化方式为___________ 。
(3)2019年Rahm利用元素价电子的结合能重新计算各元素的电负性,短周期主族元素的Rahm电负性数值如下表所示:
①写出基态B原子的价电子轨道表达式:______________________ 。
②通过上表可以推测Rahm电负性小于___________________ 的元素为金属元素。
③结合上表数据写出H3N-BH3与水反应生成一种盐和H2的化学方程式____________________ 。
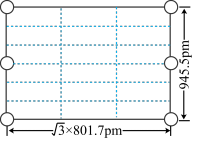
(4)Li3AlH6晶体的晶胞参数为a=b=801.7pm、c=945.5pm,α=β=90°、γ=120°,结构如图所示:

① 已知AlH 的分数坐标为(0,0,0)、
的分数坐标为(0,0,0)、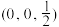 、
、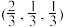 、
、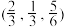 、
、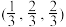 和,
和,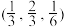 ,晶胞中Li+的个数为
,晶胞中Li+的个数为____________ 。
② 右图是上述Li3AlH6晶胞的某个截面,共含有10个AlH ,其中6个已经画出(图中的O),请在图中用O将剩余的AlH
,其中6个已经画出(图中的O),请在图中用O将剩余的AlH 画出
画出_________________ 。
③ 此晶体的密度为____________________________ g·cm-3(列出计算式,已知阿伏加 德罗常数约为6.02×1023mol-1)。
(1)复合氢化物升温加热可逐步分解放出氢气,理论上单位质量的下列复合氢化物其储氢能力由高到低的顺序是
A.Mg(NH2)2 B.NaNH2 C.H3N-BH3 D.NaAlH4 E.Li3AlH6
(2)在Mg(NH2)2和NaNH2中均存在NH
 ,NH
,NH 的空间构型为
的空间构型为(3)2019年Rahm利用元素价电子的结合能重新计算各元素的电负性,短周期主族元素的Rahm电负性数值如下表所示:
| 元素符号 | H | ||||||
| Rahm电负性 | 13.6 | ||||||
| 元素符号 | Li | Be | B | C | N | O | F |
| Rahm电负性 | 5.4 | 9.3 | 11.4 | 13.9 | 16.9 | 18.6 | 23.3 |
| 元素符号 | Na | Mg | Al | Si | P | S | Cl |
| Rahm电负性 | 5.1 | 7.6 | 9.1 | 10.8 | 12.8 | 13.6 | 16.3 |
①写出基态B原子的价电子轨道表达式:
②通过上表可以推测Rahm电负性小于
③结合上表数据写出H3N-BH3与水反应生成一种盐和H2的化学方程式
(4)Li3AlH6晶体的晶胞参数为a=b=801.7pm、c=945.5pm,α=β=90°、γ=120°,结构如图所示:


① 已知AlH
 的分数坐标为(0,0,0)、
的分数坐标为(0,0,0)、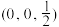 、
、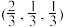 、
、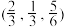 、
、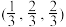 和,
和,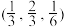 ,晶胞中Li+的个数为
,晶胞中Li+的个数为② 右图是上述Li3AlH6晶胞的某个截面,共含有10个AlH
 ,其中6个已经画出(图中的O),请在图中用O将剩余的AlH
,其中6个已经画出(图中的O),请在图中用O将剩余的AlH 画出
画出③ 此晶体的密度为
您最近一年使用:0次
名校
解题方法
9 . 元素X的基态原子中的电子共有7个能级,且最外层电子数为1,X原子的内层轨道全部排满电子.在气体分析中,常用XCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:2XCl+2CO+2H2O═X2Cl2•2CO•2H2O
(1)X基态原子的电子排布式为______ .
(2)C、H、O三种原子的电负性由大到小的顺序为______ .
(3)X2Cl2•2CO•2H2O是一种配合物,其结构如图1所示:
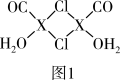
①与CO为互为等电子体的分子是______ .
②该配合物中氯原子的杂化方式为______ .
③在X2Cl2•2CO•2H2O中,每个X原子能与其他原子形成3个配位键,在图中用“→”标出相应的配位键______ .
(4)XCl的晶胞如2图所示,距离每个X+最近的Cl-的个数为______ .XCl的化学式__________

已知X的半径为apm,此晶胞的密度为dg/cm3,则阿伏加 德罗常数NA=_____________ (无需化简,列式即可)。
(1)X基态原子的电子排布式为
(2)C、H、O三种原子的电负性由大到小的顺序为
(3)X2Cl2•2CO•2H2O是一种配合物,其结构如图1所示:

①与CO为互为等电子体的分子是
②该配合物中氯原子的杂化方式为
③在X2Cl2•2CO•2H2O中,每个X原子能与其他原子形成3个配位键,在图中用“→”标出相应的配位键
(4)XCl的晶胞如2图所示,距离每个X+最近的Cl-的个数为

已知X的半径为apm,此晶胞的密度为dg/cm3,则阿伏加 德罗常数NA=
您最近一年使用:0次
解题方法
10 .  、
、 、
、 、
、 、
、 是元素周期表中前四周期的元素,各周期至少含有一种元素,且原子序数依次增大。
是元素周期表中前四周期的元素,各周期至少含有一种元素,且原子序数依次增大。 、
、 、
、 三种元素原子的最外层电子数相同,
三种元素原子的最外层电子数相同, 与
与 能够形成原子之比为
能够形成原子之比为 的化合物
的化合物 ,
, 是前四周期基态原子含有未成对电子数目最多的元素,
是前四周期基态原子含有未成对电子数目最多的元素, 与
与 形成的晶体
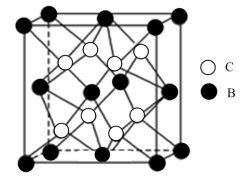
形成的晶体 结构如图所示。试用元素符号回答下列问题:
结构如图所示。试用元素符号回答下列问题:
(1) 、
、 、
、 三种元素的电负性由大到小的顺序为
三种元素的电负性由大到小的顺序为_______ 。
(2) 与
与 两种元素能够形成两种常见的化合物,则在这两种化合物分子中,原子的杂化方式分别为
两种元素能够形成两种常见的化合物,则在这两种化合物分子中,原子的杂化方式分别为______ 和______ ,且这两种分子____ (填选项)。
A 都是极性分子 B 都是非极性分子 C 其中一种是极性分子另一种是非极性分子
(3) 元素处于周期表的
元素处于周期表的____ 区,其单质晶体堆积模型的名称为_____ 。
(4) 元素的基态原子价层电子排布图为
元素的基态原子价层电子排布图为______ 。
(5)已知 能溶于某浓度的硝酸中,得到蓝色溶液的同时,会逸出一种与
能溶于某浓度的硝酸中,得到蓝色溶液的同时,会逸出一种与 互为等电子体的纯净气体,则该反应的化学方程式为
互为等电子体的纯净气体,则该反应的化学方程式为_____ 。经研究证实,所得溶液呈蓝色,是因为溶液中含有由 、
、 、
、 三种元素形成的一种配位离子,试写出该离子的结构式
三种元素形成的一种配位离子,试写出该离子的结构式______ 。
(6)由晶体 的晶胞可知,
的晶胞可知, 离子呈简单立方堆积模型,形成立方体空隙,则
离子呈简单立方堆积模型,形成立方体空隙,则 离子对这些立方体空隙的填充率为
离子对这些立方体空隙的填充率为_____  。
。
 、
、 、
、 、
、 、
、 是元素周期表中前四周期的元素,各周期至少含有一种元素,且原子序数依次增大。
是元素周期表中前四周期的元素,各周期至少含有一种元素,且原子序数依次增大。 、
、 、
、 三种元素原子的最外层电子数相同,
三种元素原子的最外层电子数相同, 与
与 能够形成原子之比为
能够形成原子之比为 的化合物
的化合物 ,
, 是前四周期基态原子含有未成对电子数目最多的元素,
是前四周期基态原子含有未成对电子数目最多的元素, 与
与 形成的晶体
形成的晶体 结构如图所示。试用元素符号回答下列问题:
结构如图所示。试用元素符号回答下列问题:
(1)
 、
、 、
、 三种元素的电负性由大到小的顺序为
三种元素的电负性由大到小的顺序为(2)
 与
与 两种元素能够形成两种常见的化合物,则在这两种化合物分子中,原子的杂化方式分别为
两种元素能够形成两种常见的化合物,则在这两种化合物分子中,原子的杂化方式分别为A 都是极性分子 B 都是非极性分子 C 其中一种是极性分子另一种是非极性分子
(3)
 元素处于周期表的
元素处于周期表的(4)
 元素的基态原子价层电子排布图为
元素的基态原子价层电子排布图为(5)已知
 能溶于某浓度的硝酸中,得到蓝色溶液的同时,会逸出一种与
能溶于某浓度的硝酸中,得到蓝色溶液的同时,会逸出一种与 互为等电子体的纯净气体,则该反应的化学方程式为
互为等电子体的纯净气体,则该反应的化学方程式为 、
、 、
、 三种元素形成的一种配位离子,试写出该离子的结构式
三种元素形成的一种配位离子,试写出该离子的结构式(6)由晶体
 的晶胞可知,
的晶胞可知, 离子呈简单立方堆积模型,形成立方体空隙,则
离子呈简单立方堆积模型,形成立方体空隙,则 离子对这些立方体空隙的填充率为
离子对这些立方体空隙的填充率为 。
。
您最近一年使用:0次



