名校
解题方法
1 . 卤素元素比较活泼,能形成种类繁多的化合物,回答下列问题:
(1)F,Cl,Br,I形成简单氢化物的沸点由高到低的顺序为:____________________________ 。
(2)卤素可形成很多酸根离子,如 、
、 、
、 、
、 等,
等, 的空间结构为
的空间结构为______________ 。
(3)卤素元素之间还能形成很多卤素互化物,如 ,
, ,
,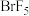 ,
,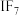 等,根据I与Cl原子的电负性大小关系写成
等,根据I与Cl原子的电负性大小关系写成 在水中水解的化学方程式:
在水中水解的化学方程式:_____________________ 。
(4)在石墨烯膜上可以制备Cl元素和Ca元素形成的新型的化合物,如图是俯视图和侧视图,俯视图中小六元环为石墨层,大六元环含3个大球(石墨六元环中心正上方)和3个小球(石墨层部分碳原子正上方),请写出该化合物的化学式______________ ,在石墨六元环中心正上方的元素为______________ 。(填元素符号)

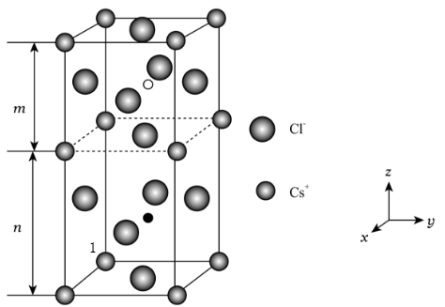
(5)卤素还被称为成盐元素,某种卤素盐的晶体中含有Cl,Cs与Au三种元素,其最简式为 ,Au有两种化合价,其一个晶胞结构如图所示,未标出的两个小球为金(Au)离子,底面正方形边长为
,Au有两种化合价,其一个晶胞结构如图所示,未标出的两个小球为金(Au)离子,底面正方形边长为 ,高为
,高为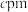 ,高分为两段,分别为
,高分为两段,分别为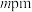 和
和 ,
, 的相对分子质量为M,回答下列问题:
的相对分子质量为M,回答下列问题:
①如果 与
与 相等,
相等, 和
和 构成
构成______________ 晶胞。
②金(Au)离子和 的配位数分别为
的配位数分别为__________ 和__________ 。
③如图所示,以原子1为原点建立坐标系,写出晶胞内部小白球的分数坐标______ 。
(1)F,Cl,Br,I形成简单氢化物的沸点由高到低的顺序为:
(2)卤素可形成很多酸根离子,如
 、
、 、
、 、
、 等,
等, 的空间结构为
的空间结构为(3)卤素元素之间还能形成很多卤素互化物,如
 ,
, ,
,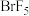 ,
,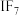 等,根据I与Cl原子的电负性大小关系写成
等,根据I与Cl原子的电负性大小关系写成 在水中水解的化学方程式:
在水中水解的化学方程式:(4)在石墨烯膜上可以制备Cl元素和Ca元素形成的新型的化合物,如图是俯视图和侧视图,俯视图中小六元环为石墨层,大六元环含3个大球(石墨六元环中心正上方)和3个小球(石墨层部分碳原子正上方),请写出该化合物的化学式

(5)卤素还被称为成盐元素,某种卤素盐的晶体中含有Cl,Cs与Au三种元素,其最简式为
 ,Au有两种化合价,其一个晶胞结构如图所示,未标出的两个小球为金(Au)离子,底面正方形边长为
,Au有两种化合价,其一个晶胞结构如图所示,未标出的两个小球为金(Au)离子,底面正方形边长为 ,高为
,高为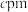 ,高分为两段,分别为
,高分为两段,分别为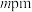 和
和 ,
, 的相对分子质量为M,回答下列问题:
的相对分子质量为M,回答下列问题:
①如果
 与
与 相等,
相等, 和
和 构成
构成②金(Au)离子和
 的配位数分别为
的配位数分别为③如图所示,以原子1为原点建立坐标系,写出晶胞内部小白球的分数坐标
您最近一年使用:0次
2 . CO、 与人体血液中的血红蛋白(Hb)可建立如下平衡:
与人体血液中的血红蛋白(Hb)可建立如下平衡: ,当HbCO浓度为
,当HbCO浓度为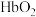 浓度的2%时,大脑就会受到严重损伤.生物大分子血红蛋白分子链的部分结构及载氧示意如图。下列说法错误的是
浓度的2%时,大脑就会受到严重损伤.生物大分子血红蛋白分子链的部分结构及载氧示意如图。下列说法错误的是

 与人体血液中的血红蛋白(Hb)可建立如下平衡:
与人体血液中的血红蛋白(Hb)可建立如下平衡: ,当HbCO浓度为
,当HbCO浓度为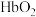 浓度的2%时,大脑就会受到严重损伤.生物大分子血红蛋白分子链的部分结构及载氧示意如图。下列说法错误的是
浓度的2%时,大脑就会受到严重损伤.生物大分子血红蛋白分子链的部分结构及载氧示意如图。下列说法错误的是
| A.构成血红蛋白分子链的多肽链之间存在氢键作用 |
B.血红素中 提供空轨道形成配位键 提供空轨道形成配位键 |
C.CO与血红素中 配位能力强于 配位能力强于 |
| D.用酸性丙酮提取血红蛋白中血红素时仅发生物理变化 |
您最近一年使用:0次
名校
解题方法
3 . 下列说法正确的是
A. 和 和 中C、O、N杂化方式均相同 中C、O、N杂化方式均相同 |
B. 和 和 分子都是含极性键的极性分子 分子都是含极性键的极性分子 |
| C.最外层电子数为2的元素都分布在s区 |
| D.石墨晶体层内是共价键,层与层间是范德华力,所以石墨是一种过渡晶体 |
您最近一年使用:0次
名校
解题方法
4 . 下列化学用语表示正确的是
A.基态 的价电子轨道表示式: 的价电子轨道表示式: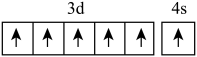 |
B.氨基的电子式: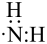 |
C.2,3-二甲基丁烷的键线式: |
D. 的VSEPR模型: 的VSEPR模型: |
您最近一年使用:0次
5 . 氢能是一种极具发展潜力的清洁能源,下列物质是具有广阔应用前景的储氢材料。
(1)氢化钠(NaH)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的化学方程式为___________ 。
(2) (氨硼烷)具有很高的储氢容量及相对低的放氢温度,是颇具潜力的储氢材料,它可通过环硼氮烷、
(氨硼烷)具有很高的储氢容量及相对低的放氢温度,是颇具潜力的储氢材料,它可通过环硼氮烷、 与
与 进行合成。
进行合成。
① 中涉及的元素H、B、N电负性最大的是
中涉及的元素H、B、N电负性最大的是___________ (填元素符号,下同);根据对角线规则,B的一些化学性质与元素___________ 相似。
② 分子中存在配位键,
分子中存在配位键,___________ 原子提供空轨道,___________ 原子提供孤对电子。
③键角:
___________  (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是___________ 。
(3)某种新型储氢材料的晶胞如图。

①该物质摩尔质量为188g/mol,其化学式为___________ 。
②该化合物中M离子的价电子排布图为___________ 。
③该晶体密度为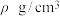 ,晶胞的边长为
,晶胞的边长为___________ nm。
(1)氢化钠(NaH)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的化学方程式为
(2)
 (氨硼烷)具有很高的储氢容量及相对低的放氢温度,是颇具潜力的储氢材料,它可通过环硼氮烷、
(氨硼烷)具有很高的储氢容量及相对低的放氢温度,是颇具潜力的储氢材料,它可通过环硼氮烷、 与
与 进行合成。
进行合成。①
 中涉及的元素H、B、N电负性最大的是
中涉及的元素H、B、N电负性最大的是②
 分子中存在配位键,
分子中存在配位键,③键角:

 (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是(3)某种新型储氢材料的晶胞如图。

①该物质摩尔质量为188g/mol,其化学式为
②该化合物中M离子的价电子排布图为
③该晶体密度为
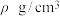 ,晶胞的边长为
,晶胞的边长为
您最近一年使用:0次
6 . 密胺树脂是仿瓷餐具的主要成分,其反应中间体的结构简式如下。下列关于该中间体说法正确的是
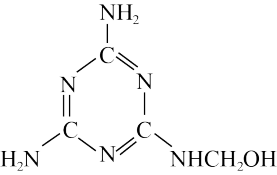

A.部分元素的第一电离能: |
| B.所有元素都处于元素周期表的p区 |
C.1个分子中采取 杂化的原子数为5 杂化的原子数为5 |
| D.基态碳原子最高能级的轨道形状为球形 |
您最近一年使用:0次
7 .  溶于氨水的反应方程式为:
溶于氨水的反应方程式为: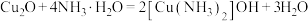 ,下列说法
,下列说法错误 的是
 溶于氨水的反应方程式为:
溶于氨水的反应方程式为: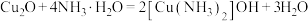 ,下列说法
,下列说法A.氮原子结构示意图为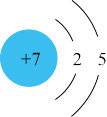 | B. 的VSEPR模型为三角锥形 的VSEPR模型为三角锥形 |
C. 的电子式为 的电子式为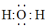 | D.基态 的价层电子排布式为 的价层电子排布式为 |
您最近一年使用:0次
解题方法
8 . 在月球玄武岩中发现了钛铁矿(主要成分的化学式含Ti、Fe、O三种元素),钛铁矿广泛应用于各个领域,包括冶金、化工、建筑、航空航天、电子等。请回答下列有关问题:
(1)铁在周期表中的位置是___________ 。
(2)基态钛原子的价层电子排布式为___________ ,其最外层电子的电子云轮廓图为___________ 。
(3)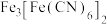 中的配体为
中的配体为___________ ;其中 C原子的杂化类型为___________ ,1 mol 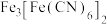 含有的σ键数目为
含有的σ键数目为___________ 。
(4)Ti的四卤化物的熔点如表所示,TiF4熔点高于其它三种卤化物,自TiCl4至TiI4熔点依次升高,其原因是___________ 。
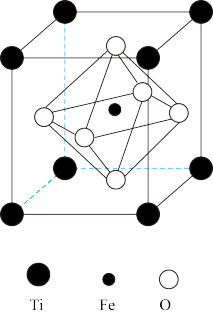
(5)钛铁矿主要成分的晶胞为立方体,其结构如图所示,钛铁矿主要成分的化学式为___________ ;已知该晶胞参数为a pm,NA为阿伏加德罗常数值,则该晶胞的密度为___________ g/cm3(用含a、NA的代数式表示)。
(1)铁在周期表中的位置是
(2)基态钛原子的价层电子排布式为
(3)
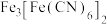 中的配体为
中的配体为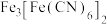 含有的σ键数目为
含有的σ键数目为(4)Ti的四卤化物的熔点如表所示,TiF4熔点高于其它三种卤化物,自TiCl4至TiI4熔点依次升高,其原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |

您最近一年使用:0次
解题方法
9 . 在硫酸铜溶液中加入浓氨水,可形成配离子[Cu(NH3)4(H2O)2]2+。下列有关说法中正确的是
| A.中心离子的配位数为4 |
| B.电负性由大到小为N>O>Cu |
| C.基态原子的第一电离能:N>O>S |
| D.键角:H2O>NH3 |
您最近一年使用:0次
10 . 法匹拉韦常用于治疗流感,其结构如下图所示,下列有关说法正确的是
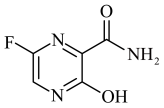
| A.法匹拉韦属于氨基酸 |
| B.法匹拉韦的分子式为C5H4FN3O2 |
| C.法匹拉韦分子中的碳原子杂化方式为sp2、sp3 |
| D.法匹拉韦分子只能跟酸反应,不能与碱反应 |
您最近一年使用:0次
2023-06-30更新
|
182次组卷
|
2卷引用:重庆市2022-2023学年高二下学期期末联合诊断检测化学试题



