名校
解题方法
1 . 氢、氮、氧、铁、铜等元素及其化合物在人们的日常生活中有着广泛的用途。回答下列问题:
(1)写出基态铜原子的价电子排布式__________________
(2)和铜在同一周期中,基态原子未成对电子数为2的元素共有______ 种。
(3)NH4HF2中HF2-的结构为F-H.......F-,则NH4HF2中含有的化学键有_________
(A)离子键 (B)共价键 (C)金属键 (D)氢键 (E)配位键
(4)写出与NH4+互为等电子体的一种分子的化学式________ ;
(5)CH3OH分子中C原子的杂化方式为_________ ,键角:H-C-H_______ H-O-C。(填“<”、“>”、“=”)
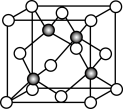
(6)Cu 与Cl 形成某种化合物的晶胞如下图所示,Cu的配位数是________ ,该晶体的密度为ρg·cm-3,晶胞边长为a cm,则阿伏加 德罗常数为____________ (用含ρ、a的代数式表示)。
(1)写出基态铜原子的价电子排布式
(2)和铜在同一周期中,基态原子未成对电子数为2的元素共有
(3)NH4HF2中HF2-的结构为F-H.......F-,则NH4HF2中含有的化学键有
(A)离子键 (B)共价键 (C)金属键 (D)氢键 (E)配位键
(4)写出与NH4+互为等电子体的一种分子的化学式
(5)CH3OH分子中C原子的杂化方式为
(6)Cu 与Cl 形成某种化合物的晶胞如下图所示,Cu的配位数是

您最近一年使用:0次
名校
解题方法
2 . 早在1998年,中国科学家便成功地在较低温度下制造出金刚石:CCl4+4Na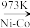 C(金刚石)+4NaCl。这项成果被“美国化学与工程新闻”评价为“稻草变黄金”。回答下列问题:
C(金刚石)+4NaCl。这项成果被“美国化学与工程新闻”评价为“稻草变黄金”。回答下列问题:
(1)Ni原子价层电子的排布式为_______ 。元素C、Cl、Na中,第一电离能最大的是______________ 。
(2)石墨在高温高压下也可转变为金刚石。在石墨和金刚石中,C原子的杂化类型分别为_____________ ,熔点较高的是_____________ ,其原因为_______________ 。
(3)NH3易与Ni形成配合物 [Ni(NH3)6]SO4,该配合物中存在的化学键类型有_____________ ,其阴离子的空间构型为_____________ 。
(4)金属间化合物MgCNi3是一种新型超导体,呈钙钛矿构型,X射线衍射实验测得其晶胞参数为a=0.3812 nm,其晶胞结构如图所示。晶胞中C位于Ni所形成的正八面体的体心,该正八面体的边长为___________ nm。( =1.414)
=1.414)

(5)在MgCNi3晶胞结构的另一种表示中,Mg处于体心位置,则C处于________________ 位置,Ni处于_______________ 位置。
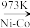 C(金刚石)+4NaCl。这项成果被“美国化学与工程新闻”评价为“稻草变黄金”。回答下列问题:
C(金刚石)+4NaCl。这项成果被“美国化学与工程新闻”评价为“稻草变黄金”。回答下列问题:(1)Ni原子价层电子的排布式为
(2)石墨在高温高压下也可转变为金刚石。在石墨和金刚石中,C原子的杂化类型分别为
(3)NH3易与Ni形成配合物 [Ni(NH3)6]SO4,该配合物中存在的化学键类型有
(4)金属间化合物MgCNi3是一种新型超导体,呈钙钛矿构型,X射线衍射实验测得其晶胞参数为a=0.3812 nm,其晶胞结构如图所示。晶胞中C位于Ni所形成的正八面体的体心,该正八面体的边长为
 =1.414)
=1.414)
(5)在MgCNi3晶胞结构的另一种表示中,Mg处于体心位置,则C处于
您最近一年使用:0次
名校
解题方法
3 . (一)是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
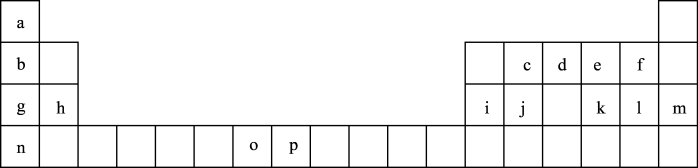
试回答下列问题:
①表中碱性最强的为_______ (写出化学式);氢化物稳定性最强的为 ______ ;(写出化学式)
②基态o原子的价电子排布图为______ ;P3+离子与KSCN反应新生成的化学键为 _____ 键。
③将周期表中g、h、i、j四种元素的第一电离能由大到小排序为_________ (用元素符号表示)。
(二)SiO2晶胞(如图1)可理解成将金刚石晶胞(如图2)中的C原子置换成Si原子,然后在Si—Si之间插入O原子而形成。
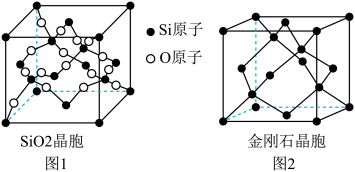
①推测SiO2晶胞中Si采用______ 杂化,O—Si—O的键角为___________ 。
②一个SiO2晶胞中,含有_______ 个Si原子。
③金刚石和晶体硅都是原子晶体,具有相似的结构,则熔点:金刚石_______ Si晶体(填“大于”,“等于”或“小于”)
④假设金刚石晶胞的边长为a pm,NA为阿伏加 德罗常数,试计算该晶胞的密度______ g·cm-3(写出表达式即可)。

试回答下列问题:
①表中碱性最强的为
②基态o原子的价电子排布图为
③将周期表中g、h、i、j四种元素的第一电离能由大到小排序为
(二)SiO2晶胞(如图1)可理解成将金刚石晶胞(如图2)中的C原子置换成Si原子,然后在Si—Si之间插入O原子而形成。

①推测SiO2晶胞中Si采用
②一个SiO2晶胞中,含有
③金刚石和晶体硅都是原子晶体,具有相似的结构,则熔点:金刚石
④假设金刚石晶胞的边长为a pm,NA为阿伏加 德罗常数,试计算该晶胞的密度
您最近一年使用:0次
2019-10-23更新
|
184次组卷
|
3卷引用:重庆南开中学高2020届高三11月月考理综化学试题
名校
4 . 我国用BeO、KBF4等原料制备KBe2BO3F2晶体,在世界上首次实现在177.3 nm深紫外激光倍频输出,其晶胞如图所示。下列说法错误的是
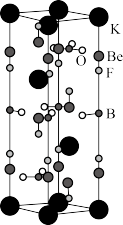
| A.构成晶体的非金属元素的电负性由大到小的顺序为F>O>B |
| B.KBF4中的阴离子的中心原子的杂化方式为sp2 |
| C.根据元素周期表中元素所处的位置可推测BeO与Al2O3性质相似 |
| D.晶胞中的K+有2个位于晶胞内部,8个位于晶胞顶点,则1mol该晶胞含3molKBe2BO3F2 |
您最近一年使用:0次
2019-10-13更新
|
1317次组卷
|
14卷引用:山东省日照市莒县第一中学2019-2020学年高三10月月考化学试卷
山东省日照市莒县第一中学2019-2020学年高三10月月考化学试卷四川省雅安中学2019-2020学年高二上学期期中考试化学试题山东省青岛市第二中学2020届高三上学期期中考试化学试题重庆市实验中学校2021-2022学年高二下学期第一次月考化学试题(人教版2019)选择性必修2 阶段性综合评估测试卷(二)鲁科版2019选择性必修2阶段性综合评估测试卷(二)河北省衡水市第十四中学2020-2021学年高二下学期一调考试化学试题河北省石家庄市第二十三中学2021-2022学年高二下学期期中考试化学试题广东省佛山市南海区南海中学2021-2022学年高二年级下学期4月月考化学试题湖南省邵东创新实验学校2021-2022学年高二下学期期中考试化学试题湖北省武汉市钢城第四中学2021-2022学年高二下学期期中考试化学试题黑龙江省哈尔滨市德强高级中学2021-2022学年高二下学期4月月考化学试题吉林省洮南市第一中学2022-2023学年高二下学期学习质量检测化学试卷广东省广州市番禺区番禺中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
5 . 过渡金属元素如Fe、Mn、Cu、Ni可用作很多反应的催化剂,在室温下以H2O2为氧化剂直接将CH4氧化,回答下列问题:
(1)基态铜原子的核外电子排布式是___ ,第四周期元素中,基态原子未成对电子数最多的元素是____ (填元素符号)
(2)C、H、O、Fe四种元素的电负性由大到小的顺序是____
(3)常温下,H2O2氧化CH4生成CH3OH、HCHO等
①CH3OH和HCHO的沸点分别是64.7℃、-19.5℃,其主要原因是____
②CH4、HCHO的键角较大的是___ ,原因是______
(4)Cu2+可与乙二胺(NH2CH2CH2NH2,简写为en)形成配合物,化学式为Cu(en)22+,乙二胺中与Cu2+形成配位键的原子是___ (填元素符号),该配合物的配位数是__
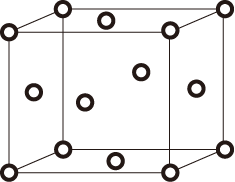
(5)Cu晶胞结构如图所示,已知铜原子半径为apm,阿伏加 德罗常数用NA表示,则铜晶体的密度为____ g/cm3(写出计算表达式)
(1)基态铜原子的核外电子排布式是
(2)C、H、O、Fe四种元素的电负性由大到小的顺序是
(3)常温下,H2O2氧化CH4生成CH3OH、HCHO等
①CH3OH和HCHO的沸点分别是64.7℃、-19.5℃,其主要原因是
②CH4、HCHO的键角较大的是
(4)Cu2+可与乙二胺(NH2CH2CH2NH2,简写为en)形成配合物,化学式为Cu(en)22+,乙二胺中与Cu2+形成配位键的原子是
(5)Cu晶胞结构如图所示,已知铜原子半径为apm,阿伏加 德罗常数用NA表示,则铜晶体的密度为

您最近一年使用:0次
名校
解题方法
6 . X、Y、Z、M、W是前四周期元素,原子序数依次增大,X元素原子最外层电子数是内层的2倍,Y的原子半径是在同周期中最大;Z元素原子的最外层电子数比次外层电子数少2,M原子外围电子排布式为3dn4sn;W的内层电子己全充满,最外层只有2个电子。
请回答下列问题:
(1)Y元素在周期表中的位置是_________ ;W2+离子的价电子排布式为__________ 。
(2)X能与S、氮、氧二种元素构成化合物XO(NH2)2,其中X原子和N原子的杂化方式为分别为_____ 、____ ,该化合物分子中的π键与 键的个数之比是
键的个数之比是____ ;该物质易溶于水的主要原因是____ 。
(3)已知Be和A1元素处于周期表中对角线位置,化学性质相似,请写出Y元素的最高价氧化物对应水化物与Be相互反应的化学方程式:____________ 。
(4)M晶体的原子堆积如图所示,则该晶体的堆积方式为________ ,晶体中M原子的配位数是_____ 。某M配合物的化学式是[M(H2O)5C1]Cl2·H2O,1mol该配合物中含配位键是_____ mol。
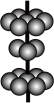
(5)Y离子和Z离子比较,半径较大的是__________ (填离子符号)元素Y与元素Z形成了晶体的晶胞结构是如图所示的正方体,每个Y离子周围与它最接近的Y离子有__________ 个。
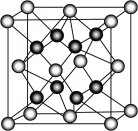
请回答下列问题:
(1)Y元素在周期表中的位置是
(2)X能与S、氮、氧二种元素构成化合物XO(NH2)2,其中X原子和N原子的杂化方式为分别为
 键的个数之比是
键的个数之比是(3)已知Be和A1元素处于周期表中对角线位置,化学性质相似,请写出Y元素的最高价氧化物对应水化物与Be相互反应的化学方程式:
(4)M晶体的原子堆积如图所示,则该晶体的堆积方式为

(5)Y离子和Z离子比较,半径较大的是

您最近一年使用:0次
名校
7 . I.有下列物质:①钠 ②金刚石 ③冰 ④Na2O2 ⑤MgCl2 ⑥氯化铵 ⑦水晶 ⑧Cl2
(1)属于原子晶体的是_________ ,属于金属晶体的是_________ 。
(2)既含有离子键又含有共价键的是_________ 。
(3)③熔化时克服作用力的有_________ 。
(4)Na2O2的电子式________________ 。
(5)②、③、⑤、⑦、⑧熔点由低到高的顺序为________________ 。
II.在生产生活以及化学科学研究中,水都有重要的作用。
(1)与H2O分子是等电子体的微粒_________ (阴离子及分子各写一个)。
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是__________ 。
A.微粒的形状发生了改变
B.氧原子的杂化类型发生了改变
C.微粒中的键角发生了改变
D.微粒的化学性质发生了改变
(3)向CuSO4溶液中加入氨水,溶液变成深蓝色,请写出发生此变化的离子方程式______________ 。
(1)属于原子晶体的是
(2)既含有离子键又含有共价键的是
(3)③熔化时克服作用力的有
(4)Na2O2的电子式
(5)②、③、⑤、⑦、⑧熔点由低到高的顺序为
II.在生产生活以及化学科学研究中,水都有重要的作用。
(1)与H2O分子是等电子体的微粒
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是
A.微粒的形状发生了改变
B.氧原子的杂化类型发生了改变
C.微粒中的键角发生了改变
D.微粒的化学性质发生了改变
(3)向CuSO4溶液中加入氨水,溶液变成深蓝色,请写出发生此变化的离子方程式
您最近一年使用:0次
名校
8 . 关于如图结构的说法不正确的是( )
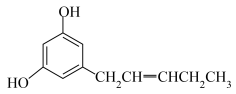

A.分子中既有 键又有π键 键又有π键 |
| B.碳原子有sp、sp2、sp3三种杂化方式 |
| C.O—H键的极性强于C-H键的极性 |
| D.羟基中氧原子采取sp3杂化,VSEPR模型为四面体形 |
您最近一年使用:0次
2019-06-26更新
|
696次组卷
|
8卷引用:【全国百强校】重庆市第八中学2018-2019学年高二下学期第二次月考化学试题
9 . 硼酸(H3BO3)是一种片层状结构的白色晶体(下图),有油腻感,可做润滑剂。硼酸对人体受伤组织有缓和防腐作用,故可以用于医药和食品防腐等方面。回答下列问题:
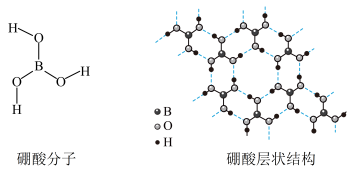
(1)B原子的结构示意图为_____________________ ;
(2)硼酸为一元弱酸,在水中电离方程式为H3BO3+H2O [B(OH)4]-+H+,写出硼酸与NaOH溶液反应的离子方程式
[B(OH)4]-+H+,写出硼酸与NaOH溶液反应的离子方程式_________________________ ;
(3)下列有关硼酸晶体的说法正确的是__________ ;
A.H3BO3分子的稳定性与氢键有关
B.含1 molH3BO3的晶体中有3 mol氢键
C.分子中B、O最外层均为8e-稳定结构
D.B原子杂化轨道的类型sp2,同层分子间的主要作用力是范德华力
(4)根据对角线规则,与B性质相似的元素是__________ 。
(5)含氧酸的通式为(HO)mROn,根据非羟基氧原子数判断,与H3BO3酸性最接近的是________ ;
A.HClO B.H4SiO4 C.H3PO4 D.HNO2
(6)一种硼酸盐的阴离子为B3O6n-,n=_____________ ;B3O6n-结构中只有一个六元环,B的空间化学环境相同,O有两种空间化学环境,画出B3O6n-的结构图(注明所带电荷数); _____________ 。

(1)B原子的结构示意图为
(2)硼酸为一元弱酸,在水中电离方程式为H3BO3+H2O
 [B(OH)4]-+H+,写出硼酸与NaOH溶液反应的离子方程式
[B(OH)4]-+H+,写出硼酸与NaOH溶液反应的离子方程式(3)下列有关硼酸晶体的说法正确的是
A.H3BO3分子的稳定性与氢键有关
B.含1 molH3BO3的晶体中有3 mol氢键
C.分子中B、O最外层均为8e-稳定结构
D.B原子杂化轨道的类型sp2,同层分子间的主要作用力是范德华力
(4)根据对角线规则,与B性质相似的元素是
(5)含氧酸的通式为(HO)mROn,根据非羟基氧原子数判断,与H3BO3酸性最接近的是
A.HClO B.H4SiO4 C.H3PO4 D.HNO2
(6)一种硼酸盐的阴离子为B3O6n-,n=
您最近一年使用:0次
2019-06-14更新
|
115次组卷
|
2卷引用:2015-2016学年重庆市第八中学高二下第三次月考化学试卷
名校
解题方法
10 . N、Fe是两种重要的元素,其单质及化合物在诸多领域中都有广泛的应用。
(1)基态N原子最高能级的电子云轮廓图形状是__________ ,其核外有______ 种不同运动状态的电子。
(2)第一电离能N_____ O(填“>”“<”或“=”),其原因是_______________________ 。
(3)在高压下氮气会发生聚合得到高聚氮。晶体中每个氮原子与另外三个氮原子结合形成空间网状结构。高聚氮的晶体类型是__________ ,氮原子的杂化轨道类型为__________ 。
(4)六方氮化硼(BN)与石墨晶体结构类似,硼原子和氮原子交替相连,但石墨可以导电而六方BN却不能导电,其原因是_____________________________ 。
(5)叠氮酸(HN3)在生产生活中有着重要应用。叠氮酸(HN3)可用HNO2氧化肼(N2H4)制得,化学方程式是N2H4 + HNO2=HN3 + 2H2O。下列叙述错误的是_________ 。
A.HN3和N2H4都是由极性键和非极性键构成的非极性分子
B.NaN3的晶格能大于KN3的晶格能
C.HN3分子中四个原子可能在一条直线上
D.叠氮酸(HN3)和水能形成分子间氢键
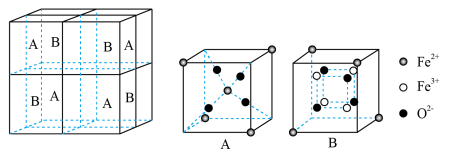
(6)某种离子型铁的氧化物晶胞如图所示,它由A、B方块组成。则该化合物中Fe2+、Fe3+、O2-的个数比是__________ (填最简整数比);已知该晶体的晶胞参数为a nm,阿伏加 德罗常数的值为NA,则该晶体的密度是_______ g cm-3(用含a和NA的代数式表示)。
cm-3(用含a和NA的代数式表示)。
(1)基态N原子最高能级的电子云轮廓图形状是
(2)第一电离能N
(3)在高压下氮气会发生聚合得到高聚氮。晶体中每个氮原子与另外三个氮原子结合形成空间网状结构。高聚氮的晶体类型是
(4)六方氮化硼(BN)与石墨晶体结构类似,硼原子和氮原子交替相连,但石墨可以导电而六方BN却不能导电,其原因是
(5)叠氮酸(HN3)在生产生活中有着重要应用。叠氮酸(HN3)可用HNO2氧化肼(N2H4)制得,化学方程式是N2H4 + HNO2=HN3 + 2H2O。下列叙述错误的是
A.HN3和N2H4都是由极性键和非极性键构成的非极性分子
B.NaN3的晶格能大于KN3的晶格能
C.HN3分子中四个原子可能在一条直线上
D.叠氮酸(HN3)和水能形成分子间氢键
(6)某种离子型铁的氧化物晶胞如图所示,它由A、B方块组成。则该化合物中Fe2+、Fe3+、O2-的个数比是
 cm-3(用含a和NA的代数式表示)。
cm-3(用含a和NA的代数式表示)。
您最近一年使用:0次
2019-06-04更新
|
262次组卷
|
2卷引用:【全国百强校】重庆市西南大学附属中学校2019届高三第十次月考理科综合化学试题



