名校
1 . X、Y、Z、W是四种原子序数依次增大的短周期元素,W的最外层电子数比X的最外层电子数少1个,X、Y、Z为同一周期元素,X、Y、Z组成一种化合物(ZXY)2的结构式如图所示。下列叙述不正确的是( )
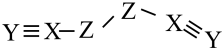
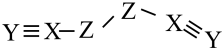
| A.化合物(ZXY)2中Z元素的化合价为-2价 |
| B.Y的氧化物对应的水化物可能是弱酸 |
| C.(ZXY)2分子中X原子的杂化方式为sp杂化 |
| D.X、Y、Z、W四种元素电负性的大小顺序为:Z>Y>X>W |
您最近一年使用:0次
2020-05-20更新
|
134次组卷
|
3卷引用:湖北省四校(曾都一中、枣阳一中等)2019-2020学年高二下学期期中考试化学试题
2 . 铁及其化合物在生产生活中有着广泛的应用。回答下列问题:
(1)基态Fe原子的外围电子排布图为____ ,基态Fe2+中,核外电子占据最高能层的符号是____ ,Fe2+和Fe3+是铁的两种常见离子,Fe3+的稳定性强于Fe2+,原因是____ 。
(2)Fe3+可以与SCN—形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验Fe3+的存在,KSCN中四种元素的电负性由小到大的顺序为_______ ,SCN—的几何构型为______ ,中心原子的杂化类型为_______ 。
(3)实验中常用K3[Fe(CN)6]检验Fe2+, K3[Fe(CN)6]晶体中的化学键有_________ (填写选项字母)
a.离子键. b.共价键 c,氢键 d .配位键 e.金属键
1mol K3[Fe(CN)6]中含有σ键与π键的数目比为_____________ 。
(4)FexO为氯化钠型结构,在实际晶体中,由于存在缺陷,x<1。 测得Fe0.92O晶体的晶胞参数a=428.0pm,则该晶体的密度ρ=__________ g/cm3 (列出计算式),晶体中最近的两个铁离子间的距离为_______ pm。
(1)基态Fe原子的外围电子排布图为
(2)Fe3+可以与SCN—形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验Fe3+的存在,KSCN中四种元素的电负性由小到大的顺序为
(3)实验中常用K3[Fe(CN)6]检验Fe2+, K3[Fe(CN)6]晶体中的化学键有
a.离子键. b.共价键 c,氢键 d .配位键 e.金属键
1mol K3[Fe(CN)6]中含有σ键与π键的数目比为
(4)FexO为氯化钠型结构,在实际晶体中,由于存在缺陷,x<1。 测得Fe0.92O晶体的晶胞参数a=428.0pm,则该晶体的密度ρ=
您最近一年使用:0次
2020-05-20更新
|
386次组卷
|
3卷引用:重庆市第八中学2020届高三高考模拟试卷化学试题(三)
解题方法
3 . 铜是人类知道最早的金属之一,也是广泛使用的第一种金属。回答下列问题:
(1)镍白铜(铜镍合金)可用于制作仿银饰品。第二电离能I2(Cu)______________ Ⅰ2(Ni)(填“>"或 “<”),其原因为______________ 。
(2)向[Cu(NH3)2]Cl溶液中通入乙炔(C2H2)气体,可生成红棕色沉淀Cu2C2。
①C2H2分子中 键与
键与 键的数目之比为
键的数目之比为______________ ;碳原子的杂化方式为______________ 。
②写出与Cu2C2中阴离子C22-互为等电子体的一种分子和一种离子______________ 。
(3)乙二胺(H2N-CH2CH2-NH2)易与Cu2+形成络合物用于Cu2+的定量测定。
①形成的络合物中提供孤对电子的原子为______________ (填元素符号)。
②乙二胺中所含元素的电负性由大到小的顺序为______________ ;乙二胺在水中溶解度较大的原因为______________ 。
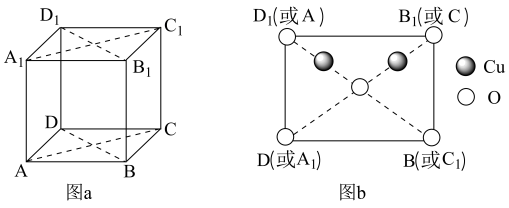
(4)铜与氧构成的某种化合物的立方晶胞如图a所示,图b是沿晶胞对角面取得的截图,晶胞中所有原子均在对角面上。氧原子的配位数为______________ ,若Cu原子之间最短距离为dpm,阿伏加 德罗常数的值为NA,该晶体的密度为______________ g·cm-3(列出计算式即可)。
(1)镍白铜(铜镍合金)可用于制作仿银饰品。第二电离能I2(Cu)
(2)向[Cu(NH3)2]Cl溶液中通入乙炔(C2H2)气体,可生成红棕色沉淀Cu2C2。
①C2H2分子中
 键与
键与 键的数目之比为
键的数目之比为②写出与Cu2C2中阴离子C22-互为等电子体的一种分子和一种离子
(3)乙二胺(H2N-CH2CH2-NH2)易与Cu2+形成络合物用于Cu2+的定量测定。
①形成的络合物中提供孤对电子的原子为
②乙二胺中所含元素的电负性由大到小的顺序为
(4)铜与氧构成的某种化合物的立方晶胞如图a所示,图b是沿晶胞对角面取得的截图,晶胞中所有原子均在对角面上。氧原子的配位数为

您最近一年使用:0次
2020-05-17更新
|
137次组卷
|
2卷引用:石家庄市2020届高三年级阶段性训练题
解题方法
4 . 铜及其化合物在生产生活中有着广泛的应用。请回答下列问题:
(1)铜元素位于元素周期表中第四周期________ 族,属于元素周期表中________ 区元素,基态Cu原子有___________ 种不同能级的电子。
(2)元素铜与镍的第二电离能分别为:ICu=1958 kJ·mol-1、INi=1753 kJ·mol-1, ICu>INi的原因是________________________________________________________ 。
(3)硫化亚铜和氧化亚铜均为离子晶体,二者比较,熔点较高的是氧化亚铜,原因为_________________________________________ 。
(4)某含铜化合物的离子结构如图1所示。

①该离子中存在的作用力有______________ (填标号)。
A.离子键 B.共价键 C.配位键 D.氢键 E.范德华力
②该离子中碳原子的杂化类型有____________ 。
(5)CuCl2和CuCl是铜的两种氯化物。
①图2中表示的是________ (填“CuCl2”或“CuCl”)的晶胞。
②原子坐标参数可用来表示晶胞内部各原子的相对位置。图2中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,1,0);则D原子的坐标参数为____________ 。
③已知图2所示晶胞中C、D两原子核间距为298pm,阿伏加 德罗常数的值为NA,则该晶体密度为___________________ g·cm-3(列出计算式即可)。
(1)铜元素位于元素周期表中第四周期
(2)元素铜与镍的第二电离能分别为:ICu=1958 kJ·mol-1、INi=1753 kJ·mol-1, ICu>INi的原因是
(3)硫化亚铜和氧化亚铜均为离子晶体,二者比较,熔点较高的是氧化亚铜,原因为
(4)某含铜化合物的离子结构如图1所示。

①该离子中存在的作用力有
A.离子键 B.共价键 C.配位键 D.氢键 E.范德华力
②该离子中碳原子的杂化类型有
(5)CuCl2和CuCl是铜的两种氯化物。
①图2中表示的是
②原子坐标参数可用来表示晶胞内部各原子的相对位置。图2中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,1,0);则D原子的坐标参数为
③已知图2所示晶胞中C、D两原子核间距为298pm,阿伏加 德罗常数的值为NA,则该晶体密度为
您最近一年使用:0次
名校
解题方法
5 . 钢化玻璃因其优良的性能广泛应用于日常生活,但由于制作玻璃时里面含有极少量硫化镍,使得钢化玻璃在极限条件下的使用受到限制。
(1)基态硫原子价层电子的轨道表达式 电子排布图
电子排布图 为
为__ ,基态镍原子中核外电子占据最高能层的符号为__ 。
(2)Ni(CO)4常用于制备纯镍,溶于乙醇、CCl4、苯等有机溶剂,为__ 晶体,Ni(CO)4空间构型与甲烷相同,中心原子的杂化轨道类型为__ ,写出与配体互为等电子体的阴离子__  任写一种
任写一种 。
。
(3)与硫同族的硒元素有两种常见的二元含氧酸,请比较它们酸性强弱__ >__  填化学式
填化学式 ,理由是
,理由是__ 。
(4)H2S的键角__ 填“大于”“小于”“等于”)H2O的键角,请从电负性的角度说明理由__ 。
(5)NiO与NaCl的晶胞结构相似,如图所示,阴离子采取面心立方堆积,阳离子填充在位于阴离子构成的__ 空隙中,已知Ni2+半径为69nm,O2-半径为140nm,阿伏加 德罗常数为NA,NiO晶体的密度为__ g/cm3(只列出计算式 。
。

(1)基态硫原子价层电子的轨道表达式
 电子排布图
电子排布图 为
为(2)Ni(CO)4常用于制备纯镍,溶于乙醇、CCl4、苯等有机溶剂,为
 任写一种
任写一种 。
。(3)与硫同族的硒元素有两种常见的二元含氧酸,请比较它们酸性强弱
 填化学式
填化学式 ,理由是
,理由是(4)H2S的键角
(5)NiO与NaCl的晶胞结构相似,如图所示,阴离子采取面心立方堆积,阳离子填充在位于阴离子构成的
 。
。
您最近一年使用:0次
名校
解题方法
6 . 元素A、B、C、D、E的原子序数依次增大,且均小于36。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;D的价电子数为2且与E同周期;E的基态原子的内部各能层均排满,且4s能级有1个单电子。回答下列问题:
(1)基态E原子的价电子排布式为____________________
(2)A、B、C三种元素第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3)与A的单质分子互为等电子体的分子和离子分别是________ (用分子和离子符号表示)。AB2的空间构型为___________ ,其中A原子的杂化类型是_______________
(4)B元素简单氢化物的沸点是同族元素中最高的,原因是_____________
(5)向含E元素的硫酸盐溶液中加入过量氨水,可得到深蓝色透明溶液。向溶液中加入乙醇,将析出深蓝色晶体。该晶体的化学式为[Cu(NH3)4]SO4∙H2O晶体中阳离子的结构式为____________
(6)C和D形成化合物的晶胞结构如图所示,已知晶体的密度为ρg/cm,阿伏加 德罗常数为NA,则晶胞边长a=______________ cm(用含ρ、NA的计算式表示)。

(1)基态E原子的价电子排布式为
(2)A、B、C三种元素第一电离能由大到小的顺序为
(3)与A的单质分子互为等电子体的分子和离子分别是
(4)B元素简单氢化物的沸点是同族元素中最高的,原因是
(5)向含E元素的硫酸盐溶液中加入过量氨水,可得到深蓝色透明溶液。向溶液中加入乙醇,将析出深蓝色晶体。该晶体的化学式为[Cu(NH3)4]SO4∙H2O晶体中阳离子的结构式为
(6)C和D形成化合物的晶胞结构如图所示,已知晶体的密度为ρg/cm,阿伏加 德罗常数为NA,则晶胞边长a=

您最近一年使用:0次
2020-05-09更新
|
105次组卷
|
2卷引用:重庆市凤鸣山中学2020届高三6月月考理综化学试题
名校
解题方法
7 . 据世界权威刊物《自然》最近报道,我国科学家选择碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料验证了三维量子霍尔效应,并发现了金属-绝缘体的转换。回答下列问题:
(1)锌和镉位于同副族,而锌与铜相邻。现有 4 种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10。失去1个电子需要的能量由大到小排序是______ (填字母)。
A.④②①③ B.④②③① C.①②④③ D.①④③②
(2)硫和碲位于同主族,H2S的分解温度高于H2Te,其主要原因是_______ 。在硫的化合物中,H2S、CS2都是三原子分子,但它们的键角(立体构型)差别很大,用价层电子对互斥理论解释:_________ ;用杂化轨道理论解释:_________ 。
(3)Cd2+与NH3等配体形成配离子。[Cd(NH3)4]2+中2个NH3被2个Cl-替代只得到1种结构,它的立体构型是___________ 。1 mol [Cd(NH3)4]2+含___________ mol σ键。
(4)砷与卤素形成多种卤化物。AsCl3、AsF3、AsBr3的熔点由高到低的排序为__________ 。
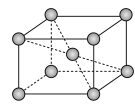
(5)锆晶胞如图所示,1个晶胞含_______ 个Zr原子;这种堆积方式称为__________ 。
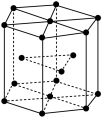
(6)镉晶胞如图所示。已知:NA是阿伏加 德罗常数的值,晶体密度为 d g·cm-3。在该晶胞中两个镉原子最近核间距为______ nm(用含NA、d的代数式表示),镉晶胞中原子空间利用率为________ (用含π的代数式表示)。
(1)锌和镉位于同副族,而锌与铜相邻。现有 4 种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10。失去1个电子需要的能量由大到小排序是
A.④②①③ B.④②③① C.①②④③ D.①④③②
(2)硫和碲位于同主族,H2S的分解温度高于H2Te,其主要原因是
(3)Cd2+与NH3等配体形成配离子。[Cd(NH3)4]2+中2个NH3被2个Cl-替代只得到1种结构,它的立体构型是
(4)砷与卤素形成多种卤化物。AsCl3、AsF3、AsBr3的熔点由高到低的排序为
(5)锆晶胞如图所示,1个晶胞含

(6)镉晶胞如图所示。已知:NA是阿伏加 德罗常数的值,晶体密度为 d g·cm-3。在该晶胞中两个镉原子最近核间距为

您最近一年使用:0次
2020-04-23更新
|
371次组卷
|
3卷引用:重庆市第一中学2019-2020学年高二下学期期末考试化学试题
名校
解题方法
8 . 储氢材料是一类能可逆地吸收和释放氢气的材料。LaNi5合金、NaBH4、H3B-NH3、Mg2NiH4等都是潜在储氢材料。回答下列问题:
(1)基态Ni原子的核外电子排布式为____ ,有___________ 个未成对的电子;
(2)NaBH4中H为-1价,Na、B、H电负性由大到小的顺序是_________ 。BH4-离子的立体构型为________ ,其中B的杂化轨道类型为_____ 。
(3)B2H6和NH3化合可以生成H3B-NH3,H3B-NH3加热时发生反应:H3B-NH3=BN+3H2,缓慢释放出H2。BN有类似于石墨的结构,B2H6、NH3和BN的沸点由高到低的顺序为_________ , 原因是___ 。
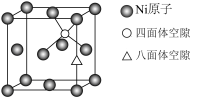
(4)X-射线衍射分析表明,Mg2NiH4 的立方晶胞的面心和顶点均被Ni原子占据,所有Mg原子的Ni配位数都相等。则Mg原子填入由Ni原子形成的_____ 空隙中(填“四面体”或“八面体”),其空隙占有百分率为_____ 。
(5)已知Mg2NiH4 晶体的晶胞参数为646.5 pm,液氢的密度为0.0708 g·cm-3。若以材料中氢的密度与液态氢密度之比定义储氢材料的储氢能力,则Mg2NiH4 的储氢能力是液氢的___ 倍(列出计算式即可)。
(1)基态Ni原子的核外电子排布式为
(2)NaBH4中H为-1价,Na、B、H电负性由大到小的顺序是
(3)B2H6和NH3化合可以生成H3B-NH3,H3B-NH3加热时发生反应:H3B-NH3=BN+3H2,缓慢释放出H2。BN有类似于石墨的结构,B2H6、NH3和BN的沸点由高到低的顺序为
(4)X-射线衍射分析表明,Mg2NiH4 的立方晶胞的面心和顶点均被Ni原子占据,所有Mg原子的Ni配位数都相等。则Mg原子填入由Ni原子形成的
(5)已知Mg2NiH4 晶体的晶胞参数为646.5 pm,液氢的密度为0.0708 g·cm-3。若以材料中氢的密度与液态氢密度之比定义储氢材料的储氢能力,则Mg2NiH4 的储氢能力是液氢的

您最近一年使用:0次
9 . 向盛有硫酸锌水溶液的试管中加入氨水,首先形成沉淀,继续滴加氨水,沉淀溶解得到无色透明的溶液。下列说法正确的是( )
| A.最后所得溶液中不存在沉淀,所以反应前后c(Zn2+)不变 |
| B.沉淀溶解是因为生成了无色的配合物离子[Zn(NH3)4]2+ |
| C.用硝酸锌溶液代替硫酸锌溶液进行实验,不能观察到同样的现象 |
| D.在[Zn(NH3)4]2+中,Zn2+提供孤对电子,NH3提供空轨道 |
您最近一年使用:0次
2020-04-10更新
|
290次组卷
|
8卷引用:【全国校级联考】福建省福州市八县(市)协作校2017-2018学年高二下学期期末联考化学试题
名校
解题方法
10 . 硼及其化合物在新材料、工农业生产等方面用途很广。请回答下列问题:
(1)写出与B元素同主族的Ga元素的基态原子核外电子排布式:________ 。
(2)立方氮化硼(BN)可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼比晶体硅具有更高的硬度和耐热性的原因是__________ 。
(3)BF3分子中中心原子的杂化轨道类型是____ 。又知若有d轨道参与杂化,能大大提高中心原子的成键能力,分析BF3、SiF4水解的产物中, 除了相应的酸外,前者生成BF4-而后者生成SiF62-的原因:_______________ 。
(4)NaBH4被认为是有机化学中的“万能还原剂”,NaBH4的电子式为_________ ,其中三种元素的电负性由大到小的顺序是_______________ 。
(5)自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作 Na2B4O7•10H2O,实际上它的结构单元是由两个H3BO3和两个B(OH)4]-(合而成的双六元环,应该写成 Na2[B4O5(OH)4]•8H2O,其结构如图所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是______________ (填字母)。

A.离子键 B.共价键 C.氢键 D.金属键 E.范德华力
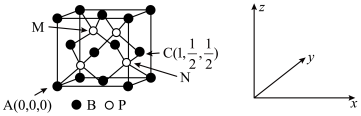
(6)磷化硼(BP)可作为金属表面的保护薄膜,其晶胞如图所示,在BP晶胞中P占据的是硼原子堆积的_____ (填“立方体”“正四面体”或“正八面体”)空隙。建立如图所示坐标系,可得晶胞中A、C处原子的分数坐标,则N处的P原子分数坐标为______ 。若晶胞中硼原子和磷原子之间的最近核间距为a pm,则晶胞边长为____________ cm。
(1)写出与B元素同主族的Ga元素的基态原子核外电子排布式:
(2)立方氮化硼(BN)可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼比晶体硅具有更高的硬度和耐热性的原因是
(3)BF3分子中中心原子的杂化轨道类型是
(4)NaBH4被认为是有机化学中的“万能还原剂”,NaBH4的电子式为
(5)自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作 Na2B4O7•10H2O,实际上它的结构单元是由两个H3BO3和两个B(OH)4]-(合而成的双六元环,应该写成 Na2[B4O5(OH)4]•8H2O,其结构如图所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是

A.离子键 B.共价键 C.氢键 D.金属键 E.范德华力
(6)磷化硼(BP)可作为金属表面的保护薄膜,其晶胞如图所示,在BP晶胞中P占据的是硼原子堆积的

您最近一年使用:0次
2020-04-09更新
|
197次组卷
|
2卷引用:重庆巴蜀中学高2020届高三下学期3月月月考理综化学试题



