名校
解题方法
1 . 下列说法错误的是
| A.羊毛织品洗后易变形,与氢键有关 |
B.基态 原子中,两种自旋状态的电子数之比为 原子中,两种自旋状态的电子数之比为 |
C.键角: |
D. 二甲醚 二甲醚 中 中 杂化的原子数为2NA 杂化的原子数为2NA |
您最近一年使用:0次
2022-11-18更新
|
431次组卷
|
3卷引用:化学(重庆A卷)-学易金卷:2023年高考第一次模拟考试卷
(已下线)化学(重庆A卷)-学易金卷:2023年高考第一次模拟考试卷山东省济南市2022-2023学年高三上学期期中考试化学试题江苏省南京市第二十九中学2022-2023学年高二下学期期中考试化学试题
名校
解题方法
2 . 秦始皇帝陵博物院首次在兵马俑的彩绘中发现了古人人工合成的“中国蓝”“中国紫”颜料。人们对这些颜料的研究发现,其成分主要是钡和铜的硅酸盐(BaCuSixOy)。
回答下列问题:
(1)基态铜原子的电子排布式为____ 。“中国蓝”的发色中心是以Cu2+为中心的配位化合物,形成该配位键,Cu2+提供____ ,若“中国蓝”的化学组成中x:y=1:3,则其化学式为____ 。
(2)“中国蓝”“中国紫”中存在SiO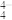 四面体结构,其中Si原子采取的杂化类型为
四面体结构,其中Si原子采取的杂化类型为___ 。与SiO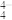 不同,CO
不同,CO 的立体构型为
的立体构型为____ 。
(3)C和Si同主族,但CO2与SiO2的熔沸点差异很大,这是因为CO2是____ 晶体,而SiO2是___ 晶体。
(4)MgO的熔沸点____ BaO(填“>”“<”“=”),原因是____ 。
(5)立方CuO晶胞结构如图所示。晶胞参数为a pm,NA代表阿伏加德罗常数的值。则两个距离最近Cu2+之间的距离为____ pm(用代数式表示),其晶体密度为____ (用代数式表示)。

回答下列问题:
(1)基态铜原子的电子排布式为
(2)“中国蓝”“中国紫”中存在SiO
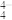 四面体结构,其中Si原子采取的杂化类型为
四面体结构,其中Si原子采取的杂化类型为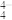 不同,CO
不同,CO 的立体构型为
的立体构型为(3)C和Si同主族,但CO2与SiO2的熔沸点差异很大,这是因为CO2是
(4)MgO的熔沸点
(5)立方CuO晶胞结构如图所示。晶胞参数为a pm,NA代表阿伏加德罗常数的值。则两个距离最近Cu2+之间的距离为

您最近一年使用:0次
2022-11-13更新
|
195次组卷
|
3卷引用:重庆市缙云教育联盟2022-2023学年高二上学期期末联考化学试题
名校
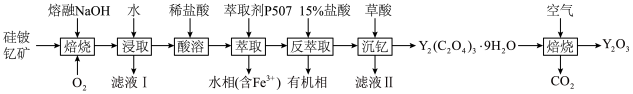
3 . 钇(Y)是稀土元素中含量丰富的元素之一,钇及其化合物在航天、电子、超导等方面有着广泛的应用。湖北应山-大悟地区含有较为丰富硅铍钇矿[ ],工业上通过如下生产流程可获得氧化钇。
],工业上通过如下生产流程可获得氧化钇。
已知: 元素与
元素与 元素性质相似;草酸可与多种过渡金属离子形成可溶性配位化合物;
元素性质相似;草酸可与多种过渡金属离子形成可溶性配位化合物;
(1)在自然界中,钇只有一种稳定同位素 ,Y位于元素周期表的第
,Y位于元素周期表的第_______ 周期第ⅢB族。硅铍钇矿[ ]中Y的化合价为+3价,
]中Y的化合价为+3价, 的化合价为
的化合价为_______ 。
(2)焙烧的目的是将矿石中的Y元素转化为 ,并将
,并将 元素转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是
元素转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是_______ 。硅铍钇矿与熔融氢氧化钠焙烧后含铁元素的产物是_______ (写化学式)。
(3)“萃取分液”实验需要的玻璃仪器有_______ 。
(4)滤液Ⅱ中的_______ (填物质名称)可参与循环使用。
(5)反应过程中,测得Y的沉淀率随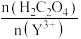 的变化情况如图所示。当草酸用量过多时,钇的沉淀率下降的原因是
的变化情况如图所示。当草酸用量过多时,钇的沉淀率下降的原因是_______ 。

(6)“焙烧”过程生成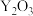 的化学方程式为
的化学方程式为_______ 。
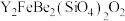 ],工业上通过如下生产流程可获得氧化钇。
],工业上通过如下生产流程可获得氧化钇。
已知:
 元素与
元素与 元素性质相似;草酸可与多种过渡金属离子形成可溶性配位化合物;
元素性质相似;草酸可与多种过渡金属离子形成可溶性配位化合物;(1)在自然界中,钇只有一种稳定同位素
 ,Y位于元素周期表的第
,Y位于元素周期表的第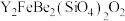 ]中Y的化合价为+3价,
]中Y的化合价为+3价, 的化合价为
的化合价为(2)焙烧的目的是将矿石中的Y元素转化为
 ,并将
,并将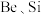 元素转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是
元素转化为可溶性钠盐,焙烧时气体与矿料逆流而行,目的是(3)“萃取分液”实验需要的玻璃仪器有
(4)滤液Ⅱ中的
(5)反应过程中,测得Y的沉淀率随
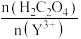 的变化情况如图所示。当草酸用量过多时,钇的沉淀率下降的原因是
的变化情况如图所示。当草酸用量过多时,钇的沉淀率下降的原因是
(6)“焙烧”过程生成
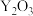 的化学方程式为
的化学方程式为
您最近一年使用:0次
2022-11-10更新
|
474次组卷
|
5卷引用:化学(重庆A卷)-学易金卷:2023年高考第一次模拟考试卷
(已下线)化学(重庆A卷)-学易金卷:2023年高考第一次模拟考试卷湖北省宜城一中、枣阳一中等六校联考2022-2023学年高三上学期期中考试化学试题湖南株洲南方中学2022-2023学年高三第四次月考化学试题湖南师范大学附属中学2023-2024学年高二上学期入学考试化学试题 (已下线)工业流程题
4 . 第三代半导体材料以碳化硅和氮化镓为主,广泛应用于新能源汽车、高铁等领域。
(1)基态Si原子的价电子排布图为_______ 。
(2)C、N、Si的第一电离能由大到小的顺序是_______ (填元素符号)。
(3) 的空间构型为
的空间构型为_______ ,其中碳原子的杂化轨道类型为_______ 。
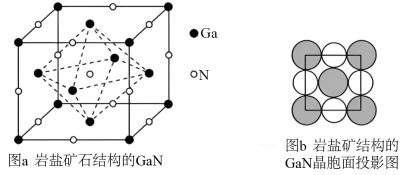
(4)岩盐矿结构的GaN晶体结构如图a、图b所示,Ga、N原子半径分别为 、
、 ,则Ga原子的配位数为
,则Ga原子的配位数为_______ ,设阿伏加德罗常数的值为NA,则该GaN的密度是_______  (列出算式)。
(列出算式)。
(5)煤的气化是一种重要的制氢途径。在一定温度下:向体积固定的密闭容器中加入足量的 和1mol
和1mol ,发生下列反应生成水煤气:
,发生下列反应生成水煤气:
Ⅰ.

Ⅱ.

反应平衡时, 的转化率为50%,CO的物质的量为0.1mol。
的转化率为50%,CO的物质的量为0.1mol。
①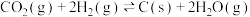

_______ 。
②下列说法正确的是_______ 。
A.将炭块粉碎,可加快反应速率
B.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
C.混合气体的密度保持不变时,说明反应体系已达到平衡
D.平衡时 的体积分数可能大于
的体积分数可能大于
③求反应Ⅱ的平衡常数K=_______ 。
(1)基态Si原子的价电子排布图为
(2)C、N、Si的第一电离能由大到小的顺序是
(3)
 的空间构型为
的空间构型为(4)岩盐矿结构的GaN晶体结构如图a、图b所示,Ga、N原子半径分别为
 、
、 ,则Ga原子的配位数为
,则Ga原子的配位数为 (列出算式)。
(列出算式)。
(5)煤的气化是一种重要的制氢途径。在一定温度下:向体积固定的密闭容器中加入足量的
 和1mol
和1mol ,发生下列反应生成水煤气:
,发生下列反应生成水煤气:Ⅰ.


Ⅱ.


反应平衡时,
 的转化率为50%,CO的物质的量为0.1mol。
的转化率为50%,CO的物质的量为0.1mol。①
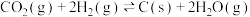

②下列说法正确的是
A.将炭块粉碎,可加快反应速率
B.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
C.混合气体的密度保持不变时,说明反应体系已达到平衡
D.平衡时
 的体积分数可能大于
的体积分数可能大于
③求反应Ⅱ的平衡常数K=
您最近一年使用:0次
名校
5 . 双香豆素是一种重要的抗凝血药物,可用于防治血栓形成,其结构如图所示。下列说法正确的是


| A.双香豆素中有3种杂化类型的碳原子 |
| B.双香豆素有4种一氯代物 |
| C.双香豆素可以形成分子内氢键 |
D.用香豆素( )和HCHO合成双香豆素反应的原子利用率为100% )和HCHO合成双香豆素反应的原子利用率为100% |
您最近一年使用:0次
2022-11-06更新
|
252次组卷
|
2卷引用:重庆市2022-2023学年高三上学期第三次质量检测化学试题
6 . 反应 可应用于解决冬季开采石油井下结蜡难题。下列说法正确的是
可应用于解决冬季开采石油井下结蜡难题。下列说法正确的是
 可应用于解决冬季开采石油井下结蜡难题。下列说法正确的是
可应用于解决冬季开采石油井下结蜡难题。下列说法正确的是A. 的空间构型为三角锥型 的空间构型为三角锥型 | B. 中仅含离子键 中仅含离子键 |
C. 仅为氧化产物 仅为氧化产物 | D.该反应的 |
您最近一年使用:0次
名校
解题方法
7 . 下列化学用语或图示表达正确的是
A.NaCl的电子式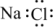 | B.基态氧原子价电子排布图: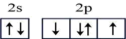 |
C.CO 的空间结构模型 的空间结构模型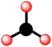 | D.p—pσ键电子云轮廓图 |
您最近一年使用:0次
2022-11-02更新
|
260次组卷
|
2卷引用:重庆市第八中学校2023届高三上学期高考适应性月考卷(四)化学试题
名校
解题方法
8 . 金属在史前就为人们所知,金属单质及其化合物的使用推动了人类文明的发展。回答下列问题:
(1)基态As原子价电子排布图为_______ ,电子占据最高能级的电子云轮廓图形状为_______ 。
(2)AsH3的空间构型为_______ 。
(3)绿矾(FeSO4⋅7H2O)结构如下图。
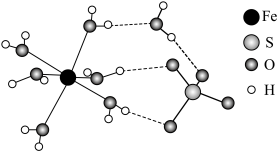
①H2O分别与Fe2+、SO 的相互作用分别为
的相互作用分别为_______ 、_______ 。
②比较SO 中的∠O—S—O
中的∠O—S—O_______ H2O中的∠H—O—H。(填“<”“>”或“=”)
(4)现在国家大力推行新能源,其中锂电池得到了巨大的发展。为了增强钴酸锂电池的安全性,科学家根据铁与钴性质的相似性,又研发出了磷酸亚铁锂电池。
①Fe在元素周期表中的位置是_______ 。
②磷青铜晶体的晶胞结构如图所示。
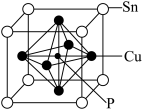
该晶体的化学式为_______ 。
(1)基态As原子价电子排布图为
(2)AsH3的空间构型为
(3)绿矾(FeSO4⋅7H2O)结构如下图。

①H2O分别与Fe2+、SO
 的相互作用分别为
的相互作用分别为②比较SO
 中的∠O—S—O
中的∠O—S—O(4)现在国家大力推行新能源,其中锂电池得到了巨大的发展。为了增强钴酸锂电池的安全性,科学家根据铁与钴性质的相似性,又研发出了磷酸亚铁锂电池。
①Fe在元素周期表中的位置是
②磷青铜晶体的晶胞结构如图所示。

该晶体的化学式为
您最近一年使用:0次
名校
解题方法
9 . 类比是学习化学的重要方法,下列类比结果合理的是
| 选项 | 已知 | 结论 |
| A | 沸点: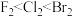 | 沸点:HF<HCl<HBr |
| B | 酸性: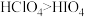 | 酸性:HCl>HI |
| C |  的分子构型为V形 的分子构型为V形 | 二甲醚的分子骨架(C—O—C)构型为V形 |
| D | 溶解度: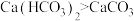 | 溶解度: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 .  代表阿伏加德罗常数的值,下列说法不正确的是
代表阿伏加德罗常数的值,下列说法不正确的是
 代表阿伏加德罗常数的值,下列说法不正确的是
代表阿伏加德罗常数的值,下列说法不正确的是A.1mol 分子中含有 分子中含有 键数为 键数为 |
B.向氨水中滴加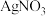 溶液可得到 溶液可得到 , , 含配位键数目为 含配位键数目为 |
C.电解熔融 ,阴极增重5.4g,外电路中通过电子的数目为 ,阴极增重5.4g,外电路中通过电子的数目为 |
D.标准状况下,11.2L 和22.4L 和22.4L 在光照条件下充分反应后的分子数为 在光照条件下充分反应后的分子数为 |
您最近一年使用:0次



