解题方法
1 . “类推”是一种重要的学习方法,但有时会产生错误,下列类推得到的结论正确的是
A.从CH4、NH 、SO 、SO 为正四面体结构,可推测PH 为正四面体结构,可推测PH 、PO 、PO 也为正四面体结构 也为正四面体结构 |
| B.H2O常温下为液态,H2S常温下也为液态 |
| C.金刚石中C-C键的键长为154.45pm,C60中C-C键的键长为140~145pm,所以C60的熔点高于金刚石 |
| D.CH4和P4都为正四面体形,CH4中键角为109°28ˊ,P4中键角也为109°28ˊ |
您最近一年使用:0次
2 . 配合物[Cu(NH3)4](OH)2的中心离子、配体、中心离子的电荷数和配位数分别为
| A.Cu2+、OH-、2+、2 | B.Cu+、NH3、1+、4 |
| C.Cu2+、NH3、2+、4 | D.Cu2+、NH3、2+、2 |
您最近一年使用:0次
2022-09-25更新
|
156次组卷
|
2卷引用:重庆市二0三中学校2021-2022学年高二下学期3月月考化学试题
名校
解题方法
3 . 用氧化镍矿石(主要成分为 ,还含有少量
,还含有少量 、
、 等)制备
等)制备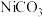 的某种工艺流程如图:
的某种工艺流程如图:

回答下列问题:
(1)“浸取”时,往往需要将矿石粉碎并适当升温,其目的为___________ ,加入 的离子反应方程式为
的离子反应方程式为___________ ,过量的 不需要另外除去,因为
不需要另外除去,因为___________ 。
(2)“除杂”时,加入 的目的是为了除去
的目的是为了除去___________ (填离子符号)。
(3)“沉镍”时产生无色无味的气体A,该反应的化学方程式为___________ ,“沉镍”时选用 而不直接用
而不直接用 ,原因是
,原因是___________ 。
(4)滤液3可在___________ 流程操作中循环使用。
 ,还含有少量
,还含有少量 、
、 等)制备
等)制备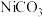 的某种工艺流程如图:
的某种工艺流程如图:
回答下列问题:
(1)“浸取”时,往往需要将矿石粉碎并适当升温,其目的为
 的离子反应方程式为
的离子反应方程式为 不需要另外除去,因为
不需要另外除去,因为(2)“除杂”时,加入
 的目的是为了除去
的目的是为了除去(3)“沉镍”时产生无色无味的气体A,该反应的化学方程式为
 而不直接用
而不直接用 ,原因是
,原因是(4)滤液3可在
您最近一年使用:0次
名校
解题方法
4 . 下列各组离子在给定溶液中一定能大量共存的是
A.与金属铝反应产生 的溶液中: 的溶液中: |
B.含有大量 的溶液中: 的溶液中: |
C.在 的氢氧化钡溶液中: 的氢氧化钡溶液中: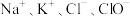 |
D.能使甲基橙变红的溶液中: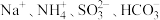 |
您最近一年使用:0次
名校
解题方法
5 . 下列化学用语书写正确的是
A.过氧化钠的电子式: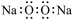 | B.乙烷的结构式: |
C. 的结构示意图: 的结构示意图: | D.氨气分子的空间充填模型: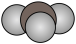 |
您最近一年使用:0次
2022-09-25更新
|
222次组卷
|
2卷引用:重庆市第八中学2023届高三上学期适应性月考卷(一)化学试题
名校
解题方法
6 . 在“碳达峰、碳中和”的大背景下,实现 的有效转化成为科研工作者的研究热点,以下是几种常见的
的有效转化成为科研工作者的研究热点,以下是几种常见的 利用方法:
利用方法:
I.以 作催化剂,可使
作催化剂,可使 在温和条件下转化为甲醇,反应经历如下过程:
在温和条件下转化为甲醇,反应经历如下过程:
i.催化剂活化: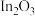 (无活性)
(无活性)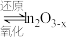 (有活性);
(有活性);
ii. 与
与 在活化的催化剂表面发生反应①:
在活化的催化剂表面发生反应①:
 ,同时也有反应②:
,同时也有反应②:
 等副反应发生。
等副反应发生。
(1)反应①中碳原子的杂化方式变化情况为___________ 。
(2)某温度下,在恒容反应器中,能说明反应①达到平衡状态的是___________(填序号)。
(3)某温度下, 与
与 的混合气体以不同流速通过恒容反应器,气体流速与
的混合气体以不同流速通过恒容反应器,气体流速与 转化率、
转化率、 选择性的关系如图,(已知:
选择性的关系如图,(已知: 选择性
选择性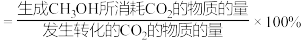 )
) 选择性随气体流速增大而升高的原因可能有:
选择性随气体流速增大而升高的原因可能有:
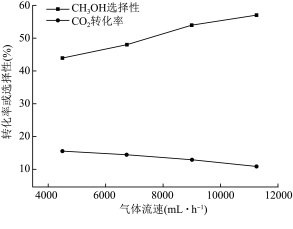
①___________ 。
②气体流速增大可减少产物中 的积累,减少催化剂的失活,从而提高
的积累,减少催化剂的失活,从而提高 选择性,请用化学方程式表示催化剂失活的原因:
选择性,请用化学方程式表示催化剂失活的原因:___________ 。
(4)碳酸氢盐分解可获得 ,在T℃时,将足量的某碳酸氢盐
,在T℃时,将足量的某碳酸氢盐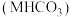 固体置于真空恒容容器中,存在如下平衡:
固体置于真空恒容容器中,存在如下平衡: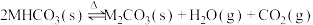 。上述反应达平衡时体系的总压为
。上述反应达平衡时体系的总压为 。保持温度不变,开始时在体系中先通入一定量的
。保持温度不变,开始时在体系中先通入一定量的 ,再加入足量
,再加入足量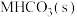 ,欲使平衡时体系中水蒸气的分压小于
,欲使平衡时体系中水蒸气的分压小于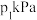 ,则开始时通入
,则开始时通入 的初始压强应大于
的初始压强应大于___________ 。
II.一种以甲醇和二氧化碳为原料,利用活性催化电极,电化学法制备甲酸(甲酸盐),其工作原理如图所示。
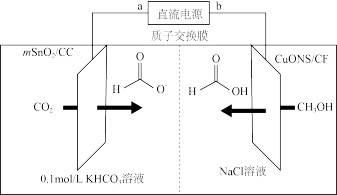
(5)①b极为直流电源的___________ 极,写出电解过程中阴极表面发生的电极反应式:___________ 。
②若有1mol 通过质子交换膜时,该装置内生成
通过质子交换膜时,该装置内生成 和HCOOH共计
和HCOOH共计___________ mol。
 的有效转化成为科研工作者的研究热点,以下是几种常见的
的有效转化成为科研工作者的研究热点,以下是几种常见的 利用方法:
利用方法:I.以
 作催化剂,可使
作催化剂,可使 在温和条件下转化为甲醇,反应经历如下过程:
在温和条件下转化为甲醇,反应经历如下过程:i.催化剂活化:
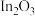 (无活性)
(无活性)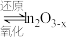 (有活性);
(有活性);ii.
 与
与 在活化的催化剂表面发生反应①:
在活化的催化剂表面发生反应①:
 ,同时也有反应②:
,同时也有反应②:
 等副反应发生。
等副反应发生。(1)反应①中碳原子的杂化方式变化情况为
(2)某温度下,在恒容反应器中,能说明反应①达到平衡状态的是___________(填序号)。
A.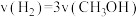 |
| B.混合气体的平均摩尔质量不变 |
| C.混合气体的密度不变 |
D. 和 和 的分压相等 的分压相等 |
 与
与 的混合气体以不同流速通过恒容反应器,气体流速与
的混合气体以不同流速通过恒容反应器,气体流速与 转化率、
转化率、 选择性的关系如图,(已知:
选择性的关系如图,(已知: 选择性
选择性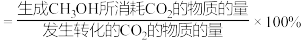 )
) 选择性随气体流速增大而升高的原因可能有:
选择性随气体流速增大而升高的原因可能有:
①
②气体流速增大可减少产物中
 的积累,减少催化剂的失活,从而提高
的积累,减少催化剂的失活,从而提高 选择性,请用化学方程式表示催化剂失活的原因:
选择性,请用化学方程式表示催化剂失活的原因:(4)碳酸氢盐分解可获得
 ,在T℃时,将足量的某碳酸氢盐
,在T℃时,将足量的某碳酸氢盐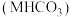 固体置于真空恒容容器中,存在如下平衡:
固体置于真空恒容容器中,存在如下平衡: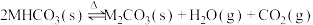 。上述反应达平衡时体系的总压为
。上述反应达平衡时体系的总压为 。保持温度不变,开始时在体系中先通入一定量的
。保持温度不变,开始时在体系中先通入一定量的 ,再加入足量
,再加入足量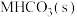 ,欲使平衡时体系中水蒸气的分压小于
,欲使平衡时体系中水蒸气的分压小于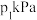 ,则开始时通入
,则开始时通入 的初始压强应大于
的初始压强应大于II.一种以甲醇和二氧化碳为原料,利用活性催化电极,电化学法制备甲酸(甲酸盐),其工作原理如图所示。

(5)①b极为直流电源的
②若有1mol
 通过质子交换膜时,该装置内生成
通过质子交换膜时,该装置内生成 和HCOOH共计
和HCOOH共计
您最近一年使用:0次
2022-09-25更新
|
368次组卷
|
2卷引用:重庆市巴蜀中学校2022-2023学年高三上学期适应性月考卷(二)化学试题
名校
7 . 制备铁触媒的主要原料三草酸合铁酸钾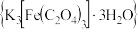 可在光照下发生分解:
可在光照下发生分解: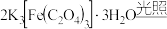
 。
。 中每个配体
中每个配体 中两个单键氧向中心
中两个单键氧向中心 配位,下列说法错误的是
配位,下列说法错误的是
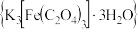 可在光照下发生分解:
可在光照下发生分解: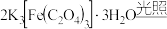
 。
。 中每个配体
中每个配体 中两个单键氧向中心
中两个单键氧向中心 配位,下列说法错误的是
配位,下列说法错误的是A. 的基态价电子排布图为 的基态价电子排布图为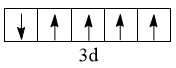 |
B. 中O原子的杂化方式为 中O原子的杂化方式为 |
C.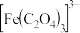 的中心离子的配位数为6 的中心离子的配位数为6 |
D. 分子中 分子中 键和 键和 键数目比为1:1 键数目比为1:1 |
您最近一年使用:0次
2022-09-25更新
|
342次组卷
|
3卷引用:重庆市巴蜀中学校2022-2023学年高三上学期适应性月考卷(二)化学试题
解题方法
8 . 一水合甘氨酸锌是一种矿物类饲料添加剂,其结构简式如图所示。下列说法错误的是


A.基态Zn原子价电子排布式为 |
B.Cu与Zn相邻,第一电离能: |
C.该物质中, 的配位数为5,配原子为O、N 的配位数为5,配原子为O、N |
D.电负性由小到大的顺序为 |
您最近一年使用:0次
2022-09-24更新
|
604次组卷
|
3卷引用:重庆第二十三中学校2021-2022学年高二下学期第一次月考化学试题
名校
9 . 虎年春晚上,一段舞蹈诗剧《只此青绿》生动还原了北宋画家王希孟的绝世之作——《千里江山图》。它之所以能够流传千年依旧色彩艳丽,璀璨夺目,与其绘制方法和所用颜料有关。
(1)绘制时,第一遍先用水墨画好山水画,第二遍上红色(赭石色),赭石主含 ,为后面的绿色做铺垫,冷暖对比,使其更鲜亮。基态氧原子核外电子的运动状态有
,为后面的绿色做铺垫,冷暖对比,使其更鲜亮。基态氧原子核外电子的运动状态有______ 种,三价铁离子的价电子排布式为______ 。
(2)第三遍上石绿(孔雀石或绿松石),孔雀石主要成分是碱式碳酸铜,化学式为: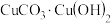 。碳酸根离子的空间构型为
。碳酸根离子的空间构型为______ 。
(3)绿松石是一种含水的铜铝酸盐矿物,属于磷酸盐矿物,化学式为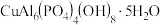 。直链多磷酸根阴离子是由两个或两个以上磷氧四面体通过共用顶角氧原子连接起来的,其结构如图所示。则由n个磷氧四面体形成的这类磷酸根离子的通式为
。直链多磷酸根阴离子是由两个或两个以上磷氧四面体通过共用顶角氧原子连接起来的,其结构如图所示。则由n个磷氧四面体形成的这类磷酸根离子的通式为______ 。

(4)第四遍还要再叠加一层绿,第五遍上青色,石青(蓝铜矿或青金石),蓝铜矿化学式为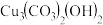 ,青金石是碱性铝硅酸盐矿物,化学式为
,青金石是碱性铝硅酸盐矿物,化学式为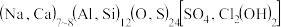 。
。
① 与
与 结合能生成
结合能生成 ,
, 中配位原子为
中配位原子为______ (用元素符号表示) 。
②根据价层电子对互斥理论, 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是______ 。 的熔沸点比
的熔沸点比 高很多,主要原因是
高很多,主要原因是______ 。
(5)《千里江山图》中还用到了黄色的颜料䧳黄,雌黄的主要成分是 ,有剧毒。
,有剧毒。
① 、
、 、
、 的键角由大到小的顺序为
的键角由大到小的顺序为______ 。
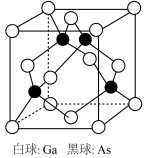
②砷化镓晶胞如图所示,若两个镓原子之间的最近距离为d pm, 代表阿伏加德罗常数的值,则砷化镓晶体的密度
代表阿伏加德罗常数的值,则砷化镓晶体的密度
______  。(用含d,
。(用含d, 的代数式表示)
的代数式表示)
(1)绘制时,第一遍先用水墨画好山水画,第二遍上红色(赭石色),赭石主含
 ,为后面的绿色做铺垫,冷暖对比,使其更鲜亮。基态氧原子核外电子的运动状态有
,为后面的绿色做铺垫,冷暖对比,使其更鲜亮。基态氧原子核外电子的运动状态有(2)第三遍上石绿(孔雀石或绿松石),孔雀石主要成分是碱式碳酸铜,化学式为:
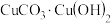 。碳酸根离子的空间构型为
。碳酸根离子的空间构型为(3)绿松石是一种含水的铜铝酸盐矿物,属于磷酸盐矿物,化学式为
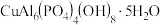 。直链多磷酸根阴离子是由两个或两个以上磷氧四面体通过共用顶角氧原子连接起来的,其结构如图所示。则由n个磷氧四面体形成的这类磷酸根离子的通式为
。直链多磷酸根阴离子是由两个或两个以上磷氧四面体通过共用顶角氧原子连接起来的,其结构如图所示。则由n个磷氧四面体形成的这类磷酸根离子的通式为
(4)第四遍还要再叠加一层绿,第五遍上青色,石青(蓝铜矿或青金石),蓝铜矿化学式为
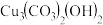 ,青金石是碱性铝硅酸盐矿物,化学式为
,青金石是碱性铝硅酸盐矿物,化学式为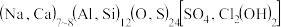 。
。①
 与
与 结合能生成
结合能生成 ,
, 中配位原子为
中配位原子为②根据价层电子对互斥理论,
 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是 的熔沸点比
的熔沸点比 高很多,主要原因是
高很多,主要原因是(5)《千里江山图》中还用到了黄色的颜料䧳黄,雌黄的主要成分是
 ,有剧毒。
,有剧毒。①
 、
、 、
、 的键角由大到小的顺序为
的键角由大到小的顺序为②砷化镓晶胞如图所示,若两个镓原子之间的最近距离为d pm,
 代表阿伏加德罗常数的值,则砷化镓晶体的密度
代表阿伏加德罗常数的值,则砷化镓晶体的密度
 。(用含d,
。(用含d, 的代数式表示)
的代数式表示)
您最近一年使用:0次
2022-09-22更新
|
1171次组卷
|
4卷引用:重庆南开中学2023届高三上学期9月月考化学试题
重庆南开中学2023届高三上学期9月月考化学试题浙江省东阳中学2023届高三浙江省普通高校招生选考科目考试仿真训练化学试题(已下线)专题02 物质结构专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)(已下线)浙江省温州市普通高中2023届高三下学期第二次适应性考试化学试题变式题(结构与性质)
解题方法
10 . 硼元素及其化合物具有各异的结构与性质。氮化硼(BN)晶体有多种相结构。六方相氮化硼(I)与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼(II)是超硬材料,有优异的耐磨性。它们的晶体结构如下图所示。
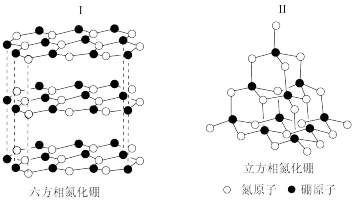
(1)基态硼原子的电子排布式为_______ ,同周期中第一电离能小于硼的元素有_______ 种。
(2)关于这两种晶体的说法,正确的是_______ (填序号)。
a.I中存在分子间作用力 b.II含有σ键和π键,所以硬度大
c.I与II结构中B:B−N的值相同 d.两种晶体中的B−N键均为共价键
(3)I中硼原子的杂化轨道类型为_______ ,判断其是否导电并说明原因_______ 。
(4)常温常压下硼酸( )晶体结构为层状,其二维平面结构如图所示。1mol
)晶体结构为层状,其二维平面结构如图所示。1mol 晶体中含有
晶体中含有_______ mol氢键。
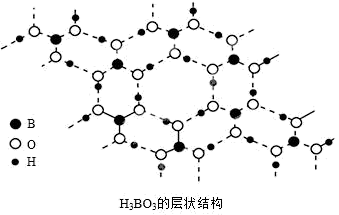
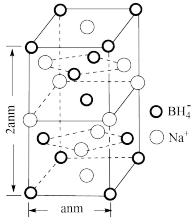
(5)硼氢化钠是一种常用的还原剂。其晶胞结构如图所示。回答下列问题:
① 分子中的O−B−O的键角
分子中的O−B−O的键角_______ (填“大于”“等于”或“小于”) 中的H−B−H的键角,判断依据是
中的H−B−H的键角,判断依据是_______ 。
②晶胞参数如图所示,已知晶胞密度为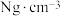 ,则阿伏加德罗常数可以表示为
,则阿伏加德罗常数可以表示为_________ ,(已知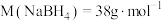 ,列出计算式即可);若硼氢化钠晶胞上下底心处的
,列出计算式即可);若硼氢化钠晶胞上下底心处的 被
被 取代,得到的晶体的化学式为
取代,得到的晶体的化学式为_______ 。

(1)基态硼原子的电子排布式为
(2)关于这两种晶体的说法,正确的是
a.I中存在分子间作用力 b.II含有σ键和π键,所以硬度大
c.I与II结构中B:B−N的值相同 d.两种晶体中的B−N键均为共价键
(3)I中硼原子的杂化轨道类型为
(4)常温常压下硼酸(
 )晶体结构为层状,其二维平面结构如图所示。1mol
)晶体结构为层状,其二维平面结构如图所示。1mol 晶体中含有
晶体中含有
(5)硼氢化钠是一种常用的还原剂。其晶胞结构如图所示。回答下列问题:

①
 分子中的O−B−O的键角
分子中的O−B−O的键角 中的H−B−H的键角,判断依据是
中的H−B−H的键角,判断依据是②晶胞参数如图所示,已知晶胞密度为
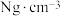 ,则阿伏加德罗常数可以表示为
,则阿伏加德罗常数可以表示为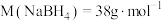 ,列出计算式即可);若硼氢化钠晶胞上下底心处的
,列出计算式即可);若硼氢化钠晶胞上下底心处的 被
被 取代,得到的晶体的化学式为
取代,得到的晶体的化学式为
您最近一年使用:0次



