名校
解题方法
1 . 铜元素是重要的金属元素,例如:黄铜矿(主要成分为 )是一种天然矿石;钡和铜的硅酸盐(
)是一种天然矿石;钡和铜的硅酸盐(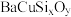 )可以人工合成“中国蓝”“中国紫”颜料。请回答下列问题:
)可以人工合成“中国蓝”“中国紫”颜料。请回答下列问题:
(1)基态Cu的价层电子排布式为___________ 。
(2)“中国蓝”“中国紫”中存在 ,其中Si原子采取的杂化类型为
,其中Si原子采取的杂化类型为___________ ;与 互为等电子体的离子是
互为等电子体的离子是___________ (写出一种化学式即可)。
(3)Si和C同主族,但 与
与 的熔沸点差异很大的原因为
的熔沸点差异很大的原因为___________ 。
(4) 在氨水溶液中可以形成
在氨水溶液中可以形成 ,
, 中含有的σ键数目为
中含有的σ键数目为___________ ;配体分子 键角大于
键角大于 的原因为
的原因为___________ 。
(5)四方晶系的 晶胞结构如图所示。
晶胞结构如图所示。

①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图中原子1的坐标为( ,
, ,
, ),则原子2的坐标为
),则原子2的坐标为___________ 。晶体中距离Fe最近的S有___________ 个。
②设阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为___________  (列出计算式即可)。
(列出计算式即可)。
 )是一种天然矿石;钡和铜的硅酸盐(
)是一种天然矿石;钡和铜的硅酸盐(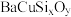 )可以人工合成“中国蓝”“中国紫”颜料。请回答下列问题:
)可以人工合成“中国蓝”“中国紫”颜料。请回答下列问题:(1)基态Cu的价层电子排布式为
(2)“中国蓝”“中国紫”中存在
 ,其中Si原子采取的杂化类型为
,其中Si原子采取的杂化类型为 互为等电子体的离子是
互为等电子体的离子是(3)Si和C同主族,但
 与
与 的熔沸点差异很大的原因为
的熔沸点差异很大的原因为(4)
 在氨水溶液中可以形成
在氨水溶液中可以形成 ,
, 中含有的σ键数目为
中含有的σ键数目为 键角大于
键角大于 的原因为
的原因为(5)四方晶系的
 晶胞结构如图所示。
晶胞结构如图所示。
①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图中原子1的坐标为(
 ,
, ,
, ),则原子2的坐标为
),则原子2的坐标为②设阿伏加德罗常数的值为
 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
名校
解题方法
2 . HCHO与[Zn(CN)4]2—在水溶液中发生反应:4HCHO+[Zn(CN)4]2—+4H++4H2O=[Zn(H2O)4]2-+4HOCH2CN,下列说法正确的是
| A.甲醛(HCHO)的键角约为120°,分子之间存在氢键 |
| B.HCN的空间构型为直线形,中心原子的杂化方式为sp |
| C.与Zn2+的配位能力:CN—<H2O |
| D.Zn2+与CN—-生成的配离子[Zn(CN)4]2-中,σ键和π键的数目之比为2:1 |
您最近一年使用:0次
2021-12-30更新
|
453次组卷
|
2卷引用:山东省威海乳山市2021-2022学年高二上学期期中考试化学试题
名校
3 . 利用共价三嗪框架作催化剂,将氧气转化为单线态氧(·O2)和超氧自由基(O2-·),·O2的协同下O ·可将苯甲醇氧化成苯甲醛,反应机理如图所示。下列有关说法正确的是
·可将苯甲醇氧化成苯甲醛,反应机理如图所示。下列有关说法正确的是
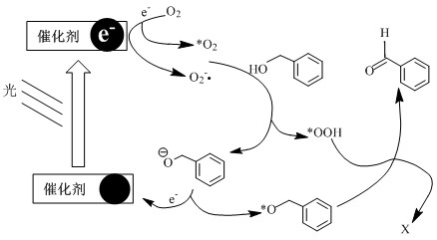
 ·可将苯甲醇氧化成苯甲醛,反应机理如图所示。下列有关说法正确的是
·可将苯甲醇氧化成苯甲醛,反应机理如图所示。下列有关说法正确的是
| A.X的化学式为H2O |
B.lmol 中σ键的数目为16×6.02×1023 中σ键的数目为16×6.02×1023 |
C. 向 向 的转化过程中有共价键的断裂与形成 的转化过程中有共价键的断裂与形成 |
| D.反应过程中,光能全部转化为化学能 |
您最近一年使用:0次
21-22高二·全国·课时练习
名校
解题方法
4 . 下列有机化合物中σ键与π键个数比为3∶2的是
| A.CH3CH3 | B.CH2=CH2 |
| C.CH≡CH | D.CH4 |
您最近一年使用:0次
2021-12-24更新
|
2260次组卷
|
17卷引用:1.1.2 有机化合物中的共价键-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修3)
(已下线)1.1.2 有机化合物中的共价键-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修3)山西省晋城市第一中学2021-2022学年高二上学期第五次调研化学试题(已下线)2.1.1 共价键-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)(已下线)2.1.1 共价键的类型——σ键和π键(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)陕西省西安中学2021-2022学年高二下学期期中考试化学试题陕西省宝鸡市金台区2021-2022学年高二下学期期中考试化学试题陕西省西安市蓝田县2021~2022学年高二下学期期末质量检测化学试题黑龙江省农垦建三江管理局第二高级中学2021-2022学年高二下学期期末考试化学试题黑龙江省哈尔滨师范大学青冈实验中学校2021-2022学年高二下学期开学考试化学试题吉林省吉林松花江中学2022-2023学年高二上学期1月期末考试化学试题贵州省贵阳清镇北大培文学校2022-2023学年高二下学期3月月考化学试题云南省丽江市2022-2023学年高二上学期期末考试化学试题天津市红桥区2022-2023学年高三上学期期末考试化学试题(已下线)第01讲 有机化合物的结构特点-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)陕西省宝鸡市扶风县法门高中2023-2024学年高二上学期期末考试化学试题(已下线)热点03 共价键山东省曹县博雅中学2022-2023学年高二上学期期末考试化学试题
名校
5 . 离子液体是在室温或接近室温时呈液态的盐类物质,应用广泛。1—乙基—3—甲基咪唑四氟硼酸盐离子液体结构如图所示,下列相关叙述错误的是
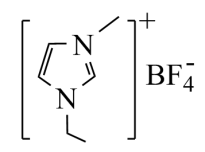
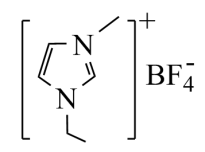
| A.该离子液体中C杂化方式为sp2和sp3 |
| B.阴离子呈正四面体形,存在共价键和配位键 |
| C.阳离子中σ键数目是π键数目的10倍 |
| D.该离子液体与水能够形成氢键 |
您最近一年使用:0次
6 . 设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.71gCl2与足量水反应,转移的电子数目为NA |
| B.78gNa2O2晶体所含阴阳离子的总数为4NA |
| C.标准状况下,22.4L15NH3含有的质子数目为10NA |
| D.1molN2中σ键的数目为3NA |
您最近一年使用:0次
7 . 有A、B、C、D、E五种元素的原子序数依次增大。A、B、C位于同一周期,A原子的第一电离能大于B原子,B原子的2p能级上有两个未成对电子,D位于第四周期且原子的d能级上没有电子,C与D形成的化合物为DC2。E原子的3d能级上电子数是4s能级上电子数的三倍。
(1)写出基态E3+的电子排布式___ 。
(2)A原子第一电离能大于B的原因___ 。
(3)一个A2C2分子中含个___ σ键,___ 个π键;AB 离子的空间构型为
离子的空间构型为___ 。
(4)上述五种元素的原子中电负性由大到小顺序是___ (填元素符号)。
(1)写出基态E3+的电子排布式
(2)A原子第一电离能大于B的原因
(3)一个A2C2分子中含个
 离子的空间构型为
离子的空间构型为(4)上述五种元素的原子中电负性由大到小顺序是
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
8 . 铬的同位素有 Cr、
Cr、 Cr、
Cr、 Cr、
Cr、 Cr。铬及其化合物在生活、生产中有广泛应用。回答下列问题:
Cr。铬及其化合物在生活、生产中有广泛应用。回答下列问题:
(1)基态 Cr的价层电子排布图为
Cr的价层电子排布图为___________ 。
(2)交警用“酒精仪”查酒驾,其化学反应原理为2K2Cr2O7+3CH3CH2OH+8H2SO4―→3CH3COOH+2Cr2(SO4)3+2K2SO4+11H2O。
①CH3CH2OH、CH3COOH的沸点高于对应的CH3OCH3(二甲醚)、HCOOCH3(甲酸甲酯),主要原因是___________ 。
②CH3COOH分子中碳原子的杂化类型是___________ ;CH3COOH分子中σ键和π键的数目之比为___________ 。
③K2SO4晶体中阴离子的立体构型是___________ 。
该反应中,只含极性键的极性分子有___________ (填分子式)。
(3)CrF3晶体、CrBr3晶体的熔点分别为1 100 ℃以上、79 ℃,其可能的原因是___________ 。
(4)晶体铬的晶胞结构如图所示,其堆积模型为___________ ;铬原子的配位数为___________ 。

 Cr、
Cr、 Cr、
Cr、 Cr、
Cr、 Cr。铬及其化合物在生活、生产中有广泛应用。回答下列问题:
Cr。铬及其化合物在生活、生产中有广泛应用。回答下列问题:(1)基态
 Cr的价层电子排布图为
Cr的价层电子排布图为(2)交警用“酒精仪”查酒驾,其化学反应原理为2K2Cr2O7+3CH3CH2OH+8H2SO4―→3CH3COOH+2Cr2(SO4)3+2K2SO4+11H2O。
①CH3CH2OH、CH3COOH的沸点高于对应的CH3OCH3(二甲醚)、HCOOCH3(甲酸甲酯),主要原因是
②CH3COOH分子中碳原子的杂化类型是
③K2SO4晶体中阴离子的立体构型是
该反应中,只含极性键的极性分子有
(3)CrF3晶体、CrBr3晶体的熔点分别为1 100 ℃以上、79 ℃,其可能的原因是
(4)晶体铬的晶胞结构如图所示,其堆积模型为

您最近一年使用:0次
2021高三·全国·专题练习
解题方法
9 . 根据所学知识回答下列问题:
(1)第一电离能氮___________ 氧(填“大于”“小于”或“等于”)。
(2)Cu+和Cu2+中较稳定的是___________ 。
(3) 的熔点低于
的熔点低于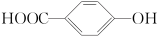 ,其原因是
,其原因是___________ 。
(4)已知无机含氧酸非羟基氧越多,酸性越强:0个非羟基氧是弱酸,1个非羟基氧是中强酸,2个非羟基氧是强酸。H3PO2是一种中强酸,则H3PO2的结构式为___________ 。
(5)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂,固态Ni(CO)4属于___________ 晶体,原子总数与价电子总数都相等的微粒互为等电子体,二者具有相似的化学键结构,如N2和CO。写出与CO互为等电子体的一种阴离子___________ ,Ni(CO)4中σ键与π键数目之比为___________ 。
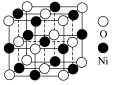
(6)立方氧化镍晶体的结构如图所示,其晶胞边长为a pm。氧化镍的化学式为___________ ,列式表示晶体的密度为___________ g·cm-3(不必计算出结果,阿伏加德罗常数的值为NA)。
(1)第一电离能氮
(2)Cu+和Cu2+中较稳定的是
(3)
 的熔点低于
的熔点低于 ,其原因是
,其原因是(4)已知无机含氧酸非羟基氧越多,酸性越强:0个非羟基氧是弱酸,1个非羟基氧是中强酸,2个非羟基氧是强酸。H3PO2是一种中强酸,则H3PO2的结构式为
(5)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂,固态Ni(CO)4属于
(6)立方氧化镍晶体的结构如图所示,其晶胞边长为a pm。氧化镍的化学式为

您最近一年使用:0次
名校
10 . 下列对分子结构及性质的叙述中正确的是
| A.四氯化碳萃取碘水中碘,HCl易溶于水都可用“相似相溶”原理解释 |
B.乳酸分子( )中不存在手性碳原子 )中不存在手性碳原子 |
C.P4( )和CH4分子的空间构型都是正四面体,键角都是109°28′,1molCH4和1molP4含有的σ键数目相同。 )和CH4分子的空间构型都是正四面体,键角都是109°28′,1molCH4和1molP4含有的σ键数目相同。 |
D.丙烯腈 分子中,碳原子的杂化方式有sp3、sp2 分子中,碳原子的杂化方式有sp3、sp2 |
您最近一年使用:0次



