解题方法
1 . 第二周期元素其单质及化合物具有一些特殊的化学性质。回答下列问题。
(1)Li、Be、B三种元素第二电离能由大到小的顺序为_______ 。
(2)由于硼的氢化物与烷烃相似,故又称之为硼烷。乙硼烷( )的分子结构如图,该分子中B原子的杂化方式为
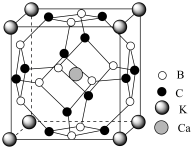
)的分子结构如图,该分子中B原子的杂化方式为_______ 。甲中化学键①为“二中心二电子键”,记作“2c-2e”,则乙硼烷的桥键②记作_______ 。氢原子仅用1s轨道就可形成桥键的原因为_______ 。_______ 。乙中由12个B与12个C构成的多面体含_______ 个棱。 溶解度(S=22g)大于
溶解度(S=22g)大于 (S=9.6g),从结构角度解释原因
(S=9.6g),从结构角度解释原因_______ 。
(1)Li、Be、B三种元素第二电离能由大到小的顺序为
(2)由于硼的氢化物与烷烃相似,故又称之为硼烷。乙硼烷(
 )的分子结构如图,该分子中B原子的杂化方式为
)的分子结构如图,该分子中B原子的杂化方式为
 溶解度(S=22g)大于
溶解度(S=22g)大于 (S=9.6g),从结构角度解释原因
(S=9.6g),从结构角度解释原因
您最近一年使用:0次
2 . 甲醛(HCHO)在化工、医药、农药等方面有广泛的应用。利用甲醇一定条件下直接脱氢可制甲醛,涉及的反应如下:
反应I:

反应II:

已知:①平衡状态下,甲醛选择性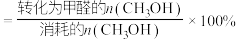 ;甲醛的收率
;甲醛的收率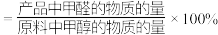 。
。
②几种物质的燃烧热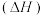 如下表:
如下表:
回答下列问题:
(1)
_______ ,HCHO的空间结构为_______ 形。
(2)反应I、反应II的反应历程可表示为:
历程i:……
历程ii: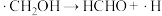
历程iii:
历程iv: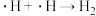
写出历程i的反应方程式:_______ 。
(3)将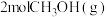 加入容积为2L的刚性密闭容器中,温度对平衡状态下
加入容积为2L的刚性密闭容器中,温度对平衡状态下 的选择性和收率的影响如图所示:
的选择性和收率的影响如图所示:_______ (填“I”或“II”),判断的依据是_______ 。
② ℃,反应进行到10min时达到平衡,此时
℃,反应进行到10min时达到平衡,此时 的转化率为
的转化率为_______ ,
_______ ,反应I的平衡常数
_______  。
。
反应I:


反应II:


已知:①平衡状态下,甲醛选择性
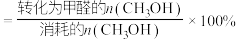 ;甲醛的收率
;甲醛的收率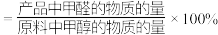 。
。②几种物质的燃烧热
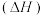 如下表:
如下表:| 物质 |  |  |  |  |
燃烧热 | -725.8 | -563.6 | -283.0 | -285.8 |
(1)

(2)反应I、反应II的反应历程可表示为:
历程i:……
历程ii:
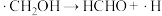
历程iii:

历程iv:
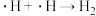
写出历程i的反应方程式:
(3)将
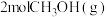 加入容积为2L的刚性密闭容器中,温度对平衡状态下
加入容积为2L的刚性密闭容器中,温度对平衡状态下 的选择性和收率的影响如图所示:
的选择性和收率的影响如图所示: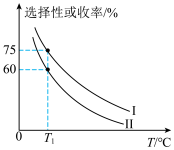
②
 ℃,反应进行到10min时达到平衡,此时
℃,反应进行到10min时达到平衡,此时 的转化率为
的转化率为

 。
。
您最近一年使用:0次
2024-06-01更新
|
273次组卷
|
3卷引用:2024届河南省周口市高三5月全真模拟理科综合试题-高中化学
名校
3 . 前四周期元素A、B、C、D、E的原子序数依次增大,基态A原子的核外电子占据3个能级且每个能级上电子数相等,基态C原子价层电子排布式为 ,C、D位于同主族,且基态D原子比基态C原子多2个电子能级,基态
,C、D位于同主族,且基态D原子比基态C原子多2个电子能级,基态 的核外电子占据的最高能层符号为M且其d轨道达到全充满结构,回答下列问题:
的核外电子占据的最高能层符号为M且其d轨道达到全充满结构,回答下列问题:
(1)基态E原子有___________ 种运动状态不同的电子,D位于元素周期表___________ 区。
(2)在A、B、C、D的简单氢化物中,沸点最高的是___________ (填化学式,下同);键角最大的是___________ 。
(3) 分子中D的杂化类型是
分子中D的杂化类型是___________ ;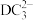 的空间结构为
的空间结构为___________ 。
(4)元素的基态气态原子得到一个电子形成 价气态阴离子时所放出的能量称为该元素的第一电子亲和能,单位为
价气态阴离子时所放出的能量称为该元素的第一电子亲和能,单位为 ,习惯规定,放出能量时电子亲和能为正值,吸收能量时电子亲和能为负值。电子亲和能越大,表明越容易得到电子,A、B、C元素的电子亲和能如图所示:
,习惯规定,放出能量时电子亲和能为正值,吸收能量时电子亲和能为负值。电子亲和能越大,表明越容易得到电子,A、B、C元素的电子亲和能如图所示:___________ 。
(5)B、E组成的一种立方晶胞如图2所示。已知晶胞参数为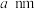 ,设
,设 为阿伏加德罗常数的值,该晶体化学式为
为阿伏加德罗常数的值,该晶体化学式为___________ ,该晶体密度为___________  。
。
 ,C、D位于同主族,且基态D原子比基态C原子多2个电子能级,基态
,C、D位于同主族,且基态D原子比基态C原子多2个电子能级,基态 的核外电子占据的最高能层符号为M且其d轨道达到全充满结构,回答下列问题:
的核外电子占据的最高能层符号为M且其d轨道达到全充满结构,回答下列问题:(1)基态E原子有
(2)在A、B、C、D的简单氢化物中,沸点最高的是
(3)
 分子中D的杂化类型是
分子中D的杂化类型是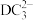 的空间结构为
的空间结构为(4)元素的基态气态原子得到一个电子形成
 价气态阴离子时所放出的能量称为该元素的第一电子亲和能,单位为
价气态阴离子时所放出的能量称为该元素的第一电子亲和能,单位为 ,习惯规定,放出能量时电子亲和能为正值,吸收能量时电子亲和能为负值。电子亲和能越大,表明越容易得到电子,A、B、C元素的电子亲和能如图所示:
,习惯规定,放出能量时电子亲和能为正值,吸收能量时电子亲和能为负值。电子亲和能越大,表明越容易得到电子,A、B、C元素的电子亲和能如图所示:
(5)B、E组成的一种立方晶胞如图2所示。已知晶胞参数为
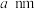 ,设
,设 为阿伏加德罗常数的值,该晶体化学式为
为阿伏加德罗常数的值,该晶体化学式为 。
。
您最近一年使用:0次
名校
解题方法
4 . 越王勾践剑是春秋晚期越国青铜器,此剑历经两千四百余年,仍锋利无比。经无损科学检测,其主要合金成分为铜、锡、铅、铁、硫,还含有少量的铝和微量的镍等。2017年,我国宣布成功完成性能优异的超级钢研制。这种超级钢造价低廉、具有优异的强度和延展性,其合金元素为锰、碳、铝、钒等。
(1)碳、锡(Sn)和铅均属___________ 族元素,其中锡的核电荷数比碳大44,则基态锡原子简化的核外电子排布式为___________ ,三者的原子半径依次递增,请解释原因___________ 。
(2)基态锰原子的价层电子轨道表示式为___________ 。
(3)硫代硫酸根离子可看作是硫酸根离子中的一个氧原子被硫原子取代的产物,则硫代硫酸根离子的空间构型是___________ ,硫代硫酸根离子作为配体可提供孤电子对与 形成
形成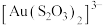 ,请判断硫代硫酸根离子中的两种硫原子
,请判断硫代硫酸根离子中的两种硫原子___________ (选填“中心硫原子”、“端基硫原子”、“均”)可以做配位原子。
(4)气态 通常以二聚体
通常以二聚体 的形式存在,
的形式存在, 气体中存在的作用力包含以下的
气体中存在的作用力包含以下的___________ (选填字母)。
a.离子键 b.配位键 c.π键 d.p-p σ键 e. -p σ键
-p σ键
(5) 的熔点为1090℃,远高于氯化铝的192℃,则
的熔点为1090℃,远高于氯化铝的192℃,则 的晶体类型为
的晶体类型为___________ 。
(6) 是一种常见催化剂,其晶胞结构如图,晶胞中黑球为
是一种常见催化剂,其晶胞结构如图,晶胞中黑球为___________ 原子(用元素符号表示)。
(1)碳、锡(Sn)和铅均属
(2)基态锰原子的价层电子轨道表示式为
(3)硫代硫酸根离子可看作是硫酸根离子中的一个氧原子被硫原子取代的产物,则硫代硫酸根离子的空间构型是
 形成
形成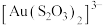 ,请判断硫代硫酸根离子中的两种硫原子
,请判断硫代硫酸根离子中的两种硫原子(4)气态
 通常以二聚体
通常以二聚体 的形式存在,
的形式存在, 气体中存在的作用力包含以下的
气体中存在的作用力包含以下的a.离子键 b.配位键 c.π键 d.p-p σ键 e.
 -p σ键
-p σ键(5)
 的熔点为1090℃,远高于氯化铝的192℃,则
的熔点为1090℃,远高于氯化铝的192℃,则 的晶体类型为
的晶体类型为(6)
 是一种常见催化剂,其晶胞结构如图,晶胞中黑球为
是一种常见催化剂,其晶胞结构如图,晶胞中黑球为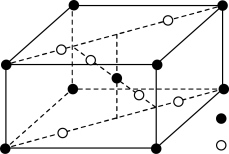
您最近一年使用:0次
5 . 氮、氧、磷、砷及其化合物在工农业生产等方面有着重要应用。请按要求回答下列问题。
(1)电负性P_______ As(填“>”或“<”或“=”)。
(2)尿素(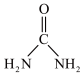 )中碳原子杂化类型
)中碳原子杂化类型_______ ; 离子的立体构型名称(即空间构型)为
离子的立体构型名称(即空间构型)为_______ 。
(3)AsH3是无色稍有大蒜味的气体。AsH3的沸点高于PH3,其主要原因是_______ 。
(4)我国的“天宫”空间站的核心舱“天和”选择了高效柔性砷化镓(GaAs)薄膜太阳能电池来供电。已知砷化镓的熔点为1238℃,GaAs的晶胞结构如图所示。_______ ,As与Ga之间存在的化学键有_______ (填字母)。
A.离子键 B.σ键 C.π键 D.氢键 E.配位键 F.金属键 G.极性键
②1号镓原子的坐标为_______ 。晶胞密度为dg∙cm-3,摩尔质量为Mg∙mol-1 ,阿伏加德罗常数的值用NA表示,则晶胞中最近的As和Ga原子核间距为_______ nm(列式表示)。
(1)电负性P
(2)尿素(
 )中碳原子杂化类型
)中碳原子杂化类型 离子的立体构型名称(即空间构型)为
离子的立体构型名称(即空间构型)为(3)AsH3是无色稍有大蒜味的气体。AsH3的沸点高于PH3,其主要原因是
(4)我国的“天宫”空间站的核心舱“天和”选择了高效柔性砷化镓(GaAs)薄膜太阳能电池来供电。已知砷化镓的熔点为1238℃,GaAs的晶胞结构如图所示。
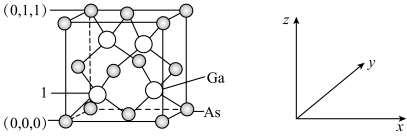
A.离子键 B.σ键 C.π键 D.氢键 E.配位键 F.金属键 G.极性键
②1号镓原子的坐标为
您最近一年使用:0次
名校
解题方法
6 . 氮、磷、砷 、锑
、锑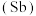 、铋
、铋 、镆
、镆 为元素周期表中原子序数依次增大的同主族元素。回答下列问题:
为元素周期表中原子序数依次增大的同主族元素。回答下列问题:
(1) 中
中 键和
键和 键的数目比例是
键的数目比例是___________ ,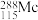 的中子数为
的中子数为___________ 。
(2)①已知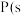 ,白磷)
,白磷) ,黑磷),该反应中
,黑磷),该反应中 的固态白磷转化为固态黑磷,放出
的固态白磷转化为固态黑磷,放出 的热量;
的热量;
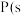 ,白磷)
,白磷) ,红磷),该反应中
,红磷),该反应中 的固态白磷转化为固态红磷,放出
的固态白磷转化为固态红磷,放出 的热量;
的热量;
由此推知,其中最稳定的磷单质是___________ 。
②比较氮和磷氢化物的热稳定性:
___________  (填“
(填“ ”“
”“ ”);写出
”);写出 结构式
结构式___________ 。
③ 与卤化氢的反应和
与卤化氢的反应和 与卤化氢的反应相似,产物的结构和性质也相似。
与卤化氢的反应相似,产物的结构和性质也相似。
下列对 与
与 反应产物的推断正确的是
反应产物的推断正确的是___________ (填序号)。
 不能与
不能与 反应
反应  含离子键、共价键
含离子键、共价键  受热易分解
受热易分解
(3)已知 溶于水后的电离方程式为
溶于水后的电离方程式为 ,若分别向上述混合体系中加入稀硫酸、
,若分别向上述混合体系中加入稀硫酸、 溶液,则生成的正盐的化学式分别为
溶液,则生成的正盐的化学式分别为___________ 、___________ 。
(4) 能与水以等物质的量之比发生较强烈的反应,生成难溶的
能与水以等物质的量之比发生较强烈的反应,生成难溶的 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 。
(5)某工厂采用辉铋矿(主要成分为 ,含有
,含有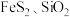 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )联合焙烧法制备
)联合焙烧法制备 和
和 ,工艺流程如图所示:
,工艺流程如图所示: 分解为
分解为 转变为
转变为 ;
;
②金属活动性: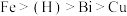 ;
;
③相关金属离子形成氢氧化物的 范围如下:
范围如下:
① 在元素周期表中的位置是
在元素周期表中的位置是___________ ,基态原子价层电子排布式为___________ 。
② 在空气中单独焙烧生成
在空气中单独焙烧生成 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
③滤渣的主要成分为___________ (填化学式)。
④生成气体 的离子方程式为
的离子方程式为___________ 。
⑤加入金属 的目的是
的目的是___________ 。
 、锑
、锑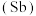 、铋
、铋 、镆
、镆 为元素周期表中原子序数依次增大的同主族元素。回答下列问题:
为元素周期表中原子序数依次增大的同主族元素。回答下列问题:(1)
 中
中 键和
键和 键的数目比例是
键的数目比例是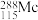 的中子数为
的中子数为(2)①已知
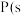 ,白磷)
,白磷) ,黑磷),该反应中
,黑磷),该反应中 的固态白磷转化为固态黑磷,放出
的固态白磷转化为固态黑磷,放出 的热量;
的热量;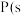 ,白磷)
,白磷) ,红磷),该反应中
,红磷),该反应中 的固态白磷转化为固态红磷,放出
的固态白磷转化为固态红磷,放出 的热量;
的热量;由此推知,其中最稳定的磷单质是
②比较氮和磷氢化物的热稳定性:

 (填“
(填“ ”“
”“ ”);写出
”);写出 结构式
结构式③
 与卤化氢的反应和
与卤化氢的反应和 与卤化氢的反应相似,产物的结构和性质也相似。
与卤化氢的反应相似,产物的结构和性质也相似。下列对
 与
与 反应产物的推断正确的是
反应产物的推断正确的是 不能与
不能与 反应
反应  含离子键、共价键
含离子键、共价键  受热易分解
受热易分解(3)已知
 溶于水后的电离方程式为
溶于水后的电离方程式为 ,若分别向上述混合体系中加入稀硫酸、
,若分别向上述混合体系中加入稀硫酸、 溶液,则生成的正盐的化学式分别为
溶液,则生成的正盐的化学式分别为(4)
 能与水以等物质的量之比发生较强烈的反应,生成难溶的
能与水以等物质的量之比发生较强烈的反应,生成难溶的 ,写出该反应的化学方程式
,写出该反应的化学方程式(5)某工厂采用辉铋矿(主要成分为
 ,含有
,含有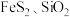 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )联合焙烧法制备
)联合焙烧法制备 和
和 ,工艺流程如图所示:
,工艺流程如图所示:
 分解为
分解为 转变为
转变为 ;
;②金属活动性:
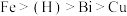 ;
;③相关金属离子形成氢氧化物的
 范围如下:
范围如下:开始沉淀 | 完全沉淀 | |
 | 6.5 | 8.3 |
 | 1.6 | 2.8 |
 | 8.1 | 10.1 |
 在元素周期表中的位置是
在元素周期表中的位置是②
 在空气中单独焙烧生成
在空气中单独焙烧生成 ,该反应的化学方程式为
,该反应的化学方程式为③滤渣的主要成分为
④生成气体
 的离子方程式为
的离子方程式为⑤加入金属
 的目的是
的目的是
您最近一年使用:0次
名校
解题方法
7 . 元素化学是化学的基石,不同的元素往往呈现出五彩缤纷的特性。回答下列问题:
(1) 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为___________ ,还原性由强到弱的顺序为___________ 。
(2)H、B、N、F四种元素可形成一种离子化合物,其阴、阳离子均为正四面体结构,阴、阳离子各含其中两种元素,写出一种符合要求的化学式:___________ 。
(3)金元素形成的部分离子氧化性很强,化学家们推测可能和“6s惰性电子对”效应有关,即失去6s电子对的离子会具有很强的氧化性。下列选项中具有此效应的离子是__________。
(4)已知 ,
, 的N原子杂化方式为
的N原子杂化方式为___________ ;比较键角 :
: 中的
中的
___________  中的
中的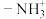 (填“
(填“ ”、“
”、“ ”或“
”或“ ”),请说明理由
”),请说明理由___________ 。
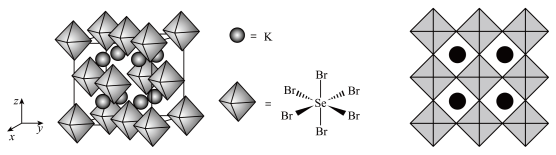
(5) 的晶体结构可以看成Ⅰ型结构和Ⅱ型结构的组合,已知Ⅰ型结构中As原子在内部,每个Ⅰ型和Ⅱ型结构可近似为边长相等的立方体。一个
的晶体结构可以看成Ⅰ型结构和Ⅱ型结构的组合,已知Ⅰ型结构中As原子在内部,每个Ⅰ型和Ⅱ型结构可近似为边长相等的立方体。一个 的晶胞中Ⅰ型结构和Ⅱ型结构的比例是
的晶胞中Ⅰ型结构和Ⅱ型结构的比例是___________ ;___________ 。
②设X的最简式的式量为 ,晶体密度为
,晶体密度为 ,则化合物X中相邻K之间的最短距离为
,则化合物X中相邻K之间的最短距离为___________ nm(列出计算式,阿伏加德罗常数的值为 )。
)。
(1)
 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为(2)H、B、N、F四种元素可形成一种离子化合物,其阴、阳离子均为正四面体结构,阴、阳离子各含其中两种元素,写出一种符合要求的化学式:
(3)金元素形成的部分离子氧化性很强,化学家们推测可能和“6s惰性电子对”效应有关,即失去6s电子对的离子会具有很强的氧化性。下列选项中具有此效应的离子是__________。
A. | B.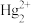 | C. | D. |
(4)已知
 ,
, 的N原子杂化方式为
的N原子杂化方式为 :
: 中的
中的
 中的
中的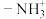 (填“
(填“ ”、“
”、“ ”或“
”或“ ”),请说明理由
”),请说明理由(5)
 的晶体结构可以看成Ⅰ型结构和Ⅱ型结构的组合,已知Ⅰ型结构中As原子在内部,每个Ⅰ型和Ⅱ型结构可近似为边长相等的立方体。一个
的晶体结构可以看成Ⅰ型结构和Ⅱ型结构的组合,已知Ⅰ型结构中As原子在内部,每个Ⅰ型和Ⅱ型结构可近似为边长相等的立方体。一个 的晶胞中Ⅰ型结构和Ⅱ型结构的比例是
的晶胞中Ⅰ型结构和Ⅱ型结构的比例是
②设X的最简式的式量为
 ,晶体密度为
,晶体密度为 ,则化合物X中相邻K之间的最短距离为
,则化合物X中相邻K之间的最短距离为 )。
)。
您最近一年使用:0次
名校
解题方法
8 . N、P同属于第VA族元素。试回答下列问题。
(1)基态N原子核外电子的空间运动状态有___________ 种。
(2)NH3分子可与Co3+形成配合物[Co(NH3)5Cl]Cl2,该配合物中H—N—H键角___________ (填“>”“<”或“=”)NH3分子中的H—N—H键角。1mol[Co(NH3)5Cl]Cl2中含有的σ键数目为___________ NA。
(3)磷和氢能组成一系列的氢化物,如PH3、P2H4、P12H16等。其中最重要的PH3。P2H4的沸点比PH3___________ (填“高”或“低”),原因是___________ 。
(4)乙二胺(H2NCH2CH2NH2)分子中氮原子的杂化类型为___________ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,其主要原因是___________ 。
(5)氮化硼、磷化铝、磷化镓(镓为第ⅢA族元素)晶胞结构都与金刚石的晶胞相似,熔点如下表所示,分析其变化的原因:___________ 。
(1)基态N原子核外电子的空间运动状态有
(2)NH3分子可与Co3+形成配合物[Co(NH3)5Cl]Cl2,该配合物中H—N—H键角
(3)磷和氢能组成一系列的氢化物,如PH3、P2H4、P12H16等。其中最重要的PH3。P2H4的沸点比PH3
(4)乙二胺(H2NCH2CH2NH2)分子中氮原子的杂化类型为
(5)氮化硼、磷化铝、磷化镓(镓为第ⅢA族元素)晶胞结构都与金刚石的晶胞相似,熔点如下表所示,分析其变化的原因:
| 物质 | 氮化硼 | 磷化铝 | 磷化镓 |
| 熔点 | 3000℃ | 2000℃ | 1477℃ |
您最近一年使用:0次
名校
解题方法
9 . 锗广泛应用于现代高新技术产业。某科研小组用氧化锌烟尘(主要成分为ZnO,含有ZnFe2O4、PbO、GeO2、GeS2、SiO2及少量As的化合物等)制取锗并回收锌的一种流程如下:
(1)浸渣的主要成分有S、PbSO4和___________ ;“浸出”后,锗元素以Ge4+形式存在于溶液中,写出“浸出”时GeS2所发生的离子反应方程式___________ 。
(2)单宁酸(H2L)“沉锗”时主要发生反应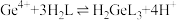 ,最佳pH=2.5,pH过低会导致
,最佳pH=2.5,pH过低会导致___________ ,使沉锗率下降;为提高沉锗速率,可采取的措施有___________ (写一种即可)。
(3)“蒸馏”得到的粗GeCl4中混有少量AsCl3杂质,二者均为分子晶体,AsCl3的空间结构为___________ ,其沸点高于GeCl4,原因是___________ 。(相对分子质量GeCl4:214.6,AsCl3:181.4)。
(4)碱浸“电解”法可生产出高质量的锌粉:先加入浓NaOH溶液将Zn2+转化为 ,再电解得到锌,
,再电解得到锌, 中与Zn2+配位的原子是
中与Zn2+配位的原子是___________ ,写出电解析出锌的电极反应___________ 。

(1)浸渣的主要成分有S、PbSO4和
(2)单宁酸(H2L)“沉锗”时主要发生反应
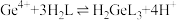 ,最佳pH=2.5,pH过低会导致
,最佳pH=2.5,pH过低会导致(3)“蒸馏”得到的粗GeCl4中混有少量AsCl3杂质,二者均为分子晶体,AsCl3的空间结构为
(4)碱浸“电解”法可生产出高质量的锌粉:先加入浓NaOH溶液将Zn2+转化为
 ,再电解得到锌,
,再电解得到锌, 中与Zn2+配位的原子是
中与Zn2+配位的原子是
您最近一年使用:0次
解题方法
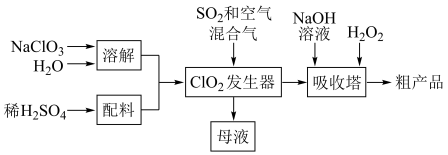
10 . 亚氯酸钠(NaClO2)是高效氧化剂和漂白剂,其制备流程如下:
已知:
① NaClO2在温度高于60 °C时易分解生成NaClO3和NaCl。
②ClO2(沸点11 ℃)浓度高时易发生分解爆炸,可用气体稀释至含量10 %以下。
ClO2极易溶于水。ClO 在酸性溶液中发生歧化反应,离子方程式为:5ClO
在酸性溶液中发生歧化反应,离子方程式为:5ClO +4H+
+4H+ 4ClO2↑+Cl-+2H2O
4ClO2↑+Cl-+2H2O
(1)根据价层电子对互斥理论,预测ClO 离子的空间结构是___________。
离子的空间结构是___________。
(2)推测发生器中鼓入空气的作用可能是___________ 。
(3)①若吸收塔内反应过程中转移2NA个电子,则生成标准状况下氧气的体积为___________ L。
A.11.2 B.22.4 C.33.6 D.44.8
②吸收塔的温度需控制在10℃以下,其原因是___________ 、___________ (列举两点)。
(4)28.25℃时,HClO2、HClO的电离平衡常数分别为:Ka(HClO2)=1.1×10-2、Ka(HClO) =2.98×10-8,常温下,等体积等物质的量浓度的NaClO2 、NaClO两种溶液,下列说法正确的是___________
(5)取0.5 mol·L-1 NaClO2溶液,调节溶液pH=5,再加入适量AgNO3溶液,发现灭菌效果明显增强,请用化学平衡移动原理解释原因。___________
(6)已知NaClO2的溶解度随温度变化曲线如图所示。

①从NaClO2溶液中获得NaClO2无水晶体的过程中对温度的控制要求较高。操作时先减压,再将NaClO2溶液加热浓缩,浓缩时的最佳温度为___________ 。
A.略低于38 ℃ B.略高于38 ℃
C.略低于60 ℃ D.略高于60 ℃
②当加热浓缩至有晶膜出现时,再在常压下___________ (填操作)、过滤、洗涤、干燥。
上述NaClO2产品的纯度测定实验为:称取m g样品溶解后、加入稍过量的KI,再滴加适量的稀硫酸,充分反应后,稀释为500 mL溶液,再移取25.00 mL上述溶液,用c mol·L−1 Na2S2O3标准溶液滴定,终点时消耗V mL,有关实验原理:ClO +4I-+4H+= 2H2O+2I2+Cl-、I2+2S2O
+4I-+4H+= 2H2O+2I2+Cl-、I2+2S2O =2I-+S4O
=2I-+S4O 。
。
(7)计算该NaClO2产品的纯度______ (用含m、c、V的代数式表示,写出计算过程)。

已知:
① NaClO2在温度高于60 °C时易分解生成NaClO3和NaCl。
②ClO2(沸点11 ℃)浓度高时易发生分解爆炸,可用气体稀释至含量10 %以下。
ClO2极易溶于水。ClO
 在酸性溶液中发生歧化反应,离子方程式为:5ClO
在酸性溶液中发生歧化反应,离子方程式为:5ClO +4H+
+4H+ 4ClO2↑+Cl-+2H2O
4ClO2↑+Cl-+2H2O(1)根据价层电子对互斥理论,预测ClO
 离子的空间结构是___________。
离子的空间结构是___________。| A.直线形 | B.V形 | C.平面三角形 | D.正四面体形 |
(2)推测发生器中鼓入空气的作用可能是
(3)①若吸收塔内反应过程中转移2NA个电子,则生成标准状况下氧气的体积为
A.11.2 B.22.4 C.33.6 D.44.8
②吸收塔的温度需控制在10℃以下,其原因是
(4)28.25℃时,HClO2、HClO的电离平衡常数分别为:Ka(HClO2)=1.1×10-2、Ka(HClO) =2.98×10-8,常温下,等体积等物质的量浓度的NaClO2 、NaClO两种溶液,下列说法正确的是___________
| A.碱性:NaClO2 > NaClO | B.离子总数:NaClO2 > NaClO |
C.2 c(Na+)=c(ClO-)+c(ClO ) ) | D. c(ClO )+c(HClO2)=c(ClO-)+c(HClO) )+c(HClO2)=c(ClO-)+c(HClO) |
(5)取0.5 mol·L-1 NaClO2溶液,调节溶液pH=5,再加入适量AgNO3溶液,发现灭菌效果明显增强,请用化学平衡移动原理解释原因。
(6)已知NaClO2的溶解度随温度变化曲线如图所示。

①从NaClO2溶液中获得NaClO2无水晶体的过程中对温度的控制要求较高。操作时先减压,再将NaClO2溶液加热浓缩,浓缩时的最佳温度为
A.略低于38 ℃ B.略高于38 ℃
C.略低于60 ℃ D.略高于60 ℃
②当加热浓缩至有晶膜出现时,再在常压下
上述NaClO2产品的纯度测定实验为:称取m g样品溶解后、加入稍过量的KI,再滴加适量的稀硫酸,充分反应后,稀释为500 mL溶液,再移取25.00 mL上述溶液,用c mol·L−1 Na2S2O3标准溶液滴定,终点时消耗V mL,有关实验原理:ClO
 +4I-+4H+= 2H2O+2I2+Cl-、I2+2S2O
+4I-+4H+= 2H2O+2I2+Cl-、I2+2S2O =2I-+S4O
=2I-+S4O 。
。(7)计算该NaClO2产品的纯度
您最近一年使用:0次



