名校
1 . 短周期元素X、Y、Z、W、Q原子序数依次增大。基态X、Z原子均有两个单电子,W简单离子在同周期离子中半径最小,Q与Y同主族。下列说法错误的是


| A.第一电离能介于W、Q之间的第三周期元素有3种 |
| B.YCl3中心原子的杂化方式为sp3 |
C.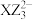 空间结构为平面三角形 空间结构为平面三角形 |
| D.Y、W形成的晶体如上图所示,Y的配位数为2 |
您最近一年使用:0次
名校
2 . 短周期主族元素R、X、Y、Z、W的原子序数依次增大,Y和W位于同族。我国科学家合成一种比硫酸酸性强的超强酸催化剂,广泛应用于有机合成,它的结构式如图所示。下列说法正确的是
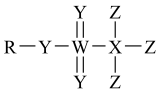
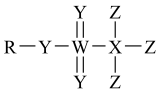
A.简单离子半径: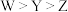 |
B. 元素形成的单质晶体中,原子的杂化类型均相同 元素形成的单质晶体中,原子的杂化类型均相同 |
C.简单氢化物的沸点: |
| D.R、X、Y只能组成一种三元化合物 |
您最近一年使用:0次
名校
解题方法
3 . 下列关于含氧物质的化学用语正确的是
| A.甲醛(HCHO)的空间结构:平面三角形 | B.中子数为10的氧原子: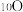 |
C. 分子中O的杂化方式: 分子中O的杂化方式: 杂化 杂化 | D.次氯酸的结构式: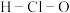 |
您最近一年使用:0次
4 . 有机化合物F是一种镇痛药,它的合成路线如下:
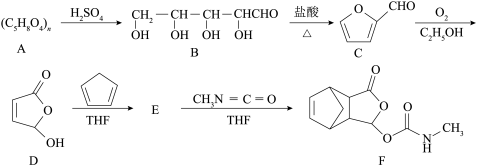
(1)B分子中含氧官能团的名称为_______ 。
(2)D分子中采取sp2杂化的碳原子数目是_______ 。
(3)已知E+CH3N=C=O → F为加成反应,中间体E的结构式为_______ 。
(4)F的同分异构体同时满足下列条件,写出一种该同分异构体的结构简式:_______ 。
I.核磁共振氢谱有3个峰,苯环上的一取代物有2种;
II.能发生水解反应,酸性条件下水解产物之一能与FeCl3溶液发生显色反应。
(5)请以2—戊烯和 CH2=CHCHO为原料制备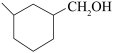 ,写出制备的合成路线流程图
,写出制备的合成路线流程图_______ 。(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)

(1)B分子中含氧官能团的名称为
(2)D分子中采取sp2杂化的碳原子数目是
(3)已知E+CH3N=C=O → F为加成反应,中间体E的结构式为
(4)F的同分异构体同时满足下列条件,写出一种该同分异构体的结构简式:
I.核磁共振氢谱有3个峰,苯环上的一取代物有2种;
II.能发生水解反应,酸性条件下水解产物之一能与FeCl3溶液发生显色反应。
(5)请以2—戊烯和 CH2=CHCHO为原料制备
 ,写出制备的合成路线流程图
,写出制备的合成路线流程图
您最近一年使用:0次
解题方法
5 . 硒( )和碲(
)和碲( )的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景,下列说法正确的是
)的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景,下列说法正确的是
 )和碲(
)和碲( )的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景,下列说法正确的是
)的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景,下列说法正确的是A. 是非极性分子 是非极性分子 |
B. 与 与 微粒中的O-S-O夹角相等 微粒中的O-S-O夹角相等 |
C.硒原子基态核外价电子排布式为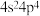 |
| D.ⅥA族元素氢化物的熔沸点从上到下依次增大 |
您最近一年使用:0次
6 . 镓(Ga)位于元素周期表第ⅢA族,镓广泛用于半导体、光电材料领域。
(1)利用炼锌渣(主要含Pb、Zn、Cu、Fe的氧化物和一定量 )为原料制备高纯镓的主要流程为:
)为原料制备高纯镓的主要流程为:
酸浸处理出渣→铜粉处理出渣→……→获取电解液
已知:(ⅰ)电解制取镓时两极均采用惰性电极;
(ⅱ) ,
, 难溶于水和稀酸;
难溶于水和稀酸;
回答下列问题:
① 基态核外电子排布式为
基态核外电子排布式为___________ 。
②“ 粉处理出渣”目的有
粉处理出渣”目的有___________ 。
③络合反应 的化学平衡常数表达式
的化学平衡常数表达式
___________ 。
④电解 溶液时,阴极的电极反应式为
溶液时,阴极的电极反应式为___________ 。
(2)我国“玉兔二号”月球车采用砷化镓(GaAs)太阳能电池。GaAs晶胞结构如图甲所示,将Mn掺杂到GaAs晶体中得到稀磁性半导体材料,结构如图乙所示。 中
中 的化合价为
的化合价为___________ 。
②每个 晶胞平均占有
晶胞平均占有___________ 个 。
。
③已知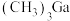 为非极性分子,则其中
为非极性分子,则其中 原子的杂化方式是
原子的杂化方式是___________ 。
④该稀磁性半导体材料的化学式为___________ 。
(1)利用炼锌渣(主要含Pb、Zn、Cu、Fe的氧化物和一定量
 )为原料制备高纯镓的主要流程为:
)为原料制备高纯镓的主要流程为:酸浸处理出渣→铜粉处理出渣→……→获取电解液

已知:(ⅰ)电解制取镓时两极均采用惰性电极;
(ⅱ)
 ,
, 难溶于水和稀酸;
难溶于水和稀酸;回答下列问题:
①
 基态核外电子排布式为
基态核外电子排布式为②“
 粉处理出渣”目的有
粉处理出渣”目的有③络合反应
 的化学平衡常数表达式
的化学平衡常数表达式
④电解
 溶液时,阴极的电极反应式为
溶液时,阴极的电极反应式为(2)我国“玉兔二号”月球车采用砷化镓(GaAs)太阳能电池。GaAs晶胞结构如图甲所示,将Mn掺杂到GaAs晶体中得到稀磁性半导体材料,结构如图乙所示。

 中
中 的化合价为
的化合价为②每个
 晶胞平均占有
晶胞平均占有 。
。③已知
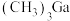 为非极性分子,则其中
为非极性分子,则其中 原子的杂化方式是
原子的杂化方式是④该稀磁性半导体材料的化学式为
您最近一年使用:0次
解题方法
7 . 实验室制备乙炔的反应为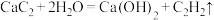 。下列说法
。下列说法不正确 的是
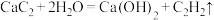 。下列说法
。下列说法A. 的电子式为 的电子式为 |
B. 的中心原子采取 的中心原子采取 杂化 杂化 |
C. 中含有离子键和共价键 中含有离子键和共价键 |
D. 的空间结构为直线形 的空间结构为直线形 |
您最近一年使用:0次
名校
8 . ECH(环氧氯丙烷,结构为 )是生产环氧树脂的中间体,工业上可由如图路线合成。
)是生产环氧树脂的中间体,工业上可由如图路线合成。

已知: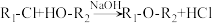
(1)A为丙烯,其分子中含有的官能团是____________ 。
(2)已知B→C为加成反应,A→B的反应类型是_________ 反应。
(3)B→C的反应中,B与次氯酸加成得到的C,有两种结构。
①C结构简式是i:ClCH2-CHCl-CH2OH和ii:_________ 。
②由分子中化学键的极性角度分析,i为B→C的主要产物的原因是_________ 。
(4)原料中的丙烯可由石油裂解得到。在裂解分离得到的含有三个碳原子的馏分中,除丙烯外,杂质气体中含有2种分子式均为C3H4的链烃D和E。
①D分子内含有sp3杂化的碳原子,则D结构简式为_________ 。
②E的核磁共振氢谱只有一组吸收峰,分子内无sp3杂化的碳原子。则
i.E中碳原子的杂化类型是_________ ;
ii.4个氢原子不在同一个平面内,由分子中碳原子的杂化解释其原因_________ 。
 )是生产环氧树脂的中间体,工业上可由如图路线合成。
)是生产环氧树脂的中间体,工业上可由如图路线合成。
已知:
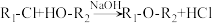
(1)A为丙烯,其分子中含有的官能团是
(2)已知B→C为加成反应,A→B的反应类型是
(3)B→C的反应中,B与次氯酸加成得到的C,有两种结构。
①C结构简式是i:ClCH2-CHCl-CH2OH和ii:
②由分子中化学键的极性角度分析,i为B→C的主要产物的原因是
(4)原料中的丙烯可由石油裂解得到。在裂解分离得到的含有三个碳原子的馏分中,除丙烯外,杂质气体中含有2种分子式均为C3H4的链烃D和E。
①D分子内含有sp3杂化的碳原子,则D结构简式为
②E的核磁共振氢谱只有一组吸收峰,分子内无sp3杂化的碳原子。则
i.E中碳原子的杂化类型是
ii.4个氢原子不在同一个平面内,由分子中碳原子的杂化解释其原因
您最近一年使用:0次
解题方法
9 . 硼的化合物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态硼原子的价电子排布图为:___________ ;B、N、H的电负性由大到小的顺序为___________ 。
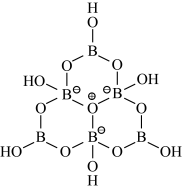
(2)科学家合成了一种含硼阴离子 ,其结构如图所示。其中硼原子的杂化方式为
,其结构如图所示。其中硼原子的杂化方式为___________ ,该结构中共有___________ 种不同化学环境的氧原子。
(3) 与
与 结合形成固态化合物
结合形成固态化合物 ,该物质在
,该物质在 时熔化电离出
时熔化电离出 和一含硼阴离子
和一含硼阴离子___________ (填离子符号); 空间构型为
空间构型为___________ 。
(1)基态硼原子的价电子排布图为:
(2)科学家合成了一种含硼阴离子
 ,其结构如图所示。其中硼原子的杂化方式为
,其结构如图所示。其中硼原子的杂化方式为
(3)
 与
与 结合形成固态化合物
结合形成固态化合物 ,该物质在
,该物质在 时熔化电离出
时熔化电离出 和一含硼阴离子
和一含硼阴离子 空间构型为
空间构型为
您最近一年使用:0次
10 . 已知元素 是组成物质
是组成物质 的其中一种元素。元素
的其中一种元素。元素 的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号
的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号 至
至 表示)如表所示:
表示)如表所示:
(1)元素 是
是___________ (填元素符号)。
(2)基态氮原子核外有___________ 种不同运动状态的电子,有___________ 种能量不同的电子。
(3) 中,电负性最大的元素是
中,电负性最大的元素是___________ (填元素符号), 的
的___________ 杂化轨道与 的
的 轨道形成
轨道形成___________ 键。
 是组成物质
是组成物质 的其中一种元素。元素
的其中一种元素。元素 的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号
的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号 至
至 表示)如表所示:
表示)如表所示: |  |  |  | |
电离能 | 578 | 1817 | 2745 | 11578 |
 是
是(2)基态氮原子核外有
(3)
 中,电负性最大的元素是
中,电负性最大的元素是 的
的 的
的 轨道形成
轨道形成
您最近一年使用:0次



