名校
1 . 下列关于SO2、SO3、NH3、NH 说法中正确的是
说法中正确的是
 说法中正确的是
说法中正确的是| A.SO2水溶液能导电,SO2是电解质 | B.NH 中含有配位键 中含有配位键 |
| C.SO3中硫原子轨道杂化类型为sp3 | D.NH3为非极性分子 |
您最近一年使用:0次
名校
解题方法
2 . 氮族和碳族元素的单质及其化合物在研究和生产中有着广泛的应用。试回答下列问题:
(1) 是一种重要的化工原料,有毒,
是一种重要的化工原料,有毒, 也是一种食品添加剂,使用时须严格控制用量。已知:
也是一种食品添加剂,使用时须严格控制用量。已知: 有强氧化性,酸性
有强氧化性,酸性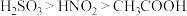 。
。
①亚硝酰氯 是一种红褐色液体,每个原子最外层都达到8电子结构,则其电子式为
是一种红褐色液体,每个原子最外层都达到8电子结构,则其电子式为_____ ,其与水反应会生成两种酸,写出该化学方程式_______ 。
②往冷的 溶液中加入下列某种物质可得
溶液中加入下列某种物质可得 稀溶液,该物质是
稀溶液,该物质是______ (填字母)。
a.稀硫酸 b.二氧化碳 c.二氧化硫 d.醋酸
(2)硅和氯气单质反应可以得到 。
。
①和 互为等电子体的阴离子有
互为等电子体的阴离子有___________ 。(写一种)___________ ,1个 中含有
中含有___________ 个 键。
键。
(3)砷化镓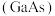 是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。
是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。
①基态 原子外围电子轨道表示式为
原子外围电子轨道表示式为___________ ,N、 、
、 第一电离能由大到小的顺序是
第一电离能由大到小的顺序是___________ 。
②砷化镓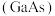 太阳能电池为我国“玉兔二号”月球车提供充足能量。
太阳能电池为我国“玉兔二号”月球车提供充足能量。 的晶胞结构如图甲所示,将
的晶胞结构如图甲所示,将 掺杂到
掺杂到 的晶体中得到稀磁性半导体材料如图乙所示。
的晶体中得到稀磁性半导体材料如图乙所示。 中
中 的化合价为
的化合价为___________ 。在 掺杂到
掺杂到 的晶体中每个
的晶体中每个 最近且等距离的
最近且等距离的 的数目为
的数目为___________ 。
(1)
 是一种重要的化工原料,有毒,
是一种重要的化工原料,有毒, 也是一种食品添加剂,使用时须严格控制用量。已知:
也是一种食品添加剂,使用时须严格控制用量。已知: 有强氧化性,酸性
有强氧化性,酸性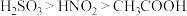 。
。①亚硝酰氯
 是一种红褐色液体,每个原子最外层都达到8电子结构,则其电子式为
是一种红褐色液体,每个原子最外层都达到8电子结构,则其电子式为②往冷的
 溶液中加入下列某种物质可得
溶液中加入下列某种物质可得 稀溶液,该物质是
稀溶液,该物质是a.稀硫酸 b.二氧化碳 c.二氧化硫 d.醋酸
(2)硅和氯气单质反应可以得到
 。
。①和
 互为等电子体的阴离子有
互为等电子体的阴离子有② 与
与 -甲基咪唑(
-甲基咪唑(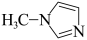 )反应可以得到
)反应可以得到 ,其结构如图所示:
,其结构如图所示:
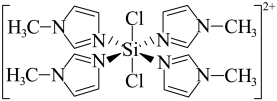
 中含有
中含有 键。
键。(3)砷化镓
 是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。
是当前最重要,技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。①基态
 原子外围电子轨道表示式为
原子外围电子轨道表示式为 、
、 第一电离能由大到小的顺序是
第一电离能由大到小的顺序是②砷化镓
 太阳能电池为我国“玉兔二号”月球车提供充足能量。
太阳能电池为我国“玉兔二号”月球车提供充足能量。 的晶胞结构如图甲所示,将
的晶胞结构如图甲所示,将 掺杂到
掺杂到 的晶体中得到稀磁性半导体材料如图乙所示。
的晶体中得到稀磁性半导体材料如图乙所示。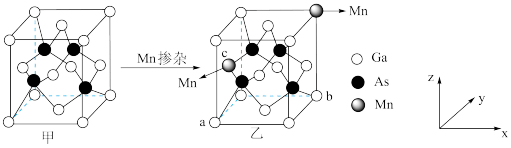
 中
中 的化合价为
的化合价为 掺杂到
掺杂到 的晶体中每个
的晶体中每个 最近且等距离的
最近且等距离的 的数目为
的数目为
您最近一年使用:0次
解题方法
3 . 维生素C,别称L-抗坏血酸,具有抗氧化、抗自由基的作用。其结构如下图所示,下列关于维生素C叙述错误 的是


| A.分子中含有2个手性碳原子 |
| B.分子中碳原子的杂化轨道类型为sp3和sp2 |
| C.维生素C结构中的含氧官能团为酮羰基和羟基 |
| D.该分子易溶于水 |
您最近一年使用:0次
名校
解题方法
4 . 四氟肼可发生反应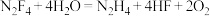 。下列有关叙述中正确的是
。下列有关叙述中正确的是
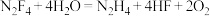 。下列有关叙述中正确的是
。下列有关叙述中正确的是A. 的电子式为 的电子式为 |
B.O的价电子排布式为 |
C. 在水溶液中的电离方程式: 在水溶液中的电离方程式: |
D. 中N的杂化轨道: 中N的杂化轨道: |
您最近一年使用:0次
2023-09-01更新
|
78次组卷
|
2卷引用:黑龙江省哈尔滨市第七十三中学校2022-2023学年高三上学期12月期中考试化学试题
名校
解题方法
5 . 下列对分子性质的解释中,不正确的是


| A.在氨水中,大部分NH3与H2O以氢键(用“⋯”表示)结合形成NH3·H2O分子,则NH3·H2O的结构式如图1 |
B. 和 和 的中心原子杂化方式不同,前者是 的中心原子杂化方式不同,前者是 后者是 后者是 |
C. 、 、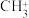 、 、 的空间构型相同 的空间构型相同 |
D.由如图2可知酸性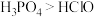 ,因为 ,因为 分子中有1个非羟基氧原子 分子中有1个非羟基氧原子 |
您最近一年使用:0次
名校
解题方法
6 . NA为阿伏加德罗常数的值。下列叙述错误的是
| A.1mol[Cu(NH3)4]2+中配位键的个数为4NA |
| B.46gCH3CH2OH中sp3杂化的原子数为2NA |
| C.0.5molSF6中S的价层电子对数为3NA |
| D.1molNaHSO4固体中离子数目为2NA |
您最近一年使用:0次
名校
解题方法
7 . 推广磷酸亚铁锂(LiFePO4)电池的新能源汽车对减少二氧化碳排放和大气污染具有重要意义。工业上用FeCl3、NH4H2PO4、LiCl及苯胺(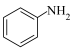 )为原料制磷酸亚铁锂材料。回答下列问题:
)为原料制磷酸亚铁锂材料。回答下列问题:
(1)基态铁原子核外电子运动状态有_______ 种,基态Fe3+较基态Fe2+稳定的原因是_______ (从价层电子排布角度分析)。
(2)在NH4H2PO4中,N、P、O三种元素的第一电离能由大到小的顺序是_______ ;LiFePO4中, 的空间结构为
的空间结构为_______ 。
(3)1 mol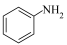 中含有
中含有_______ mol σ键。苯胺水溶性大于苯的主要原因是_______ 。
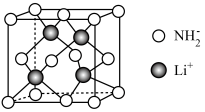
(4)LiNH2常用作电池电极,LiNH2晶体中, 为面心立方堆积,Li+填充了其中一半的四面体空隙,晶胞如图1所示,则一个LiNH2晶胞中共含有
为面心立方堆积,Li+填充了其中一半的四面体空隙,晶胞如图1所示,则一个LiNH2晶胞中共含有_______ 个共价键;设该晶胞的边长为acm,用NA表示阿伏加德罗常数的值,则该晶体的密度为_______ (用含a和NA的代数式表示) 。
。
 )为原料制磷酸亚铁锂材料。回答下列问题:
)为原料制磷酸亚铁锂材料。回答下列问题:(1)基态铁原子核外电子运动状态有
(2)在NH4H2PO4中,N、P、O三种元素的第一电离能由大到小的顺序是
 的空间结构为
的空间结构为(3)1 mol
 中含有
中含有(4)LiNH2常用作电池电极,LiNH2晶体中,
 为面心立方堆积,Li+填充了其中一半的四面体空隙,晶胞如图1所示,则一个LiNH2晶胞中共含有
为面心立方堆积,Li+填充了其中一半的四面体空隙,晶胞如图1所示,则一个LiNH2晶胞中共含有 。
。
您最近一年使用:0次
名校
解题方法
8 . 前四周期元素A、B、C、D、E的原子序数依次增大,A元素原子的核外电子只有一种运动状态;基态B原子s能级的电子总数比p能级的多1;基态C原子中成对电子数均是未成对电子数的3倍;D形成简单离子的半径在同周期元素形成的简单离子中最小;元素E是第四周期中未成对电子数最多的元素,回答下列问题:
(1)基态E原子的价层电子轨道表示式为_______ 。
(2)写出A与C原子个数比为1:1的化合物的电子式:_______ ,该化合物为_______ 分子(填“极性”或“非极性”)。
(3)元素A、B、C中,电负性最大的是_______ (填元素符号),写出D的氢氧化物与氢氧化钠反应的离子方程式:_______ 。
(4)与同族其他元素X形成的XA3相比,BA3易液化的原因是_______ ;BA3分子中键角_______ (填“>”“<”或“=”)109°28′。
(5) 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为_______ ,A3C+的空间结构为_______ 。
(1)基态E原子的价层电子轨道表示式为
(2)写出A与C原子个数比为1:1的化合物的电子式:
(3)元素A、B、C中,电负性最大的是
(4)与同族其他元素X形成的XA3相比,BA3易液化的原因是
(5)
 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为
您最近一年使用:0次
名校
解题方法
9 . 下列关于苯乙炔的说法不正确的是


| A.该分子有八个σ键 | B.该分子中碳原子有sp和sp2杂化 |
| C.该分子存在非极性键 | D.该分子中8个碳原子在同一平面上 |
您最近一年使用:0次
名校
解题方法
10 . 徐光宪在《分子共和国》一书中介绍了许多明星分子,如H2O2、CO2、BF3、CH3COOH等。下列说法正确的是
| A.H2O2分子为非极性分子 | B.CO2 分子中C原子为sp2杂化 |
| C.BF3分子为平面三角形 | D.CH3COOH分子间只存在范德华力 |
您最近一年使用:0次



