名校
解题方法
1 . 氯化铜是共价化合物,通常用作有机和无机反应催化剂、媒染剂等。 溶液与乙二胺(
溶液与乙二胺( )可形成配离子
)可形成配离子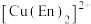 (En是乙二胺的简写),如图所示,下列说法中错误的是
(En是乙二胺的简写),如图所示,下列说法中错误的是
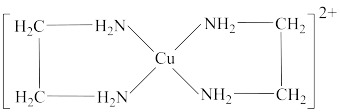
 溶液与乙二胺(
溶液与乙二胺( )可形成配离子
)可形成配离子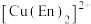 (En是乙二胺的简写),如图所示,下列说法中错误的是
(En是乙二胺的简写),如图所示,下列说法中错误的是
A.基态 的未成对电子数为1 的未成对电子数为1 |
B.配离子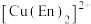 中N原子提供孤对电子 中N原子提供孤对电子 |
C.乙二胺和三甲胺 均属于胺,沸点更高的是三甲胺 均属于胺,沸点更高的是三甲胺 |
D.配离子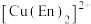 中涉及的元素的电负性由大到小的顺序为N>C>H>Cu 中涉及的元素的电负性由大到小的顺序为N>C>H>Cu |
您最近一年使用:0次
2023-05-21更新
|
455次组卷
|
3卷引用:江西省龙南中学2022-2023学年高二下学期6月期末考试化学试题
22-23高二下·江西·阶段练习
名校
2 . 已知 为阿伏伽德罗常数的值,下列有关说法正确的是
为阿伏伽德罗常数的值,下列有关说法正确的是
 为阿伏伽德罗常数的值,下列有关说法正确的是
为阿伏伽德罗常数的值,下列有关说法正确的是A.常温下, 的盐酸溶液中氢离子数目为 的盐酸溶液中氢离子数目为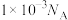 |
B. 冰醋酸分子中含有 冰醋酸分子中含有 杂化的原子数目为 杂化的原子数目为 |
C.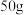 质量分数为46%的乙醇水溶液中含有 质量分数为46%的乙醇水溶液中含有 键数目为 键数目为 |
D.  中共价键的个数为 中共价键的个数为 |
您最近一年使用:0次
3 . 某配合物W的化学式为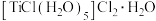 ,下列说法正确的是
,下列说法正确的是
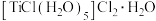 ,下列说法正确的是
,下列说法正确的是A.中心离子 提供空轨道 提供空轨道 |
B. 的W溶液中 的W溶液中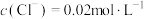 |
| C.基态钛原子的价层电子数为2 |
D.配体 中氢原子提供孤电子对 中氢原子提供孤电子对 |
您最近一年使用:0次
2023-05-21更新
|
154次组卷
|
3卷引用:江西省九江市彭泽县第二高级中学2022-2023学年高二下学期7月期末化学试题
名校
4 . 冰晶石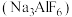 是冶炼铝时使用的助熔剂,该物质中不可能存在的化学键是
是冶炼铝时使用的助熔剂,该物质中不可能存在的化学键是
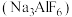 是冶炼铝时使用的助熔剂,该物质中不可能存在的化学键是
是冶炼铝时使用的助熔剂,该物质中不可能存在的化学键是| A.离子键 | B.配位键 | C. 键 键 | D. 键 键 |
您最近一年使用:0次
2023-05-21更新
|
119次组卷
|
2卷引用:江西省九江市湖口中学2022-2023学年高二下学期7月期末考试化学试题
名校
5 . 设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,11.2LCHCl3的原子总数为2.5NA |
| B.1mol[Cu(H2O)4]2+中含有的σ键数目为12NA |
| C.1mol冰中含有的氢键数目为2NA |
| D.6gSiO2中所含Si-O键的数目为0.2NA |
您最近一年使用:0次
2023-05-20更新
|
57次组卷
|
2卷引用:江西省吉安市第三中学2022-2023学年高二下学期6月期末考试化学试题
名校
解题方法
6 . 近日,科学家开发用于人工固氮的 型碳材料高效利用
型碳材料高效利用 和
和 固氮合成
固氮合成 。反应原理如图所示。
。反应原理如图所示。

回答下列问题:
(1)基态C原子核外有___________ 种不同空间运动状态的电子;基态N原子有___________ 个不同运动状态的电子。
(2)基态H原子电子云轮廓图为___________ (填名称)。
(3) 的空间构型为
的空间构型为___________ , 的VSEPR模型为
的VSEPR模型为___________ 。
(4)从上述反应机理看出,第一步,1个 分子断键与
分子断键与 形成
形成___________ (填“共价键”“配位键”或“离子键”)。
(5) 催化剂中,C原子杂化类型是
催化剂中,C原子杂化类型是___________ ,N原子杂化类型是___________ 。
(6)C和N形成一种超硬度新材料,其熔点高于金刚石,其晶体部分结构如图所示。

①该晶体类型是___________ ,加热该材料时破坏的作用力类型是___________ 。
②该超硬度新材料的化学式为___________ 。
 型碳材料高效利用
型碳材料高效利用 和
和 固氮合成
固氮合成 。反应原理如图所示。
。反应原理如图所示。
回答下列问题:
(1)基态C原子核外有
(2)基态H原子电子云轮廓图为
(3)
 的空间构型为
的空间构型为 的VSEPR模型为
的VSEPR模型为(4)从上述反应机理看出,第一步,1个
 分子断键与
分子断键与 形成
形成(5)
 催化剂中,C原子杂化类型是
催化剂中,C原子杂化类型是(6)C和N形成一种超硬度新材料,其熔点高于金刚石,其晶体部分结构如图所示。

①该晶体类型是
②该超硬度新材料的化学式为
您最近一年使用:0次
2023-05-18更新
|
110次组卷
|
2卷引用:江西省南昌市等5地2022-2023学年高二下学期4月期中考试化学试题
名校
7 . 某化合物的结构示意图如图,下列关于该化合物的叙述中正确的是


| A.该化合物含有 H、O、N、Ni 四种元素 |
| B.该化合物属于配合物,中心离子是 N |
| C.该化合物中含有σ键、π键、极性键、非极性键、配位键和氢键 |
| D.该化合物是配合物,中心离子的配位数是2,配体是氮元素 |
您最近一年使用:0次
2023-05-17更新
|
164次组卷
|
3卷引用:江西省九江市湖口中学2022-2023学年高二下学期7月期末考试化学试题
名校
解题方法
8 . Ⅰ.配位化合物在生产生活中有重要应用,请根据要求回答下列问题:
(1) 可以形成多种配离子,如
可以形成多种配离子,如 、
、 、丁二酮肟镍分子(见图)等。
、丁二酮肟镍分子(见图)等。

① 中
中 键角比
键角比 分子中
分子中 键角
键角___________ (填“大”或“小”)。
②丁二酮肟镍分子内含有的作用力有___________ (填字母)。
a.配位键 b.离子键 c.氢键 d.金属键
(2)关于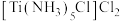 的说法中错误的是
的说法中错误的是___________ 。
A.中心原子的化合价为+3价
B.中心原子的配位数是6
C.含1mol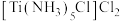 的水溶液中加入足量
的水溶液中加入足量 溶液,产生3mol白色沉淀
溶液,产生3mol白色沉淀
(3)已知 立体结构如图,其中1~6处的小圆圈表示
立体结构如图,其中1~6处的小圆圈表示 分子,且各相邻的
分子,且各相邻的 分子间的距离相等(图中虚线长度相等)。
分子间的距离相等(图中虚线长度相等)。 位于正八面体的中心,若其中两个
位于正八面体的中心,若其中两个 被
被 取代,所形成的
取代,所形成的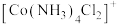 的结构的数目为
的结构的数目为___________ 。

Ⅱ.碳元素能形成多种单质,其中石墨和富勒烯( )是两类常见的物质。
)是两类常见的物质。 以其完美的球烯受到科学家重视。
以其完美的球烯受到科学家重视。

(4)石墨晶体中存在的作用力类型有___________ 。
a.σ键 b.极性键 c.非极性键 d.离子键 e.范德华力
(5)石墨、 互为同素异形体,但相同条件下,石墨的熔点比
互为同素异形体,但相同条件下,石墨的熔点比 高得多,原因是
高得多,原因是___________ 。
(6) 的晶胞结构如图所示,每个白球代表1个
的晶胞结构如图所示,每个白球代表1个 分子。已知一定条件下晶胞的棱长为acm,阿伏伽德罗常数为
分子。已知一定条件下晶胞的棱长为acm,阿伏伽德罗常数为 ,则该条件下
,则该条件下 的摩尔体积为
的摩尔体积为___________ cm ⋅mol
⋅mol (用含a、
(用含a、 的代数式表示)
的代数式表示)

(7) 常态下是为紫色固体,不导电,但给富勒烯掺杂金属后(用金属原子把富勒烯分子连起来或者把金属原子放进富勒烯笼子里),其在一定条件下甚至可以成为超导体。
常态下是为紫色固体,不导电,但给富勒烯掺杂金属后(用金属原子把富勒烯分子连起来或者把金属原子放进富勒烯笼子里),其在一定条件下甚至可以成为超导体。 晶体结构中存在四面体空隙(如图中1、3、6、7围成的空隙)和八面体空隙(如图中3、6、7、8、9、12围成的空隙)。所有空隙中均填充一个金属M原子,可获得某条件下的超导材料。则该超导材料中,平均一个
晶体结构中存在四面体空隙(如图中1、3、6、7围成的空隙)和八面体空隙(如图中3、6、7、8、9、12围成的空隙)。所有空隙中均填充一个金属M原子,可获得某条件下的超导材料。则该超导材料中,平均一个 晶胞需掺杂
晶胞需掺杂___________ 个M原子。
(1)
 可以形成多种配离子,如
可以形成多种配离子,如 、
、 、丁二酮肟镍分子(见图)等。
、丁二酮肟镍分子(见图)等。
①
 中
中 键角比
键角比 分子中
分子中 键角
键角②丁二酮肟镍分子内含有的作用力有
a.配位键 b.离子键 c.氢键 d.金属键
(2)关于
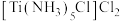 的说法中错误的是
的说法中错误的是A.中心原子的化合价为+3价
B.中心原子的配位数是6
C.含1mol
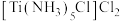 的水溶液中加入足量
的水溶液中加入足量 溶液,产生3mol白色沉淀
溶液,产生3mol白色沉淀(3)已知
 立体结构如图,其中1~6处的小圆圈表示
立体结构如图,其中1~6处的小圆圈表示 分子,且各相邻的
分子,且各相邻的 分子间的距离相等(图中虚线长度相等)。
分子间的距离相等(图中虚线长度相等)。 位于正八面体的中心,若其中两个
位于正八面体的中心,若其中两个 被
被 取代,所形成的
取代,所形成的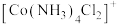 的结构的数目为
的结构的数目为
Ⅱ.碳元素能形成多种单质,其中石墨和富勒烯(
 )是两类常见的物质。
)是两类常见的物质。 以其完美的球烯受到科学家重视。
以其完美的球烯受到科学家重视。
(4)石墨晶体中存在的作用力类型有
a.σ键 b.极性键 c.非极性键 d.离子键 e.范德华力
(5)石墨、
 互为同素异形体,但相同条件下,石墨的熔点比
互为同素异形体,但相同条件下,石墨的熔点比 高得多,原因是
高得多,原因是(6)
 的晶胞结构如图所示,每个白球代表1个
的晶胞结构如图所示,每个白球代表1个 分子。已知一定条件下晶胞的棱长为acm,阿伏伽德罗常数为
分子。已知一定条件下晶胞的棱长为acm,阿伏伽德罗常数为 ,则该条件下
,则该条件下 的摩尔体积为
的摩尔体积为 ⋅mol
⋅mol (用含a、
(用含a、 的代数式表示)
的代数式表示)
(7)
 常态下是为紫色固体,不导电,但给富勒烯掺杂金属后(用金属原子把富勒烯分子连起来或者把金属原子放进富勒烯笼子里),其在一定条件下甚至可以成为超导体。
常态下是为紫色固体,不导电,但给富勒烯掺杂金属后(用金属原子把富勒烯分子连起来或者把金属原子放进富勒烯笼子里),其在一定条件下甚至可以成为超导体。 晶体结构中存在四面体空隙(如图中1、3、6、7围成的空隙)和八面体空隙(如图中3、6、7、8、9、12围成的空隙)。所有空隙中均填充一个金属M原子,可获得某条件下的超导材料。则该超导材料中,平均一个
晶体结构中存在四面体空隙(如图中1、3、6、7围成的空隙)和八面体空隙(如图中3、6、7、8、9、12围成的空隙)。所有空隙中均填充一个金属M原子,可获得某条件下的超导材料。则该超导材料中,平均一个 晶胞需掺杂
晶胞需掺杂
您最近一年使用:0次
2023-05-15更新
|
393次组卷
|
2卷引用:江西省南昌市第十九中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
9 . 氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应得到BF3和BN,如图所示。下列叙述正确的是
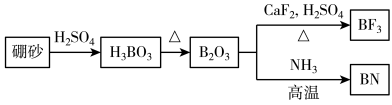
| A.硼酸具有片层状结构,层与层之间、H3BO3单元间都仅以范德华力连接 |
| B. NH3与BF3都是由极性键构成的极性分子 |
C. 与HF反应后再用氨气中和得到 与HF反应后再用氨气中和得到 ,1 mol ,1 mol 含有配位键的数目为 含有配位键的数目为 |
| D.立方氮化硼结构与金刚石相似,立方氮化硼晶胞中每个氮原子周围有4个硼原子 |
您最近一年使用:0次
2023-05-13更新
|
216次组卷
|
3卷引用:江西省南昌市第一中学2023-2024学年高二下学期4月期中考试化学试题
名校
解题方法
10 . 离子液体是在室温或接近室温时呈液态的盐类物质,应用广泛。1-乙基-3-甲基咪唑四氟硼酸盐离子液体结构如图所示,其环状结构中存在大π键。下列相关叙述错误的是


| A.阳离子中至少10原子共平面 | B.阴离子呈正四面体形 |
| C.该离子液体存在共价键、配位键、离子键 | D.阳离子中 键数目是π键数目的10倍 键数目是π键数目的10倍 |
您最近一年使用:0次
2023-05-10更新
|
206次组卷
|
2卷引用:江西省九江市湖口中学2022-2023学年高二下学期7月期末考试化学试题



