名校
解题方法
1 . 某物质的结构如图所示,W、X、Y、Z、M为原子序数依次增大的短周期元素,元素Z的原子序数是X原子最外层电子数的2倍。如果不慎将碱沾到皮肤上,应立即用大量的水冲洗,然后涂上W的最高价含氧酸的稀溶液。下列说法正确的是
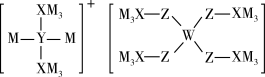
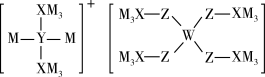
| A.阴离子中所有原子均满足8电子结构 |
| B.上述元素中M元素最高价氧化物水化物的酸性最强 |
| C.阴阳离子中均存在极性键、非极性键、配位键 |
D.微粒半径 |
您最近一年使用:0次
2023-07-15更新
|
113次组卷
|
2卷引用:江西省萍乡市安源中学2022-2023学年高二下学期期中考试化学试题
名校
解题方法
2 . 铁的化合物在日常生产、生活中应用非常广泛。某含 化合物的制备需氮气、丙酮和乙醇参与。
化合物的制备需氮气、丙酮和乙醇参与。
(1)CO、NO均能够与血红蛋白(Hb)中 形成稳定的配合物使血红蛋白失去携氧能力,因而其有毒性。
形成稳定的配合物使血红蛋白失去携氧能力,因而其有毒性。
已知: 进入血液后有如下平衡:
进入血液后有如下平衡:
①基态 中未成对电子数为
中未成对电子数为_______ 。
②C、N、O三种元素,第一电离能由大到小的顺序为_______ 。
③在 、
、 结构中,C、N、O原子均含有孤电子对,与
结构中,C、N、O原子均含有孤电子对,与 配位时,配位原子均不是
配位时,配位原子均不是 原子,理由是
原子,理由是_______ 。
(2)乙醇的沸点(78.3℃)高于丙酮的沸点(56.5℃),原因是_______ 。
(3)合成氨催化剂前驱体(主要成分为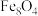 )使用前
)使用前 还原,生成
还原,生成 包裹的
包裹的 。已知
。已知 属于立方晶系,晶胞参数
属于立方晶系,晶胞参数 ,密度为
,密度为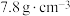 ,则
,则 晶胞中含有
晶胞中含有 的原子数为
的原子数为_______ (列出计算式,阿伏加德罗常数的值为 )。
)。
 化合物的制备需氮气、丙酮和乙醇参与。
化合物的制备需氮气、丙酮和乙醇参与。(1)CO、NO均能够与血红蛋白(Hb)中
 形成稳定的配合物使血红蛋白失去携氧能力,因而其有毒性。
形成稳定的配合物使血红蛋白失去携氧能力,因而其有毒性。已知:
 进入血液后有如下平衡:
进入血液后有如下平衡:
①基态
 中未成对电子数为
中未成对电子数为②C、N、O三种元素,第一电离能由大到小的顺序为
③在
 、
、 结构中,C、N、O原子均含有孤电子对,与
结构中,C、N、O原子均含有孤电子对,与 配位时,配位原子均不是
配位时,配位原子均不是 原子,理由是
原子,理由是(2)乙醇的沸点(78.3℃)高于丙酮的沸点(56.5℃),原因是
(3)合成氨催化剂前驱体(主要成分为
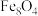 )使用前
)使用前 还原,生成
还原,生成 包裹的
包裹的 。已知
。已知 属于立方晶系,晶胞参数
属于立方晶系,晶胞参数 ,密度为
,密度为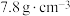 ,则
,则 晶胞中含有
晶胞中含有 的原子数为
的原子数为 )。
)。
您最近一年使用:0次
2023-07-12更新
|
79次组卷
|
2卷引用:江西省乐安县第二中学2023-2024学年高三上学期开学考试化学试题
名校
3 .  的配位化合物较稳定且应用广泛。
的配位化合物较稳定且应用广泛。 可与
可与 、
、 、
、 等配体形成使溶液呈浅紫色的
等配体形成使溶液呈浅紫色的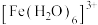 、红色的
、红色的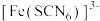 、无色的
、无色的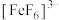 等配离子。某同学按如下步骤进行实验:
等配离子。某同学按如下步骤进行实验:

已知:大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为 。下列说法正确的是
。下列说法正确的是
 的配位化合物较稳定且应用广泛。
的配位化合物较稳定且应用广泛。 可与
可与 、
、 、
、 等配体形成使溶液呈浅紫色的
等配体形成使溶液呈浅紫色的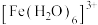 、红色的
、红色的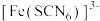 、无色的
、无色的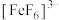 等配离子。某同学按如下步骤进行实验:
等配离子。某同学按如下步骤进行实验:
已知:大π键可用符号
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为 。下列说法正确的是
。下列说法正确的是A. 的第一电离能 的第一电离能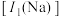 大于 大于 的第一电离能 的第一电离能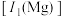 |
B. 与 与 均为直线形结构, 均为直线形结构, 中存在大π键,可表示为 中存在大π键,可表示为 |
C.基态 和基态 和基态 的核外电子排布中,未成对电子数之比 的核外电子排布中,未成对电子数之比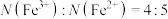 |
D. 中 中 的键角小于 的键角小于 分子中 分子中 的键角 的键角 |
您最近一年使用:0次
2023-07-10更新
|
378次组卷
|
6卷引用:江西省吉安市双校联盟2022-2023学年高二下学期期中考试化学试题
名校
解题方法
4 . 哈尔滨工业大学的李惠等人和加州大学洛杉矶分校的黄昱、段镶锋合作合成了具备超轻、高力学强度和超级隔热三大特点的氮化硼(hBNAGs)以及碳化硅( -SiCAGs)陶瓷气凝胶材料,这种坚固的材料系统非常适用于当作极端条件下的超热绝缘体使用,主要用于航天器领域。回答下列问题:
-SiCAGs)陶瓷气凝胶材料,这种坚固的材料系统非常适用于当作极端条件下的超热绝缘体使用,主要用于航天器领域。回答下列问题:
(1)硅原子的价电子排布图为___________ 。B、N、O、Al的第一电离能由大到小的顺序为___________ (用元素符号表示)。
(2)硼元素深受配位化学家的喜爱,其原因在于B容易与配体形成配位键,如BF 。硼酸[B(OH)3]在水中电离产生H+过程为:B(OH)3 + H2O
。硼酸[B(OH)3]在水中电离产生H+过程为:B(OH)3 + H2O H+ + [B(OH)4]−。
H+ + [B(OH)4]−。
① 从原子结构分析B容易与配体形成配位键的原因___________ 。
② 下列有关硼酸及其相关化合物的说法正确的是___________ (填标号)。
A.硼酸的电离过程中有配位键形成
B.硼酸为三元酸
C.Na[B(OH)4]的水溶液呈碱性
D.硼酸和[B(OH)4]−中的键角相同
(3)氨硼烷(NH3BH3)具有良好的储氢能力。已知B、N、H三种元素的电负性如下:
① 下列有关氨硼烷(NH3BH3)的说法中错误的是___________ (填标号)。
A.H元素为+1价
B.氨硼烷中有配位键
C.N和B原子均为sp3杂化
D.氨硼烷在一定条件下能与水反应产生氢气
② 氨硼烷中H−N−H的键角___________ (填“>”“<”或“=”)H−B−H的键角。
 -SiCAGs)陶瓷气凝胶材料,这种坚固的材料系统非常适用于当作极端条件下的超热绝缘体使用,主要用于航天器领域。回答下列问题:
-SiCAGs)陶瓷气凝胶材料,这种坚固的材料系统非常适用于当作极端条件下的超热绝缘体使用,主要用于航天器领域。回答下列问题:(1)硅原子的价电子排布图为
(2)硼元素深受配位化学家的喜爱,其原因在于B容易与配体形成配位键,如BF
 。硼酸[B(OH)3]在水中电离产生H+过程为:B(OH)3 + H2O
。硼酸[B(OH)3]在水中电离产生H+过程为:B(OH)3 + H2O H+ + [B(OH)4]−。
H+ + [B(OH)4]−。① 从原子结构分析B容易与配体形成配位键的原因
② 下列有关硼酸及其相关化合物的说法正确的是
A.硼酸的电离过程中有配位键形成
B.硼酸为三元酸
C.Na[B(OH)4]的水溶液呈碱性
D.硼酸和[B(OH)4]−中的键角相同
(3)氨硼烷(NH3BH3)具有良好的储氢能力。已知B、N、H三种元素的电负性如下:
| 元素符号 | H | B | N |
| 电负性 | 2.1 | 2.0 | 3.0 |
A.H元素为+1价
B.氨硼烷中有配位键
C.N和B原子均为sp3杂化
D.氨硼烷在一定条件下能与水反应产生氢气
② 氨硼烷中H−N−H的键角
您最近一年使用:0次
2023-07-06更新
|
106次组卷
|
2卷引用:江西省吉安市万安中学2023-2024学年高三上学期开学考试化学试题
解题方法
5 . 我国科学家制备的 催化剂能实现氨硼烷
催化剂能实现氨硼烷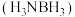 高效制氢,发生反应的化学方程式为
高效制氢,发生反应的化学方程式为 。下列有关说法错误的是
。下列有关说法错误的是
 催化剂能实现氨硼烷
催化剂能实现氨硼烷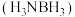 高效制氢,发生反应的化学方程式为
高效制氢,发生反应的化学方程式为 。下列有关说法错误的是
。下列有关说法错误的是| A.基态Ni的价电子有6种空间运动状态 |
B.第一电离能: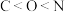 |
C.氨气中键角 大于氨硼烷中键角 大于氨硼烷中键角 |
| D.氨硼烷中N提供孤电子对和B提供的空轨道形成配位键 |
您最近一年使用:0次
解题方法
6 . 按要求回答下列问题:
(1)9.0g某有机化合物完全燃烧可产生0.3molCO2和0.3molH2O。该物质的蒸气对氢气的相对密度是45,则该有机化合物的分子式为_________ 。若该物质为链状结构,其核磁共振氢谱有4组峰,峰面积之比为1∶2∶2∶1,且自身能够发生缩聚反应生成聚酯,其结构简式为_________ 。
(2)氨气极易溶于水的原因是_________ 。
(3)CH3COOH的酸性小于CCl3COOH的原因是_________ 。
(4)三价铬离子能形成多种配位化合物。在 中,提供电子对形成配位键的原子除了N、Cl外,还有
中,提供电子对形成配位键的原子除了N、Cl外,还有_________ (填元素符号), 中含有
中含有_________ molσ键。
(1)9.0g某有机化合物完全燃烧可产生0.3molCO2和0.3molH2O。该物质的蒸气对氢气的相对密度是45,则该有机化合物的分子式为
(2)氨气极易溶于水的原因是
(3)CH3COOH的酸性小于CCl3COOH的原因是
(4)三价铬离子能形成多种配位化合物。在
 中,提供电子对形成配位键的原子除了N、Cl外,还有
中,提供电子对形成配位键的原子除了N、Cl外,还有 中含有
中含有
您最近一年使用:0次
2023-07-02更新
|
84次组卷
|
2卷引用:江西省吉安市吉州区部分学校联考2022-2023学年高二下学期期末考试化学试题
名校
解题方法
7 . 硫酸镍溶于氨水形成 蓝色溶液,下列说法正确的是
蓝色溶液,下列说法正确的是
 蓝色溶液,下列说法正确的是
蓝色溶液,下列说法正确的是A.第一电离能: |
B. 分子的空间结构:平面三角形 分子的空间结构:平面三角形 |
| C.S元素位于元素周期表的第三周期第IVA族 |
| D.基态Ni原子的价层电子排布式:3d84s2 |
您最近一年使用:0次
2023-06-30更新
|
183次组卷
|
4卷引用:江西省吉安市第三中学2023-2024学年高三上学期开学考试化学试题
解题方法
8 . X、Y、Z是常见的三种冠醚,其结构如图所示。它们能与碱金属离子作用,并随着环的大小不同而与不同金属离子作用。Li+的体积与x的空腔大小相近,恰好能进入X的环内,且Li+与氧原子的一对孤电子对作用形成稳定结构W(如图所示)。
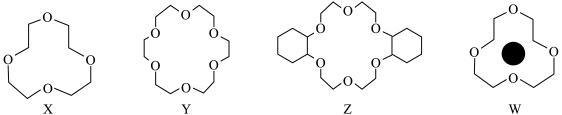
例如:冠醚Z可与KMnO4发生如图所示的变化:
KMnO4+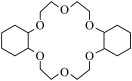

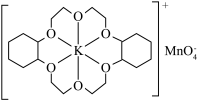
下列说法正确的是

例如:冠醚Z可与KMnO4发生如图所示的变化:
KMnO4+



下列说法正确的是
| A.W中Li+与冠醚x之间的作用属于离子键 |
| B.冠醚Y既能与K+形成稳定结构,也能与Li+形成稳定结构 |
| C.烯烃难溶于水,被KMnO4水溶液氧化的效果较差,若烯烃中溶入冠醚Z,氧化效果明显提升 |
| D.与W相比,X中的C-O-C键角更大 |
您最近一年使用:0次
名校
解题方法
9 . 工业上可由菱锌矿(主要成分为ZnCO3,还含有Ni、Cd、Fe、Mn等元素)制备ZnO,工艺流程如图所示:
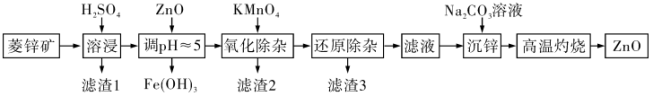
相关金属离子[ ]形成氢氧化物沉淀的pH如下:
]形成氢氧化物沉淀的pH如下:
已知:①“溶浸”后的溶液pH=1,所含金属离子主要有: 、
、 、
、 、
、 、
、 。
。
②弱酸性溶液中KMnO4氧化 时,产物中含Mn元素物质只有MnO2。
时,产物中含Mn元素物质只有MnO2。
③氧化性强弱顺序: 。
。
(1)ZnO溶于氨水生成 ,1 mol
,1 mol  共有
共有________ mol的 键。
键。
(2)①“溶浸”过程中,为了提高浸出率,可采取的措施是___________ (写一条即可)。
②“调pH”时,可替代ZnO的一种含锌化合物是___________ (用化学式表示)。
③“调pH”时,若pH=5.5,此时溶液中 的最大浓度c=
的最大浓度c=___________ mol/L。
(3)写出“氧化除杂”时KMnO4溶液与 反应的离子方程式
反应的离子方程式___________ 。
(4)“还原除杂”除去的离子是___________ ,加入的还原剂是___________ 。

相关金属离子[
 ]形成氢氧化物沉淀的pH如下:
]形成氢氧化物沉淀的pH如下:| 金属离子 |  |  |  |  |  |  |
| 开始沉淀的pH | 1.5 | 6.3 | 6.0 | 7.4 | 8.1 | 6.9 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.0 | 9.4 | 10.1 | 8.9 |
 、
、 、
、 、
、 、
、 。
。②弱酸性溶液中KMnO4氧化
 时,产物中含Mn元素物质只有MnO2。
时,产物中含Mn元素物质只有MnO2。③氧化性强弱顺序:
 。
。(1)ZnO溶于氨水生成
 ,1 mol
,1 mol  共有
共有 键。
键。(2)①“溶浸”过程中,为了提高浸出率,可采取的措施是
②“调pH”时,可替代ZnO的一种含锌化合物是
③“调pH”时,若pH=5.5,此时溶液中
 的最大浓度c=
的最大浓度c=(3)写出“氧化除杂”时KMnO4溶液与
 反应的离子方程式
反应的离子方程式(4)“还原除杂”除去的离子是
您最近一年使用:0次
2023-06-29更新
|
126次组卷
|
2卷引用:江西省南昌十九中2023-2024学年高三上学期第一次月考化学试卷

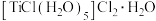 的说法不正确的是
的说法不正确的是 和
和 ,配离子是
,配离子是

 该配合物中加入足量
该配合物中加入足量 溶液,可以得到
溶液,可以得到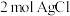 沉淀
沉淀

