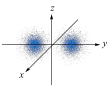
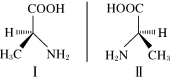1 . 下列示意图或图示正确的是
|
|
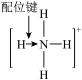
| A.基态铍原子价电子云图 | B. 的结构式 的结构式 |
|
|
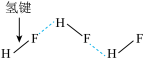
| C.丙氨酸的手性异构体 | D.HF分子间的氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 钙钛矿具有独特的晶体结构,广泛应用于太阳能电池材料、传感器等诸多领域。图1、2均为钙钛矿型化合物,图1中另两种离子为 、
、 ,图2中另两种离子为
,图2中另两种离子为 和
和 ,晶胞参数
,晶胞参数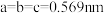 ,
, a=B=y=90°。图2钙钛矿型化合物制成的太阳能电池与锂硫电池集成,可实现太阳能直接对锂硫电池充电,其原理如图3所示:
a=B=y=90°。图2钙钛矿型化合物制成的太阳能电池与锂硫电池集成,可实现太阳能直接对锂硫电池充电,其原理如图3所示:
 、
、 ,图2中另两种离子为
,图2中另两种离子为 和
和 ,晶胞参数
,晶胞参数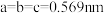 ,
, a=B=y=90°。图2钙钛矿型化合物制成的太阳能电池与锂硫电池集成,可实现太阳能直接对锂硫电池充电,其原理如图3所示:
a=B=y=90°。图2钙钛矿型化合物制成的太阳能电池与锂硫电池集成,可实现太阳能直接对锂硫电池充电,其原理如图3所示: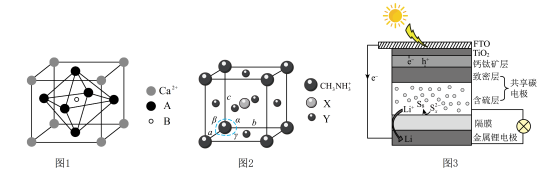
A.钛酸钙的化学式为 | B.图2中Y为 |
C. 中存在配位键 中存在配位键 | D.图2晶体的密度为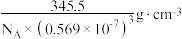 |
您最近一年使用:0次
名校
解题方法
3 . 物质的结构决定其性质,下列实例与解释不 相符的是
| 选项 | 实例 | 解释 |
| A | 邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点 | 分子间氢键使熔沸点升高,分子内氢键使熔沸点降低 |
| B |  与 与 形成配合物 形成配合物 |  中的 中的 有空轨道,可接受 有空轨道,可接受 中 中 的孤电子对 的孤电子对 |
| C |  的沸点高于 的沸点高于 |  原子半径小, 原子半径小, 键能大 键能大 |
| D | 超分子冠醚(18-冠-6)如图所示,其空穴与 尺寸适配 尺寸适配
| 两者能通过弱相互作用(非化学键)形成超分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 .  、
、 与
与 在一定条件下发生如下反应:
在一定条件下发生如下反应: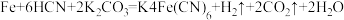 ,下列说法正确的是
,下列说法正确的是
 、
、 与
与 在一定条件下发生如下反应:
在一定条件下发生如下反应: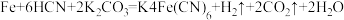 ,下列说法正确的是
,下列说法正确的是A.依据反应方程式可知: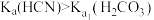 |
B.键角: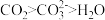 |
C.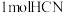 分子中含有 分子中含有 键的数目为 键的数目为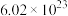 |
D.配合物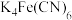 的中心离子的价层电子中有5个未成对电子 的中心离子的价层电子中有5个未成对电子 |
您最近一年使用:0次
5 . 近日,美国斯克利普斯研究所余金权教授课题组成功地实现了Cu(Ⅰ)催化N-甲氧基酰胺的双模式脱氢/内酯化反应,从而将廉价易得的羧酸快速转化为高价值的内酯和脱氢伯酰胺(图中Me为甲基)。下列叙述错误的是
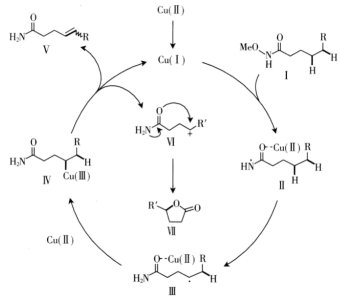
A.Ⅰ→Ⅱ过程中断裂 键 键 | B.Ⅳ中C提供孤电子对与 (Ⅲ)形成配位键 (Ⅲ)形成配位键 |
C.脱氢模式总反应为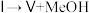 | D.若 和 和 均为烃基,则可用稀硫酸区别Ⅴ和Ⅶ 均为烃基,则可用稀硫酸区别Ⅴ和Ⅶ |
您最近一年使用:0次
6 . 锌是一种重要的金属,锌及其化合物被广泛应用于汽车、建筑、船舶、电池等行业。现某科研小组以固体废锌催化剂(主要成分是 ,含少量
,含少量 、
、 、
、 、
、 等杂质)为原料制备锌的工艺流程如图所示:
等杂质)为原料制备锌的工艺流程如图所示:
①“浸取”时, 和
和 转化为
转化为 、
、 进入溶液。
进入溶液。
② 时,
时, ,
, 。
。
③深度除杂标准:溶液中 ≤2.0×10-6。
≤2.0×10-6。
(1)“浸取”温度为 ,锌的浸出率可达
,锌的浸出率可达 ,继续升温浸出率反而下降,其原因为
,继续升温浸出率反而下降,其原因为___________ 。
(2)“滤渣1”的主要成分为 、
、___________ 。
(3)“深度除锰”是将残留的 转化为
转化为 ,写出该过程的离子方程式
,写出该过程的离子方程式___________ 。
(4)“深度除铜”时,锌的最终回收率,除铜效果(用反应后溶液中的铜锌比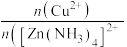 表示)与
表示)与 加入量的关系曲线如图所示。
加入量的关系曲线如图所示。
①当 达到一定量的时候,锌的最终回收率下降的原因是
达到一定量的时候,锌的最终回收率下降的原因是___________ (用离子方程式解释)。
②“深度除铜”时 加入量最优选择
加入量最优选择___________ (填标号)。
A.100% B.110% C.120% D.130%
(5) 原子能形成多种配位化合物,一种锌的配合物结构如图:
原子能形成多种配位化合物,一种锌的配合物结构如图:___________ 。
②基态 原子的价电子排布式为
原子的价电子排布式为___________ 。
 ,含少量
,含少量 、
、 、
、 、
、 等杂质)为原料制备锌的工艺流程如图所示:
等杂质)为原料制备锌的工艺流程如图所示: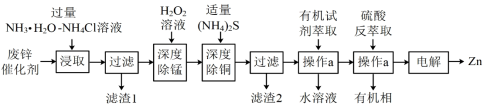
①“浸取”时,
 和
和 转化为
转化为 、
、 进入溶液。
进入溶液。②
 时,
时, ,
, 。
。③深度除杂标准:溶液中
 ≤2.0×10-6。
≤2.0×10-6。(1)“浸取”温度为
 ,锌的浸出率可达
,锌的浸出率可达 ,继续升温浸出率反而下降,其原因为
,继续升温浸出率反而下降,其原因为(2)“滤渣1”的主要成分为
 、
、(3)“深度除锰”是将残留的
 转化为
转化为 ,写出该过程的离子方程式
,写出该过程的离子方程式(4)“深度除铜”时,锌的最终回收率,除铜效果(用反应后溶液中的铜锌比
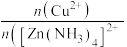 表示)与
表示)与 加入量的关系曲线如图所示。
加入量的关系曲线如图所示。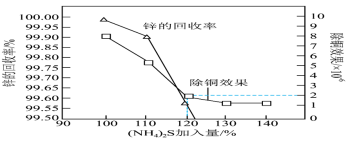
①当
 达到一定量的时候,锌的最终回收率下降的原因是
达到一定量的时候,锌的最终回收率下降的原因是②“深度除铜”时
 加入量最优选择
加入量最优选择A.100% B.110% C.120% D.130%
(5)
 原子能形成多种配位化合物,一种锌的配合物结构如图:
原子能形成多种配位化合物,一种锌的配合物结构如图:
②基态
 原子的价电子排布式为
原子的价电子排布式为
您最近一年使用:0次
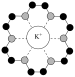
7 .  的结构如图1所示,
的结构如图1所示,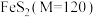 晶胞为立方体,棱长为a nm,如图2所示,设阿伏加德罗常数的值为
晶胞为立方体,棱长为a nm,如图2所示,设阿伏加德罗常数的值为 ,下列说法错误的是
,下列说法错误的是
 的结构如图1所示,
的结构如图1所示,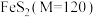 晶胞为立方体,棱长为a nm,如图2所示,设阿伏加德罗常数的值为
晶胞为立方体,棱长为a nm,如图2所示,设阿伏加德罗常数的值为 ,下列说法错误的是
,下列说法错误的是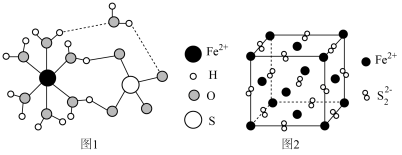
A.图1与图2中的 的配位数都是6 的配位数都是6 |
B.相邻两个 的最短距离为 的最短距离为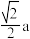 nm nm |
C. 晶胞的密度为 晶胞的密度为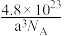 g/cm3 g/cm3 |
D. 中存在配位键、极性键、氢键等化学键 中存在配位键、极性键、氢键等化学键 |
您最近一年使用:0次
解题方法
8 . 某离子液体由原子序数依次增大的短周期元素X、Y、Z、W、M组成,结构简式如图。其中Y、Z位于同周期相邻主族,W和M的p轨道均含一个未成对电子。下列说法正确的是
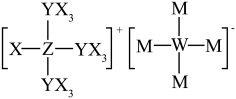
A.简单离子半径: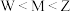 | B.第一电离能: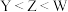 |
| C.该离子液体的阴离子不含有配位键 | D. 中Z的杂化方式为 中Z的杂化方式为 |
您最近一年使用:0次
名校
解题方法
9 . 下列对一些实验事实的理论解释正确的是
| 选项 | 实验事实 | 理论解释 |
| A | 酸性: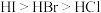 | 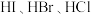 中范德华力逐渐减小 中范德华力逐渐减小 |
| B | 与水反应剧烈程度: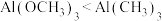 | 键长: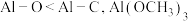 更稳定 更稳定 |
| C |  的稳定性强于 的稳定性强于 |  分子之间存在氢键 分子之间存在氢键 |
| D | 冠醚(18-冠-6)的空穴与 尺寸适配 尺寸适配 | 两者能通过离子键形成超分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 .  与
与 溶液反应的化学方程式为
溶液反应的化学方程式为 。下列说法正确的是
。下列说法正确的是
 与
与 溶液反应的化学方程式为
溶液反应的化学方程式为 。下列说法正确的是
。下列说法正确的是A.基态 原子中含有2个未成对电子 原子中含有2个未成对电子 |
B.每生成 转移电子数为 转移电子数为 |
C.常温下,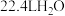 中心原子上含有的孤电子对数是 中心原子上含有的孤电子对数是 |
D. 中的中心离子是 中的中心离子是 ,配位数为3 ,配位数为3 |
您最近一年使用:0次