1 . 黄铜矿的主要成份为 ,现有如下转化关系制备有关物质。
,现有如下转化关系制备有关物质。

已知:沉淀D的摩尔质量为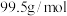 。请回答:
。请回答:
(1)尾气中 经过充分综合利用可以得到石膏,请写出石膏的化学式:
经过充分综合利用可以得到石膏,请写出石膏的化学式:___________ 。
(2)煅烧含硫量高的矿物得到高浓度的 ,干燥的
,干燥的 气体与氯气在活性炭催化下可生成一种用于有机合成的常见物质A,该物质水解时发生非氧化还原反应得到两种强酸。
气体与氯气在活性炭催化下可生成一种用于有机合成的常见物质A,该物质水解时发生非氧化还原反应得到两种强酸。
①写出物质A分子的结构式:___________ 。
②一定压强下,化合物A的沸点低于硫酸的原因是___________ 。
(3)生成沉淀D的离子反应方程式___________ 。
(4)请设计实验检验溶液C中的阳离子___________ 。
 ,现有如下转化关系制备有关物质。
,现有如下转化关系制备有关物质。
已知:沉淀D的摩尔质量为
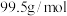 。请回答:
。请回答:(1)尾气中
 经过充分综合利用可以得到石膏,请写出石膏的化学式:
经过充分综合利用可以得到石膏,请写出石膏的化学式:(2)煅烧含硫量高的矿物得到高浓度的
 ,干燥的
,干燥的 气体与氯气在活性炭催化下可生成一种用于有机合成的常见物质A,该物质水解时发生非氧化还原反应得到两种强酸。
气体与氯气在活性炭催化下可生成一种用于有机合成的常见物质A,该物质水解时发生非氧化还原反应得到两种强酸。①写出物质A分子的结构式:
②一定压强下,化合物A的沸点低于硫酸的原因是
(3)生成沉淀D的离子反应方程式
(4)请设计实验检验溶液C中的阳离子
您最近一年使用:0次
解题方法
2 . 工业上以制作印刷电路的废液(含 、
、 、
、 、
、 )生产
)生产 和蚀刻液重新生成的流程如下:
和蚀刻液重新生成的流程如下: 是一种白色粉末,微溶于水、不溶于乙醇。
是一种白色粉末,微溶于水、不溶于乙醇。
请回答下列问题:
(1)Y中所含溶质的化学式为___________ 。
(2)下列说法正确的是___________ 。
A. 微溶于水、不溶于乙醇是因为水的极性比乙醇小
微溶于水、不溶于乙醇是因为水的极性比乙醇小
B.相同条件下,滤渣1和X分别与等浓度的盐酸反应,滤渣①的反应速率快
C. 分子的VSEPR模型为平面三角形
分子的VSEPR模型为平面三角形
D.基态亚铜的价层电子排布式为 ,故
,故 与稀硫酸不反应
与稀硫酸不反应
E.工业上对滤渣2用浓硫酸进行了处理,符合绿色化学的原则
(3)写出上述流程中生成 的化学方程式
的化学方程式___________ 。
(4)浓硫酸是一种高沸点的酸,溶于水放出大量的热,请从物质结构与微粒之间作用力的角度解释上述硫酸的两点性质___________ 。
(5)滤液1需要加过量Z,检验Z过量的方法是___________ 。
 、
、 、
、 、
、 )生产
)生产 和蚀刻液重新生成的流程如下:
和蚀刻液重新生成的流程如下: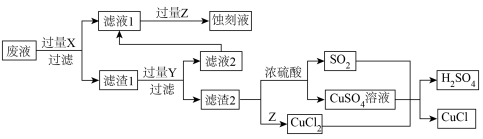
 是一种白色粉末,微溶于水、不溶于乙醇。
是一种白色粉末,微溶于水、不溶于乙醇。请回答下列问题:
(1)Y中所含溶质的化学式为
(2)下列说法正确的是
A.
 微溶于水、不溶于乙醇是因为水的极性比乙醇小
微溶于水、不溶于乙醇是因为水的极性比乙醇小B.相同条件下,滤渣1和X分别与等浓度的盐酸反应,滤渣①的反应速率快
C.
 分子的VSEPR模型为平面三角形
分子的VSEPR模型为平面三角形D.基态亚铜的价层电子排布式为
 ,故
,故 与稀硫酸不反应
与稀硫酸不反应E.工业上对滤渣2用浓硫酸进行了处理,符合绿色化学的原则
(3)写出上述流程中生成
 的化学方程式
的化学方程式(4)浓硫酸是一种高沸点的酸,溶于水放出大量的热,请从物质结构与微粒之间作用力的角度解释上述硫酸的两点性质
(5)滤液1需要加过量Z,检验Z过量的方法是
您最近一年使用:0次
3 . 乙二酸(俗称草酸)是最简单的二元羧酸。下图流程表示其部分转化关系。[已知: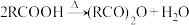 ]
]
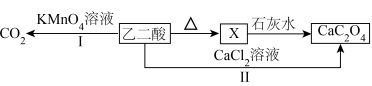
请回答:
(1)草酸是一种重要的还原剂,在分析化学上常被用作测定高锰酸钾溶液浓度的试剂。写出途径Ⅰ反应的离子方程式_____ 。
(2)①X是具有六元环状结构的碳氧化合物,C、O原子均满足8电子结构。写出X的结构式_____ 。
②下列说法正确的是_____ 。
A.X是一种酸性氧化物B.由途径Ⅱ可知,草酸钙不溶于稀盐酸
C.乙二酸的酸性比乙酸强D.乙二酸跟足量乙醇反应生成乙二酸乙二酯
③乙二酸易溶于乙醇,难溶于苯和氯仿,原因是_____ 。
(3)设计实验验证气态化合物X既有氧化性又有还原性_____ 。
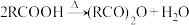 ]
]
请回答:
(1)草酸是一种重要的还原剂,在分析化学上常被用作测定高锰酸钾溶液浓度的试剂。写出途径Ⅰ反应的离子方程式
(2)①X是具有六元环状结构的碳氧化合物,C、O原子均满足8电子结构。写出X的结构式
②下列说法正确的是
A.X是一种酸性氧化物B.由途径Ⅱ可知,草酸钙不溶于稀盐酸
C.乙二酸的酸性比乙酸强D.乙二酸跟足量乙醇反应生成乙二酸乙二酯
③乙二酸易溶于乙醇,难溶于苯和氯仿,原因是
(3)设计实验验证气态化合物X既有氧化性又有还原性
您最近一年使用:0次
4 . 下列化学用语表示正确的是
A. 分子的球棍模型: 分子的球棍模型: |
B. 的VSEPR模型名称是四面体型 的VSEPR模型名称是四面体型 |
C.邻羟基苯甲醛的分子内氢键: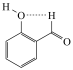 |
D.聚丙烯的结构简式: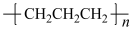 |
您最近一年使用:0次
名校
5 . 质子交换膜氢氧燃料电池具有能量密度高等优点,质子交换膜主要成分为全氟磺酸聚合物,吸水后,强疏水性主链和亲水性侧链形成尺寸为3-5纳米的离子通道。质子通过水、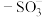 等载体之间氢键的伸缩振动,定向连续传递。电池及膜的工作原理如下图所示,下列说法
等载体之间氢键的伸缩振动,定向连续传递。电池及膜的工作原理如下图所示,下列说法不正确 的是
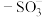 等载体之间氢键的伸缩振动,定向连续传递。电池及膜的工作原理如下图所示,下列说法
等载体之间氢键的伸缩振动,定向连续传递。电池及膜的工作原理如下图所示,下列说法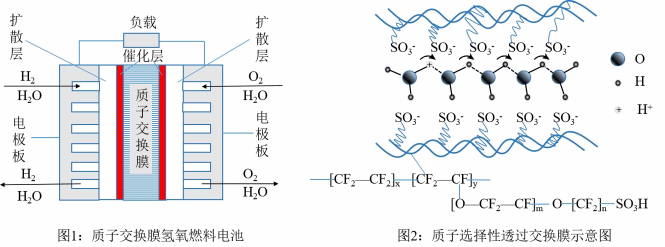
A.通 电极的电势比通 电极的电势比通 电极的电势高 电极的电势高 |
| B.质子交换膜燃料电池的电解质为全氟磺酸聚合物 |
C.给出质子能力: >质子交换膜的 >质子交换膜的 |
| D.质子交换膜吸水后形成离子通道 |
您最近一年使用:0次
2023-12-03更新
|
418次组卷
|
3卷引用:浙江省台州市2023-2024学年高三上学期第一次教学质量评估试题-化学试题卷
浙江省台州市2023-2024学年高三上学期第一次教学质量评估试题-化学试题卷(已下线)专题05 化学反应与能量(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)湖南省衡阳市第八中学2024届高三下学期高考模拟预测化学试题
6 . 已知A、B、C、D是周期表中前三周期元素,且原子序数依次增大,其中A、B、C为同周期的非金属元素,且B、C原子中均有两个未成对电子,D元素s能级与p能级电子数相等,下列说法正确的是
| A.原子半径:A>B>C>D | B.第一电离能:A<B<C<D |
| C.D与 C 可形成高熔点的化合物 | D.最低价气态氢化物的沸点:A<C<B |
您最近一年使用:0次
名校
7 . 铁、钴、镍三种元素位于元素周期表中第4周期第Ⅷ族,通常将铁钴镍三种元素称为铁系元素,请回答:
(1)基态镍原子的价层电子排布式___________
(2)已知无水三氯化铁熔点为307.6℃,沸点约为306℃,可以升华,400℃以下的气态氯化铁主要通过配位键以二聚体形式存在,据此判断氯化铁的晶体类型___________ ,氯化铁二聚体的结构式是___________
(3)铁系元素易通过配位键形成各种多环系化合物,钴酞菁是其中的一种。图1是酞菁和钴酞菁的分子结构,酞菁分子中所有原子共平面,下列说法正确的是___________

(4)邻苯二甲酸酐(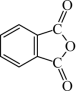 )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺(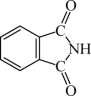 )都是合成酞菁的原料,后者熔点高于前者,主要原因是
)都是合成酞菁的原料,后者熔点高于前者,主要原因是___________ 。
(5)下图为一种常见锂离子电池电极材料的六棱柱结构单元及其沿垂直底面方向的投影图,其底面是正六边形 。
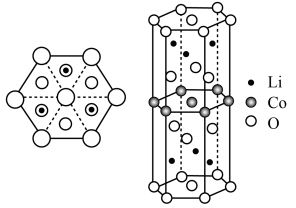
①该电极材料物质的化学式为___________ 。
②该晶体中Li原子周围距离最近且相等的O原子有___________ 个。
(1)基态镍原子的价层电子排布式
(2)已知无水三氯化铁熔点为307.6℃,沸点约为306℃,可以升华,400℃以下的气态氯化铁主要通过配位键以二聚体形式存在,据此判断氯化铁的晶体类型
(3)铁系元素易通过配位键形成各种多环系化合物,钴酞菁是其中的一种。图1是酞菁和钴酞菁的分子结构,酞菁分子中所有原子共平面,下列说法正确的是___________

| A.标注①②的N原子的杂化方式是sp2,③的N原子的杂化方式sp3 |
| B.钴酞菁中元素的电负性由大到小顺序为:N>C>H>Co |
| C.钴酞菁中钴元素的化合价是+2 |
| D.钴酞菁中的作用力有:离子键、氢键、配位键、π键、σ键 |
 )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺( )都是合成酞菁的原料,后者熔点高于前者,主要原因是
)都是合成酞菁的原料,后者熔点高于前者,主要原因是(5)下图为一种常见锂离子电池电极材料的六棱柱结构单元及其沿垂直底面方向的投影图,其底面是

①该电极材料物质的化学式为
②该晶体中Li原子周围距离最近且相等的O原子有
您最近一年使用:0次
解题方法
8 . 碳酸二甲酯 是一种环保性能优异、用途广泛的化工原料,可以通过下列流程制备:
是一种环保性能优异、用途广泛的化工原料,可以通过下列流程制备:

已知:酰氯具有酯的性质。请回答:
(1)写出NH3的电子式_______ 。
(2)写出步骤Ⅲ的化学反应方程式_______ 。
(3)下列说法正确的是_______。
(4)碳酸二甲酯比碳酸一甲酯的沸点_______ (填“低”或“高”),分析其原因_______ 。
(5)设计实验方案检验COCl2中的氯元素_______ 。
 是一种环保性能优异、用途广泛的化工原料,可以通过下列流程制备:
是一种环保性能优异、用途广泛的化工原料,可以通过下列流程制备:
已知:酰氯具有酯的性质。请回答:
(1)写出NH3的电子式
(2)写出步骤Ⅲ的化学反应方程式
(3)下列说法正确的是_______。
| A.液氯和氯水工业上均可用铁槽车运送 |
| B.CO(NH2)2属于铵盐,含氮量高,可作氮肥 |
| C.碳酸二甲酯在酸性条件下水解产生的气体是非极性分子 |
| D.CO与Fe可形成配合物Fe(CO)5,其中配位原子是O |
(4)碳酸二甲酯比碳酸一甲酯的沸点
(5)设计实验方案检验COCl2中的氯元素
您最近一年使用:0次
解题方法
9 . 工业上按如下流程制备硝酸和肼(N2H4)。

(1)途径Ⅰ是工业制硝酸的第一步,写出化学方程式___________ 。
(2) N2H4的制法可通过途径Ⅱ:用过量NH3和CH3CHO的混合物与氯气进行气相反应合成异肼 ,然后使其水解得到肼。
,然后使其水解得到肼。
①下列说法不正确 的是___________ 。
A.NH3属于电解质 B.途径Ⅱ中氯气作还原剂
C.N2、H2、N2H4均为非极性分子 D.异肼中氮的化合价呈负价
②相同条件下,氨的沸点低于肼的主要原因是___________ 。
(3)Zn元素的化学性质与Al相似。Zn与很稀的硝酸反应,氮元素被还原到最低价,写出该反应的离子方程式___________ ;检验反应后溶液中除H+外的阳离子的方法是___________ 。

(1)途径Ⅰ是工业制硝酸的第一步,写出化学方程式
(2) N2H4的制法可通过途径Ⅱ:用过量NH3和CH3CHO的混合物与氯气进行气相反应合成异肼
 ,然后使其水解得到肼。
,然后使其水解得到肼。①下列说法
A.NH3属于电解质 B.途径Ⅱ中氯气作还原剂
C.N2、H2、N2H4均为非极性分子 D.异肼中氮的化合价呈负价
②相同条件下,氨的沸点低于肼的主要原因是
(3)Zn元素的化学性质与Al相似。Zn与很稀的硝酸反应,氮元素被还原到最低价,写出该反应的离子方程式
您最近一年使用:0次
22-23高二下·浙江·期中
解题方法
10 . Ⅰ.试从物质结构角度解释:
(1)邻羟基苯甲醛熔点比对羟基苯甲醛低的原因是:_________ 。
(2)配合物Fe(CO)5中配位原子是_______ ,原因是_______ 。
(3)酸性CH3COOH________ CF3COOH(填>、=或<)。原因是________ 。
Ⅱ.钛(Ti)被称为未来金属,二氧化钛是一种优良的催化剂,可催化如下反应,请回答:

(4)基态Ti原子的价电子排布图为_______ 。
(5)该反应涉及的C、O、N三种元素的第一电离能从大到小的顺序为_______ 。 分子sp2杂化的碳原子个数与sp3杂化的碳原子个数之比为
分子sp2杂化的碳原子个数与sp3杂化的碳原子个数之比为_______ 。
(6)1mol[Ti(H2O)6]Cl3中含有σ键的数目为________ ,与H2O互为等电子体的阴离子为_______ 。
(7)已知N与Ti形成的化合物的晶胞结构如图所示,若晶胞中Ti原子与N原子的最近距离为apm。则该晶胞的密度为________ g•cm-3(阿伏加德罗常数的值为NA,用含有a、NA的代数式表示)

(1)邻羟基苯甲醛熔点比对羟基苯甲醛低的原因是:
(2)配合物Fe(CO)5中配位原子是
(3)酸性CH3COOH
Ⅱ.钛(Ti)被称为未来金属,二氧化钛是一种优良的催化剂,可催化如下反应,请回答:

(4)基态Ti原子的价电子排布图为
(5)该反应涉及的C、O、N三种元素的第一电离能从大到小的顺序为
 分子sp2杂化的碳原子个数与sp3杂化的碳原子个数之比为
分子sp2杂化的碳原子个数与sp3杂化的碳原子个数之比为(6)1mol[Ti(H2O)6]Cl3中含有σ键的数目为
(7)已知N与Ti形成的化合物的晶胞结构如图所示,若晶胞中Ti原子与N原子的最近距离为apm。则该晶胞的密度为

您最近一年使用:0次



