名校
解题方法
1 . 氯及其部分化合物相关转化如下.
(1)常温下, 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:___________ .
(2)下列有关流程中的物质的说法正确的是:_______________.
(3) 与浓硫酸反应可得
与浓硫酸反应可得 (
(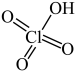 ):
):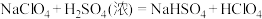 ,利用减压蒸馏分离
,利用减压蒸馏分离 .试解释高氯酸比硫酸易从体系中分离的原因(从结构角度分析):
.试解释高氯酸比硫酸易从体系中分离的原因(从结构角度分析):__________ . 在液态时为双聚体,请写出
在液态时为双聚体,请写出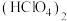 的结构式:
的结构式:___________ .
(4)通过分析,M分子中只有一种化学环境的氢原子. 与
与 经过氧化反应、取代反应,两步生成M和D,写出总反应化学方程式:
经过氧化反应、取代反应,两步生成M和D,写出总反应化学方程式:______________ 。设计实验检验D:_______________ 。

(1)常温下,
 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:(2)下列有关流程中的物质的说法正确的是:_______________.
A.工业上采用软锰矿(主要成分是 )与浓盐酸混合加热制备 )与浓盐酸混合加热制备 |
| B.混合物A、B的物质的量之比为可为5:1 |
C.若C中的各原子最外层均达8电子稳定结构,C确定为 |
D. 具有强氧化性,用作自来水的消毒剂 具有强氧化性,用作自来水的消毒剂 |
(3)
 与浓硫酸反应可得
与浓硫酸反应可得 (
( ):
):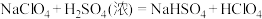 ,利用减压蒸馏分离
,利用减压蒸馏分离 .试解释高氯酸比硫酸易从体系中分离的原因(从结构角度分析):
.试解释高氯酸比硫酸易从体系中分离的原因(从结构角度分析): 在液态时为双聚体,请写出
在液态时为双聚体,请写出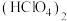 的结构式:
的结构式:(4)通过分析,M分子中只有一种化学环境的氢原子.
 与
与 经过氧化反应、取代反应,两步生成M和D,写出总反应化学方程式:
经过氧化反应、取代反应,两步生成M和D,写出总反应化学方程式:
您最近半年使用:0次
名校
解题方法
2 . 碳、氮和氧是构建化合物的常见元素。请回答:
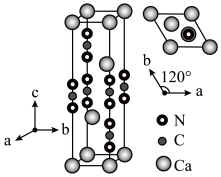
(1)某化合物的晶胞如图,其化学式是___________ ,晶体类型是___________ 。
(2)下列说法正确的是___________。
(3)①聚吡咯作柔性电极材料,其单体为吡咯(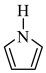 )。吡咯、呋喃(
)。吡咯、呋喃(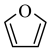 )、噻吩(
)、噻吩(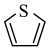 )都是平面杂环化合物,均存在共轭大π键,其中吡咯的N原子杂化方式为
)都是平面杂环化合物,均存在共轭大π键,其中吡咯的N原子杂化方式为___________ ;比较沸点:吡咯___________ 噻吩___________ 呋喃(填“>”、“<”或“=”),请说明理由___________ 。
②同位素示踪实验可证实S2O 中两个S原子的化学环境不同,实验过程为
中两个S原子的化学环境不同,实验过程为 。过程ii中,
。过程ii中,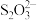 断裂的只有硫硫键,若过程i所用试剂是Na232SO3和35S,过程ii含硫产物是
断裂的只有硫硫键,若过程i所用试剂是Na232SO3和35S,过程ii含硫产物是___________ 。
(1)某化合物的晶胞如图,其化学式是

(2)下列说法正确的是___________。
| A.电负性:B>N>O | B.离子半径:K+<S2−<Cl− |
| C.第一电离能:Ge<As<Se | D.基态Fe2+的简化电子排布式:[Ar]3d6 |
(3)①聚吡咯作柔性电极材料,其单体为吡咯(
 )。吡咯、呋喃(
)。吡咯、呋喃( )、噻吩(
)、噻吩( )都是平面杂环化合物,均存在共轭大π键,其中吡咯的N原子杂化方式为
)都是平面杂环化合物,均存在共轭大π键,其中吡咯的N原子杂化方式为②同位素示踪实验可证实S2O
 中两个S原子的化学环境不同,实验过程为
中两个S原子的化学环境不同,实验过程为 。过程ii中,
。过程ii中,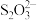 断裂的只有硫硫键,若过程i所用试剂是Na232SO3和35S,过程ii含硫产物是
断裂的只有硫硫键,若过程i所用试剂是Na232SO3和35S,过程ii含硫产物是
您最近半年使用:0次
2024-02-11更新
|
317次组卷
|
2卷引用:浙江省2023-2024学年高三上学期2月 模拟选考化学试题
名校
3 . 回答下列问题
(1)①HClO的结构式为___________ ;
②水分子的空间构型___________ ;
③铁红的化学式___________ ;
(2)相同条件下,冰的密度比水小的原因是___________ ;
(3)氧元素的一种核素,核内有10个中子,该核素的符号可表示为___________ ;
(4)用氯气制备“84”消毒液的离子方程式为___________ ,消毒液消毒衣服时要先用温水稀释后再浸泡一段时间,但温度不能高于50℃。则温度不宜过高的原因是___________ ;
(5)写出铝粉与氢氧化钠溶液的反应的化学方程式,并用单线桥表示电子转移的方向和数目___________ 。
(6) 遇水产生氢气,该反应的化学方程式
遇水产生氢气,该反应的化学方程式___________ 。
(1)①HClO的结构式为
②水分子的空间构型
③铁红的化学式
(2)相同条件下,冰的密度比水小的原因是
(3)氧元素的一种核素,核内有10个中子,该核素的符号可表示为
(4)用氯气制备“84”消毒液的离子方程式为
(5)写出铝粉与氢氧化钠溶液的反应的化学方程式,并用单线桥表示电子转移的方向和数目
(6)
 遇水产生氢气,该反应的化学方程式
遇水产生氢气,该反应的化学方程式
您最近半年使用:0次
4 . 请回答以下问题:
(1)在载人航天器中,通过以下两个反应实现氧的循环:
Ⅰ.

Ⅱ.
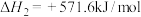
写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式__________ 。
(2)在 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(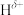 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(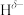 ),这三种元素电负性从大到小的顺序是
),这三种元素电负性从大到小的顺序是__________ 。
(3)100mLpH=10.00的 溶液中水电离出
溶液中水电离出 的物质的量为
的物质的量为__________ mol。
(4)已知:25℃时碳酸的 、
、 ,次氯酸的
,次氯酸的 。写出在NaClO溶液中通入
。写出在NaClO溶液中通入 气体的离子方程式
气体的离子方程式__________ 。
(5)据文献报道, 可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是
可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是__________ 。
(6)锗(Ge)与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是__________ 。
(7)乙醇的挥发性比水的强,原因是__________ 。
(1)在载人航天器中,通过以下两个反应实现氧的循环:
Ⅰ.


Ⅱ.

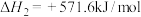
写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式
(2)在
 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(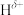 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(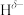 ),这三种元素电负性从大到小的顺序是
),这三种元素电负性从大到小的顺序是(3)100mLpH=10.00的
 溶液中水电离出
溶液中水电离出 的物质的量为
的物质的量为(4)已知:25℃时碳酸的
 、
、 ,次氯酸的
,次氯酸的 。写出在NaClO溶液中通入
。写出在NaClO溶液中通入 气体的离子方程式
气体的离子方程式(5)据文献报道,
 可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是
可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是(6)锗(Ge)与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是
(7)乙醇的挥发性比水的强,原因是
您最近半年使用:0次
5 . 氮元素可形成多种结构和性质特殊的化合物。回答下列问题:
(1)As和氮同主族,基态As原子的核外电子排布式为______ 。
(2)聚吡咯作柔性电极材料,其单体为吡咯(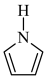 )。吡咯、呋喃(
)。吡咯、呋喃(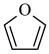 )、噻吩(
)、噻吩(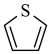 )都是杂环化合物,沸点:吡咯>噻吩>呋喃,原因是
)都是杂环化合物,沸点:吡咯>噻吩>呋喃,原因是______ 。
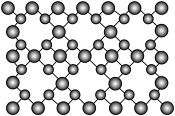
(3)我国科学家用激光将置于铁室中石墨靶上的碳原子炸松,再用射频电火花喷射氮气,获得超硬新材料 -氮化碳薄膜,结构如图。下列有关
-氮化碳薄膜,结构如图。下列有关 -氮化碳的说法错误的是______。
-氮化碳的说法错误的是______。
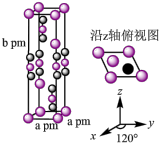
(4)一定条件下, 和
和 反应生成碳单质和化合物X。已知X属于六方晶系,晶胞结构如右图所示,其中碳的化合价为+4价。X的化学式为
反应生成碳单质和化合物X。已知X属于六方晶系,晶胞结构如右图所示,其中碳的化合价为+4价。X的化学式为______ 。 的配位数为
的配位数为______ 。若阿伏加德罗常数的值为 ,该晶体的摩尔体积
,该晶体的摩尔体积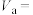
______  (列出算式)。
(列出算式)。
(1)As和氮同主族,基态As原子的核外电子排布式为
(2)聚吡咯作柔性电极材料,其单体为吡咯(
 )。吡咯、呋喃(
)。吡咯、呋喃( )、噻吩(
)、噻吩( )都是杂环化合物,沸点:吡咯>噻吩>呋喃,原因是
)都是杂环化合物,沸点:吡咯>噻吩>呋喃,原因是(3)我国科学家用激光将置于铁室中石墨靶上的碳原子炸松,再用射频电火花喷射氮气,获得超硬新材料
 -氮化碳薄膜,结构如图。下列有关
-氮化碳薄膜,结构如图。下列有关 -氮化碳的说法错误的是______。
-氮化碳的说法错误的是______。
A.与石墨相比, -氮化碳导电性增强 -氮化碳导电性增强 |
B.与金刚石相比, -氮化碳的熔点更高 -氮化碳的熔点更高 |
C. -氮化碳中C、N的杂化方式相同 -氮化碳中C、N的杂化方式相同 |
D. -氮化碳中C原子数与C-N键之比为1∶2 -氮化碳中C原子数与C-N键之比为1∶2 |
(4)一定条件下,
 和
和 反应生成碳单质和化合物X。已知X属于六方晶系,晶胞结构如右图所示,其中碳的化合价为+4价。X的化学式为
反应生成碳单质和化合物X。已知X属于六方晶系,晶胞结构如右图所示,其中碳的化合价为+4价。X的化学式为 的配位数为
的配位数为 ,该晶体的摩尔体积
,该晶体的摩尔体积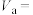
 (列出算式)。
(列出算式)。
您最近半年使用:0次
名校
6 . 下列说法正确的是
| A.硝酸是强电解质,在熔融状态下能导电 |
| B.硝酸分子中含有羟基,可形成分子间氢键,难挥发 |
C.工业制备硝酸第三步时不能用水直接吸收 |
| D.浓硝酸溅到皮肤上,皮肤会变黄 |
您最近半年使用:0次
7 . 下列说法不正确的是
A.键角: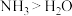 |
B.硬度: |
C.沸点:   |
D.化学键中离子键成分的百分数: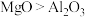 |
您最近半年使用:0次
名校
解题方法
8 . B2O3的气态分子结构如图1所示,硼酸(H3BO3)晶体结构为层状,其二维平面结构如图2所示。下列说法不正确的是
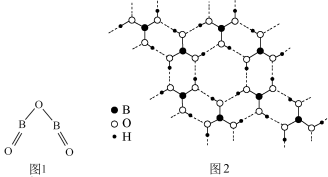

| A.两分子中B原子分别采用sp杂化、sp2杂化 |
| B.硼酸晶体中层与层之前存在范德华力 |
| C.1molH3BO3晶体中含有6mol氢键 |
| D.元素第一电离能:B<Be |
您最近半年使用:0次
2024-01-30更新
|
125次组卷
|
2卷引用:08-2023新东方高二上期中考化学
名校
9 . 下列说法不正确的是
| A.邻羟基苯甲酸的沸点低于对羟基苯甲酸的沸点 |
| B.棉花的葡萄糖结构单元中含有羟基,具有一定的吸湿性 |
| C.苯酚在浓氨水作用下与甲醛反应生成线型热塑性高分子化合物 |
D.18-冠-6(空腔直径260~320pm)能与 (276pm)通过某种相互作用力形成超分子 (276pm)通过某种相互作用力形成超分子 |
您最近半年使用:0次
2024-01-24更新
|
260次组卷
|
2卷引用:浙江省北斗星盟2024届高三上学期12月联考-化学试题
名校
解题方法
10 . 工业上以NH3为原料按如下流程制取化合物A。

已知:水溶液中,ClO-可与 反应生成Cl-
反应生成Cl-
请回答:
(1)写出NH3催化氧化生成NO的化学方程式________ 。
(2)等物质的量的HNO3与ClF反应除生成A外,另一种产物为HF。
①电子衍射研究表明,气态HF中存在环状六聚体(HF)6,而其他卤素的气态氢化物却不存在,气态HF中存在环状六聚体(HF)6的原因是_____ 。
②下列说法正确的是_____ 。
A.尾气的主要成分是NO,可用NaOH溶液直接吸收 B.ClF中的Cl呈零价
C.化合物A具有强氧化性 D.TiCl4与A反应能生成Ti(NO3)4
(3)①设计实验验证化合物A中含有Cl元素___________ 。
②写出实验过程中涉及的反应方程式___________ 。

已知:水溶液中,ClO-可与
 反应生成Cl-
反应生成Cl-请回答:
(1)写出NH3催化氧化生成NO的化学方程式
(2)等物质的量的HNO3与ClF反应除生成A外,另一种产物为HF。
①电子衍射研究表明,气态HF中存在环状六聚体(HF)6,而其他卤素的气态氢化物却不存在,气态HF中存在环状六聚体(HF)6的原因是
②下列说法正确的是
A.尾气的主要成分是NO,可用NaOH溶液直接吸收 B.ClF中的Cl呈零价
C.化合物A具有强氧化性 D.TiCl4与A反应能生成Ti(NO3)4
(3)①设计实验验证化合物A中含有Cl元素
②写出实验过程中涉及的反应方程式
您最近半年使用:0次



