名校
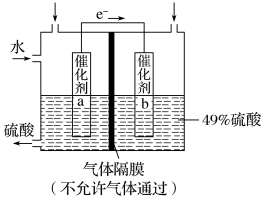
1 . I.如图是利用电化学装置将SO2转化为重要的化工原料H2SO4的原理示意图。
请回答下列问题:
(1)该装置将_______ 能转化为______ 能。
(2)催化剂b表面O2发生_______ 反应,其附近溶液酸性______ (填“增强”、“不变”或“减弱”)。
(3)催化剂a表面的电极反应式:_______ 。
II.某废料铁泥主要成分是Fe2O3、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe2O3,设计实验流程如图:

(4)步骤(I)充分反应后进行的实验操作名称是______ 。
(5)步骤(II)中加入H2O2溶液后需要适当加热但温度不能过高,原因是______ 。
(6)为了检验溶液B中是否有亚铁离子剩余,有同学提出只需要取少量溶液B于试管中并向其中滴加氢氧化钠溶液,然后观察现象即可证明。请你判断该同学的方法是否可行并说出理由______ 。
(7)步骤(III)中将NaOH溶液换成氨气也可以得到Fe(OH)3沉淀,反应的离子方程式为______ 。

请回答下列问题:
(1)该装置将
(2)催化剂b表面O2发生
(3)催化剂a表面的电极反应式:
II.某废料铁泥主要成分是Fe2O3、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe2O3,设计实验流程如图:

(4)步骤(I)充分反应后进行的实验操作名称是
(5)步骤(II)中加入H2O2溶液后需要适当加热但温度不能过高,原因是
(6)为了检验溶液B中是否有亚铁离子剩余,有同学提出只需要取少量溶液B于试管中并向其中滴加氢氧化钠溶液,然后观察现象即可证明。请你判断该同学的方法是否可行并说出理由
(7)步骤(III)中将NaOH溶液换成氨气也可以得到Fe(OH)3沉淀,反应的离子方程式为
您最近一年使用:0次
2023-05-19更新
|
711次组卷
|
2卷引用:江西省宜春市高安市灰埠中学2022-2023学年高一下学期7月期末化学试题
名校
解题方法
2 . 镍基合金是一种适宜于制造涡轮喷气发动机叶片的重要材料。某工厂用红土镍矿(主要成分为NiO,还含有FeO、 、
、 、MgO等)制取金属镍和高效催化剂黄铵铁矾
、MgO等)制取金属镍和高效催化剂黄铵铁矾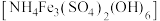 ,工艺流程如下:
,工艺流程如下: 、
、 不能氧化
不能氧化 。
。
②常温下, ,
,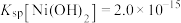 。
。
(1)提高红土镍矿“酸浸”浸取率的措施是___________ (任写一种)。
(2)滤渣的主要成分为___________ ,其重要用途为___________ (任写一种)。
(3)“氧化”时反应的离子方程式为___________ 。“沉铁”时反应的离子方程式为___________ 。
(4)“沉镁”前加入MgO将溶液pH调节至5.5~6.0的原因是___________ 。若调节pH后的溶液中 ,则至少需要加入
,则至少需要加入___________ molNaF 固体“沉镁”,使1L“沉镁”后的溶液中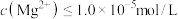 (忽略体积的变化)。
(忽略体积的变化)。
(5)工业上可用如图所示的装置电解 溶液制备Ni和较浓的硫酸,则该电解池的阳极反应式为
溶液制备Ni和较浓的硫酸,则该电解池的阳极反应式为___________ 。
 、
、 、MgO等)制取金属镍和高效催化剂黄铵铁矾
、MgO等)制取金属镍和高效催化剂黄铵铁矾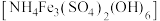 ,工艺流程如下:
,工艺流程如下: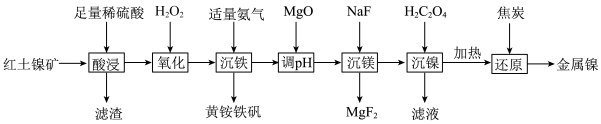
 、
、 不能氧化
不能氧化 。
。②常温下,
 ,
,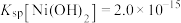 。
。(1)提高红土镍矿“酸浸”浸取率的措施是
(2)滤渣的主要成分为
(3)“氧化”时反应的离子方程式为
(4)“沉镁”前加入MgO将溶液pH调节至5.5~6.0的原因是
 ,则至少需要加入
,则至少需要加入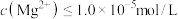 (忽略体积的变化)。
(忽略体积的变化)。(5)工业上可用如图所示的装置电解
 溶液制备Ni和较浓的硫酸,则该电解池的阳极反应式为
溶液制备Ni和较浓的硫酸,则该电解池的阳极反应式为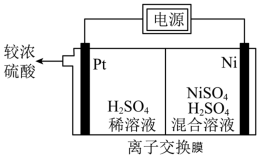
您最近一年使用:0次
2024-04-19更新
|
429次组卷
|
2卷引用:2024届江西省上饶市信州区上饶市第一中学高三下学期模拟预测化学试题
名校
解题方法
3 . 钠长石是地表岩石最重要的造岩矿物,也是工业生产的重要原料。钠长石富含钠元素,同时还有少量的钙和铁元素,铁元素在矿石中既有+2 价 Fe(II)也有+3 价 Fe(III)。钠长石的化学式为:NaxFe4CaO7,以该矿石为原料制备金属钠的工艺流程如下:
请回答下列问题:
(1)“粉碎研磨”的作用是_______ 。
(2)写出 NaClO 与溶液 A 反应的离子方程式_______ 。下面物质中可以替换 NaClO 的是_______ (填字母)。
A.H2O2 B.NaCl C.KMnO4 D.Na2O2
(3)“难溶物 1”的成份是_______ 。(写化学式)
(4)写出制备金属钠的反应方程式_______ 。
(5)溶液 C 中有 Na+还有少量 Ca2+,可用试剂_______ (写化学式)除去 Ca2+。
(6)钠长石中铁元素的化合价有+2 和+3,且 Fe(II)和 Fe(III)的个数比为 3:1,则钠长石的化学式中 x=_______ 。
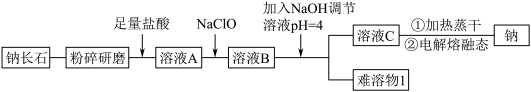
| Ca2+ | Fe2+ | Fe3+ | |
| Mn+完全沉淀时的pH | 12.0 | 5.8 | 4.0 |
(1)“粉碎研磨”的作用是
(2)写出 NaClO 与溶液 A 反应的离子方程式
A.H2O2 B.NaCl C.KMnO4 D.Na2O2
(3)“难溶物 1”的成份是
(4)写出制备金属钠的反应方程式
(5)溶液 C 中有 Na+还有少量 Ca2+,可用试剂
(6)钠长石中铁元素的化合价有+2 和+3,且 Fe(II)和 Fe(III)的个数比为 3:1,则钠长石的化学式中 x=
您最近一年使用:0次
2022-12-21更新
|
524次组卷
|
6卷引用:江西省南昌市第三中学2023-2024学年高一上学期期中考试化学试题
解题方法
4 . 海洋化学资源的综合利用对人类的发展意义重大。
(1)经海水晒盐获得的粗盐水中含有Ca2+、Mg2+、SO 三种杂质离子,为了除去上述三种杂质离子,需加入四种试剂:①Na2CO3、②BaCl2、③NaOH、④稀盐酸。①四种试剂的加入次序正确的是
三种杂质离子,为了除去上述三种杂质离子,需加入四种试剂:①Na2CO3、②BaCl2、③NaOH、④稀盐酸。①四种试剂的加入次序正确的是___________ (填字母)。
a.④①②③ b.②①③④ c.③①②④ d.②③①④
②加入稀盐酸的目的是___________ (用离子方程式表示)。
(2)利用氧化还原反应原理,将Cl2通入提取食盐后的母液中,将溶液中的溴离子转化为溴单质,再鼓入热空气,使溴单质从溶液中分离出来。
①鼓入热空气将溴单质从溶液中分离出来的原理是___________ 。
②将溴离子转化为溴单质的离子反应方程式为___________ 。
(1)经海水晒盐获得的粗盐水中含有Ca2+、Mg2+、SO
 三种杂质离子,为了除去上述三种杂质离子,需加入四种试剂:①Na2CO3、②BaCl2、③NaOH、④稀盐酸。①四种试剂的加入次序正确的是
三种杂质离子,为了除去上述三种杂质离子,需加入四种试剂:①Na2CO3、②BaCl2、③NaOH、④稀盐酸。①四种试剂的加入次序正确的是a.④①②③ b.②①③④ c.③①②④ d.②③①④
②加入稀盐酸的目的是
(2)利用氧化还原反应原理,将Cl2通入提取食盐后的母液中,将溶液中的溴离子转化为溴单质,再鼓入热空气,使溴单质从溶液中分离出来。
①鼓入热空气将溴单质从溶液中分离出来的原理是
②将溴离子转化为溴单质的离子反应方程式为
您最近一年使用:0次
2023-04-30更新
|
271次组卷
|
2卷引用:江西省九江市彭泽县第二高级中学2022-2023学年高一下学期7月期末化学试题
名校
解题方法
5 . 碘化钾( )是实验室常用的化学试剂,用途广泛。一种利用含碘废液(碘的主要存在形式为
)是实验室常用的化学试剂,用途广泛。一种利用含碘废液(碘的主要存在形式为 和
和 )制备碘化钾的实验步骤如下:
)制备碘化钾的实验步骤如下:
步骤Ⅰ:取含碘废液,调节溶液 为
为 ,加入一定量
,加入一定量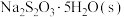 ,溶解,加热至30℃,加入稍过量
,溶解,加热至30℃,加入稍过量 粉末,搅拌,充分反应后,过滤得
粉末,搅拌,充分反应后,过滤得 沉淀;
沉淀;
步骤Ⅱ:在 圆底烧瓶中加入上述制备的
圆底烧瓶中加入上述制备的 沉淀,铁粉(过量),
沉淀,铁粉(过量), 蒸馏水,搅拌,沸水浴加热1小时,冷却,抽滤。将滤液倒入
蒸馏水,搅拌,沸水浴加热1小时,冷却,抽滤。将滤液倒入 烧杯中,加入约
烧杯中,加入约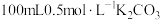 溶液,搅拌,煮沸,静置,过滤,得滤液A;
溶液,搅拌,煮沸,静置,过滤,得滤液A;
步骤Ⅲ:用氢碘酸调滤液A的 ,将滤液倒入___________(填仪器名称)中加热至___________(填现象),冷却,干燥,得到
,将滤液倒入___________(填仪器名称)中加热至___________(填现象),冷却,干燥,得到 晶体。
晶体。
回答下列问题:
(1)步骤Ⅰ中的控温方法为___________ , 与
与 转化为
转化为 的反应为①
的反应为① ,②
,② ,则反应②中氧化剂与还原剂的物质的量之比为
,则反应②中氧化剂与还原剂的物质的量之比为___________ 。
(2)步骤Ⅱ中铁粉转化为 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(3)步骤Ⅲ中,仪器的名称是___________ ,现象是___________ 。
(4)产品中KI含量的测定
称取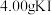 4.00样品,配成
4.00样品,配成 溶液,取
溶液,取 溶液于锥形瓶中,加入
溶液于锥形瓶中,加入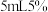 乙酸溶液及3滴曙红钠盐作指示剂,用
乙酸溶液及3滴曙红钠盐作指示剂,用 的
的 标准溶液避光滴定至沉淀呈红色(终点),平行滴定三次,消耗
标准溶液避光滴定至沉淀呈红色(终点),平行滴定三次,消耗 标准溶液分别为
标准溶液分别为 、
、 、
、 。
。
①用 标准溶液滴定时要避光的原因是
标准溶液滴定时要避光的原因是___________ ,在滴定时 溶液应盛放在
溶液应盛放在___________ (“酸式”或“碱式”)滴定管。
②样品中 的质量分数为
的质量分数为___________ 。
 )是实验室常用的化学试剂,用途广泛。一种利用含碘废液(碘的主要存在形式为
)是实验室常用的化学试剂,用途广泛。一种利用含碘废液(碘的主要存在形式为 和
和 )制备碘化钾的实验步骤如下:
)制备碘化钾的实验步骤如下:步骤Ⅰ:取含碘废液,调节溶液
 为
为 ,加入一定量
,加入一定量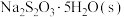 ,溶解,加热至30℃,加入稍过量
,溶解,加热至30℃,加入稍过量 粉末,搅拌,充分反应后,过滤得
粉末,搅拌,充分反应后,过滤得 沉淀;
沉淀;步骤Ⅱ:在
 圆底烧瓶中加入上述制备的
圆底烧瓶中加入上述制备的 沉淀,铁粉(过量),
沉淀,铁粉(过量), 蒸馏水,搅拌,沸水浴加热1小时,冷却,抽滤。将滤液倒入
蒸馏水,搅拌,沸水浴加热1小时,冷却,抽滤。将滤液倒入 烧杯中,加入约
烧杯中,加入约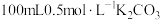 溶液,搅拌,煮沸,静置,过滤,得滤液A;
溶液,搅拌,煮沸,静置,过滤,得滤液A;步骤Ⅲ:用氢碘酸调滤液A的
 ,将滤液倒入___________(填仪器名称)中加热至___________(填现象),冷却,干燥,得到
,将滤液倒入___________(填仪器名称)中加热至___________(填现象),冷却,干燥,得到 晶体。
晶体。回答下列问题:
(1)步骤Ⅰ中的控温方法为
 与
与 转化为
转化为 的反应为①
的反应为① ,②
,② ,则反应②中氧化剂与还原剂的物质的量之比为
,则反应②中氧化剂与还原剂的物质的量之比为(2)步骤Ⅱ中铁粉转化为
 ,该反应的化学方程式为
,该反应的化学方程式为(3)步骤Ⅲ中,仪器的名称是
(4)产品中KI含量的测定
称取
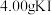 4.00样品,配成
4.00样品,配成 溶液,取
溶液,取 溶液于锥形瓶中,加入
溶液于锥形瓶中,加入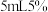 乙酸溶液及3滴曙红钠盐作指示剂,用
乙酸溶液及3滴曙红钠盐作指示剂,用 的
的 标准溶液避光滴定至沉淀呈红色(终点),平行滴定三次,消耗
标准溶液避光滴定至沉淀呈红色(终点),平行滴定三次,消耗 标准溶液分别为
标准溶液分别为 、
、 、
、 。
。①用
 标准溶液滴定时要避光的原因是
标准溶液滴定时要避光的原因是 溶液应盛放在
溶液应盛放在②样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
2024-01-02更新
|
210次组卷
|
2卷引用:江西省部分地区2023-2024学年高三上学期11月期中化学试题
名校
解题方法
6 . 硅是带来人类文明的重要元素之一,硅与二氧化硅广泛应用于通讯行业。
(1)工业上常用石英砂与焦炭在高温下反应制粗硅,其化学方程式是___________ 。
(2)工业上可以通过如图所示的流程制取纯硅:___________ 。
②整个过程中必须严格控制无氧。在有氧环境下,除了有不安全因素外还可能使产品中混有杂质___________ 。整个过程中可以循环利用的物质是___________ (填化学式)。
(3)如图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。___________ 。
②将洗净的石英砂研磨成粉末,目的是___________ 。
③在以上流程中,能否将盐酸改为NaOH溶液,请说明理由___________ 。
(1)工业上常用石英砂与焦炭在高温下反应制粗硅,其化学方程式是
(2)工业上可以通过如图所示的流程制取纯硅:
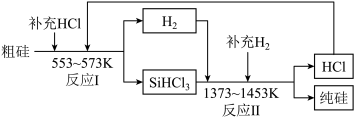
②整个过程中必须严格控制无氧。在有氧环境下,除了有不安全因素外还可能使产品中混有杂质
(3)如图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。
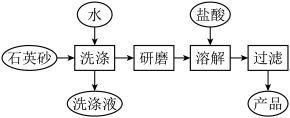
②将洗净的石英砂研磨成粉末,目的是
③在以上流程中,能否将盐酸改为NaOH溶液,请说明理由
您最近一年使用:0次
2023-07-06更新
|
199次组卷
|
4卷引用:江西省萍乡市安源中学2022-2023学年高一下学期期中考试化学试题
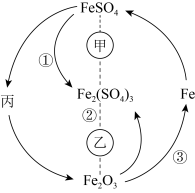
7 . 在一定条件下,某些物质具有如图所示的转化关系。丙为白色固体,其悬浊液在空气中会迅速变为灰绿色,最终变为红褐色。请回答下列问题: 表示一定条件下A能一步转化为B,A……B表示一定条件下A能与B反应。
表示一定条件下A能一步转化为B,A……B表示一定条件下A能与B反应。
(1)根据分析可知丙为______ (填化学式);甲可能是______ (填标号,下同),乙可能是______ 。
A.稀硝酸 B. 溶液
溶液
C. D.
D. 溶液
溶液
(2)实验室保存 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量______ (填药品名称);可以用______ (填化学式)溶液来检验 溶液中的
溶液中的 是否被氧化。
是否被氧化。
(3)丙的悬浊液在空气中变色的原因为______ (填化学方程式);工业上高炉炼铁可以实现③的转化,所得到的炽热的铁水注入模具之前,模具必须进行充分的干燥处理,原因是______ (填化学方程式)。
(4)绿矾 常用于制备铁触媒催化剂。隔绝空气条件下,
常用于制备铁触媒催化剂。隔绝空气条件下, 绿矾受热过程中固体的质量随温度变化的曲线如图所示,加热至
绿矾受热过程中固体的质量随温度变化的曲线如图所示,加热至 时,绿矾发生反应的化学方程式为
时,绿矾发生反应的化学方程式为______ ; 点对应的固体是一种金属氧化物,该物质的化学式为
点对应的固体是一种金属氧化物,该物质的化学式为______ 。
 表示一定条件下A能一步转化为B,A……B表示一定条件下A能与B反应。
表示一定条件下A能一步转化为B,A……B表示一定条件下A能与B反应。(1)根据分析可知丙为
A.稀硝酸 B.
 溶液
溶液C.
 D.
D. 溶液
溶液(2)实验室保存
 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量 溶液中的
溶液中的 是否被氧化。
是否被氧化。(3)丙的悬浊液在空气中变色的原因为
(4)绿矾
 常用于制备铁触媒催化剂。隔绝空气条件下,
常用于制备铁触媒催化剂。隔绝空气条件下, 绿矾受热过程中固体的质量随温度变化的曲线如图所示,加热至
绿矾受热过程中固体的质量随温度变化的曲线如图所示,加热至 时,绿矾发生反应的化学方程式为
时,绿矾发生反应的化学方程式为 点对应的固体是一种金属氧化物,该物质的化学式为
点对应的固体是一种金属氧化物,该物质的化学式为
您最近一年使用:0次
2024-03-27更新
|
163次组卷
|
5卷引用:江西省部分地区2023-2024学年高一下学期3月月考化学试题
8 . 自1943年侯德榜先生发明侯氏制碱法以来,我国纯碱工业高速发展。纯碱作为基本化工原料,被广泛应用于造纸、冶金、纺织、石油、国防、医药等领域,纯碱同时也是制造其他化学品的原料。可以用如图装置模拟侯氏制碱法,根据所学知识回答下列问题:

(1)仪器 的名称为
的名称为_____ ;仪器 的作用为
的作用为_____ 。
(2)装置 中生成
中生成 的反应的化学方程式为
的反应的化学方程式为_____ 。装置C中反应的离子方程式为_____ 。
(3)通过对粗盐(含有 杂质,杂质在实际生产中还容易造成设备堵塞)进行精制可制得饱和
杂质,杂质在实际生产中还容易造成设备堵塞)进行精制可制得饱和 溶液,涉及步骤如下:
溶液,涉及步骤如下:
①加入过量 溶液②加入过量
溶液②加入过量 溶液③加入足量盐酸④过滤⑤蒸发浓缩⑥加入过量
溶液③加入足量盐酸④过滤⑤蒸发浓缩⑥加入过量 溶液正确的操作顺序为_____(填标号)。
溶液正确的操作顺序为_____(填标号)。
(4)实验室模拟侯氏制碱法首先制得的是 ,然后将其在
,然后将其在_____ (填仪器名称)中,进一步制得纯碱。
(5)在实际生产中为了得到更多的产品,经常加入适量的食盐促进产品的析出,这会导致所得的 产品中混有少量
产品中混有少量 。为了确定加热后固体的组成,某化学兴趣小组准确称取
。为了确定加热后固体的组成,某化学兴趣小组准确称取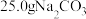 产品,配制成
产品,配制成 溶液,向所得溶液中加入
溶液,向所得溶液中加入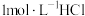 溶液,所得气体体积(已折算为标准状况)与加入盐酸体积的关系如图所示。
溶液,所得气体体积(已折算为标准状况)与加入盐酸体积的关系如图所示。
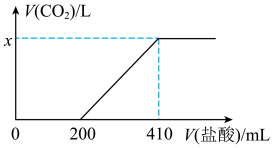
①由已知条件及图像分析, 产品中的杂质为
产品中的杂质为_____ (填化学式)。
②图中
_____ ;若每制得 该样品平均消耗标准状况下
该样品平均消耗标准状况下 ,则在合成
,则在合成 时
时 的转化率为
的转化率为_____ (保留两位小数)%。

(1)仪器
 的名称为
的名称为 的作用为
的作用为(2)装置
 中生成
中生成 的反应的化学方程式为
的反应的化学方程式为(3)通过对粗盐(含有
 杂质,杂质在实际生产中还容易造成设备堵塞)进行精制可制得饱和
杂质,杂质在实际生产中还容易造成设备堵塞)进行精制可制得饱和 溶液,涉及步骤如下:
溶液,涉及步骤如下:①加入过量
 溶液②加入过量
溶液②加入过量 溶液③加入足量盐酸④过滤⑤蒸发浓缩⑥加入过量
溶液③加入足量盐酸④过滤⑤蒸发浓缩⑥加入过量 溶液正确的操作顺序为_____(填标号)。
溶液正确的操作顺序为_____(填标号)。| A.①④⑥④②④③⑤ | B.⑥①②④③⑤ |
| C.②⑥①④③⑤ | D.⑥①②③④⑤ |
(4)实验室模拟侯氏制碱法首先制得的是
 ,然后将其在
,然后将其在(5)在实际生产中为了得到更多的产品,经常加入适量的食盐促进产品的析出,这会导致所得的
 产品中混有少量
产品中混有少量 。为了确定加热后固体的组成,某化学兴趣小组准确称取
。为了确定加热后固体的组成,某化学兴趣小组准确称取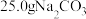 产品,配制成
产品,配制成 溶液,向所得溶液中加入
溶液,向所得溶液中加入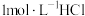 溶液,所得气体体积(已折算为标准状况)与加入盐酸体积的关系如图所示。
溶液,所得气体体积(已折算为标准状况)与加入盐酸体积的关系如图所示。
①由已知条件及图像分析,
 产品中的杂质为
产品中的杂质为②图中

 该样品平均消耗标准状况下
该样品平均消耗标准状况下 ,则在合成
,则在合成 时
时 的转化率为
的转化率为
您最近一年使用:0次
2023-11-22更新
|
444次组卷
|
2卷引用:江西省赣州市十八县23校2023-2024学年高二上学期期中联考化学试题
名校
9 . 自古至今,铁及其化合物在人类生产生活中的使用发挥了巨大的作用。
(1)四大发明之一的司南是由天然磁石制成的,其主要成分是___________ (填化学式) 。
(2)由于Fe(OH)2易被氧化,所以制备时常隔绝空气制备,写出Fe(OH)2露置在空气中被氧化的化学方程式___________ 。
(3)某工业废渣wg (主要含二氧化硅、氧化铁、氧化镁)中提取氧化铁的工业流程如图(部分操作和条件略):
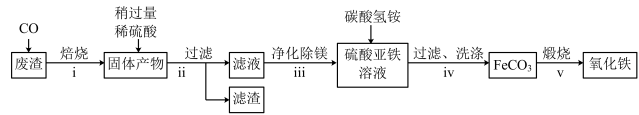
提示:二氧化硅不溶于稀硫酸。
①验证硫酸亚铁溶液中是否存在Fe3+的常用的试剂是___________ (填化学式)。
②步骤Ⅴ中,发生反应的化学方程式为___________ 。
③若提取过程中铁元素的损耗忽略不计,最终获得n g的氧化铁。则废渣中铁元素的质量分数为___________ 。
(1)四大发明之一的司南是由天然磁石制成的,其主要成分是
(2)由于Fe(OH)2易被氧化,所以制备时常隔绝空气制备,写出Fe(OH)2露置在空气中被氧化的化学方程式
(3)某工业废渣wg (主要含二氧化硅、氧化铁、氧化镁)中提取氧化铁的工业流程如图(部分操作和条件略):

提示:二氧化硅不溶于稀硫酸。
①验证硫酸亚铁溶液中是否存在Fe3+的常用的试剂是
②步骤Ⅴ中,发生反应的化学方程式为
③若提取过程中铁元素的损耗忽略不计,最终获得n g的氧化铁。则废渣中铁元素的质量分数为
您最近一年使用:0次
2023-07-10更新
|
306次组卷
|
2卷引用:江西省宁冈中学2023-2024学年高二上学期开学考试化学试题
10 . 下列A、B、C、D是中学常见的混合物分离或提纯的基本装置.

请根据混合物分离或提纯的原理,将A、B、C、D 填入适当的空格中.
(1)用四氯化碳碘水中提取碘_____ ;
(2)除去粗盐中的泥沙_____ ;
(3)与海水晒盐原理相似的是_____ ;
(4)分离CCl4(沸点:76.75℃)和甲苯(沸点:110.6℃)的混合物_____ .

请根据混合物分离或提纯的原理,将A、B、C、D 填入适当的空格中.
(1)用四氯化碳碘水中提取碘
(2)除去粗盐中的泥沙
(3)与海水晒盐原理相似的是
(4)分离CCl4(沸点:76.75℃)和甲苯(沸点:110.6℃)的混合物
您最近一年使用:0次
2019-07-01更新
|
740次组卷
|
7卷引用:江西省上饶县中学2018-2019学年新高一下学期第二次月考化学试题
江西省上饶县中学2018-2019学年新高一下学期第二次月考化学试题(已下线)2019年8月31日 《每日一题》 必修1 周末培优苏教版(2019)新教材化学同步.2.1.1 实验安全与基本规范 物质的分离提纯练习甘肃省庆阳市宁县第二中学2019-2020学年高一上学期第一次月考化学试题(已下线)2.1.1 实验安全与基本规范 物质的分离提纯 练习(2)——《高中新教材同步备课》(苏教版 必修第一册)(已下线)练习5 常见物质的分离和提纯-2020-2021学年【补习教材·寒假作业】高一化学(苏教版)四川省荥经中学2020-2021学年高一上学期中检测化学试题



