名校
解题方法
1 . 工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH接近4时,Fe3+以Fe(OH)3的形式完全沉淀。回答下列问题:
(1)为除去溶液中的Fe2+,可先加入_______ ,(从下面四个选项选择)将Fe2+氧化为Fe3+,反应的离子方程式为_______ ,然后加入适量的_______ ,(从下面四个选项选择)调整溶液的pH使Fe3+转化为Fe(OH)3沉淀。
A.CuO B.Cl2 C.Cu(OH)2 D.H2O2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp = 1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3mol•L-1,则Cu(OH)2开始沉淀时溶液的pH为___________ ,Fe3+完全沉淀时溶液的pH为___________ ,通过计算即可确定上述方案是否可行。
(1)为除去溶液中的Fe2+,可先加入
A.CuO B.Cl2 C.Cu(OH)2 D.H2O2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp = 1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3mol•L-1,则Cu(OH)2开始沉淀时溶液的pH为
您最近一年使用:0次
2021-08-24更新
|
1679次组卷
|
9卷引用:吉林省延边第二中学2020-2021学年高二上学期第二次考试月考化学试题
吉林省延边第二中学2020-2021学年高二上学期第二次考试月考化学试题吉林省汪清县第六中学2021-2022学年高二12月月考化学试题吉林省延边第二中学2022-2023学年高二上学期期末考试化学试题河南省洛阳市2020-2021学年高二上学期期中考试化学试题(已下线)第三章 水溶液中的离子反应与平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)山东省莱西市第一中学2020-2021学年高二上学期12月月考化学试题课选择性必修1 专题3 第四单元 课时2 Ksp相关计算及其图像分析(已下线)第三章第四节 难溶电解的溶解平衡(备作业)-【上好课】2021-2022学年高二化学选修4同步备课系列(人教版)3.4.2沉淀溶解平衡原理的应用 课后
名校
解题方法
2 . 过二硫酸盐[例:(NH4)2S2O8、Na2S2O8]都具有强氧化性,可作为氧化剂和漂白剂,(NH4)2S2O8被广泛用于蓄电池工业,在照相工业上用来除去海波。
I.(NH4)2S2O8的制备原理为H2O2+2H2SO4+2NH3=(NH4)2S2O8+2H2O。实验室模拟制备(NH4)2S2O8的装置如图所示。
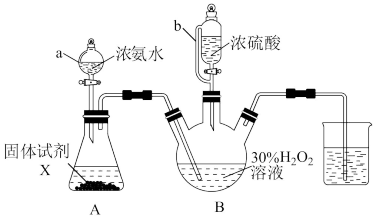
(1)仪器a的名称是________ 。
(2)充分反应后,将B中混合液经一系列操作得到晶体,用无水乙醚洗涤,目的是______ 。
(3)烘干产品时,用红外灯低温供干,可能的原因是_______ 。
II.(NH4)2S2O8的性质及应用。
(4)过二硫酸(H2S2O8)是一种强氧化性酸,在Ag+催化作用下, 能与Mn2+在水溶液中发生反应生成
能与Mn2+在水溶液中发生反应生成 和
和 ,1mol
,1mol 能氧化的Mn2+的物质的量为
能氧化的Mn2+的物质的量为_____ mol。过二硫酸铵可用于检验废水中的Cr3+是否超标,如果超标,溶液会变成橙色(还原产物为 ),写出该反应的离子方程式
),写出该反应的离子方程式______ 。
III.标定(NH4)2S2O8溶液的浓度。
(5)称取一定质量的(NH4)2S2O8,配制成溶液,并用碘量法标定该溶液的浓度,移取20.00mL(NH4)2S2O8溶液于锥形瓶中,加入过量的KI,然后加入几滴淀粉溶液,再用0.1mol·L-1的Na2S2O3溶液滴定,发生反应:I2+2 =2I-+
=2I-+ 。重复上述操作三次,平均消耗Na2S2O3溶液的体积为18.40mL,滴定终点时的颜色变化为
。重复上述操作三次,平均消耗Na2S2O3溶液的体积为18.40mL,滴定终点时的颜色变化为______ ,所标定的(NH4)2S2O8的浓度为________ mol∙L-1。
I.(NH4)2S2O8的制备原理为H2O2+2H2SO4+2NH3=(NH4)2S2O8+2H2O。实验室模拟制备(NH4)2S2O8的装置如图所示。

(1)仪器a的名称是
(2)充分反应后,将B中混合液经一系列操作得到晶体,用无水乙醚洗涤,目的是
(3)烘干产品时,用红外灯低温供干,可能的原因是
II.(NH4)2S2O8的性质及应用。
(4)过二硫酸(H2S2O8)是一种强氧化性酸,在Ag+催化作用下,
 能与Mn2+在水溶液中发生反应生成
能与Mn2+在水溶液中发生反应生成 和
和 ,1mol
,1mol 能氧化的Mn2+的物质的量为
能氧化的Mn2+的物质的量为 ),写出该反应的离子方程式
),写出该反应的离子方程式III.标定(NH4)2S2O8溶液的浓度。
(5)称取一定质量的(NH4)2S2O8,配制成溶液,并用碘量法标定该溶液的浓度,移取20.00mL(NH4)2S2O8溶液于锥形瓶中,加入过量的KI,然后加入几滴淀粉溶液,再用0.1mol·L-1的Na2S2O3溶液滴定,发生反应:I2+2
 =2I-+
=2I-+ 。重复上述操作三次,平均消耗Na2S2O3溶液的体积为18.40mL,滴定终点时的颜色变化为
。重复上述操作三次,平均消耗Na2S2O3溶液的体积为18.40mL,滴定终点时的颜色变化为
您最近一年使用:0次
2022-01-11更新
|
353次组卷
|
6卷引用:吉林省白山市2021-2022学年高三上学期期末考试化学试题
名校
解题方法
3 . 钠长石是地表岩石最重要的造岩矿物,也是工业生产的重要原料。钠长石富含钠元素,同时还有少量的钙和铁元素,铁元素在矿石中既有+2 价 Fe(II)也有+3 价 Fe(III)。钠长石的化学式为:NaxFe4CaO7,以该矿石为原料制备金属钠的工艺流程如下:
请回答下列问题:
(1)“粉碎研磨”的作用是_______ 。
(2)写出 NaClO 与溶液 A 反应的离子方程式_______ 。下面物质中可以替换 NaClO 的是_______ (填字母)。
A.H2O2 B.NaCl C.KMnO4 D.Na2O2
(3)“难溶物 1”的成份是_______ 。(写化学式)
(4)写出制备金属钠的反应方程式_______ 。
(5)溶液 C 中有 Na+还有少量 Ca2+,可用试剂_______ (写化学式)除去 Ca2+。
(6)钠长石中铁元素的化合价有+2 和+3,且 Fe(II)和 Fe(III)的个数比为 3:1,则钠长石的化学式中 x=_______ 。
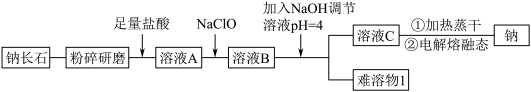
| Ca2+ | Fe2+ | Fe3+ | |
| Mn+完全沉淀时的pH | 12.0 | 5.8 | 4.0 |
(1)“粉碎研磨”的作用是
(2)写出 NaClO 与溶液 A 反应的离子方程式
A.H2O2 B.NaCl C.KMnO4 D.Na2O2
(3)“难溶物 1”的成份是
(4)写出制备金属钠的反应方程式
(5)溶液 C 中有 Na+还有少量 Ca2+,可用试剂
(6)钠长石中铁元素的化合价有+2 和+3,且 Fe(II)和 Fe(III)的个数比为 3:1,则钠长石的化学式中 x=
您最近一年使用:0次
2022-12-21更新
|
524次组卷
|
6卷引用:吉林省松原市2022-2023学年高一上学期期中化学试题
解题方法
4 . 除去Na2CO3粉末中少量NaHCO3的方法是___ ,所涉及的化学反应方程式是___ 。
您最近一年使用:0次
2020-11-14更新
|
755次组卷
|
2卷引用:吉林省长春市榆树高级中学2020-2021学年高一上学期期中考试化学试题
真题
名校
5 . 用含有A1203、SiO2和少量FeO·xFe2O3的铝灰制备A12(SO4)3·18H2O。,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)H2SO4溶解A12O3的离子方程式是_______________ 1;
(2)KMnO4-氧化Fe2+的离子方程式补充完整:______
 1MnO
1MnO +
+ Fe2++
Fe2++ ______=
______= Mn2++
Mn2++ Fe3++
Fe3++ ______
______
(3)已知:
生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol·L-1
根据表中数据解释步骤Ⅱ的目的:._________________ ;
(4)已知:一定条件下,MnO 可与Mn2+反应生成MnO2,
可与Mn2+反应生成MnO2,
①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是_____________ ;
②Ⅳ中加入MnSO4的目的是:______________ ;
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)H2SO4溶解A12O3的离子方程式是
(2)KMnO4-氧化Fe2+的离子方程式补充完整:
 1MnO
1MnO +
+ Fe2++
Fe2++ ______=
______= Mn2++
Mn2++ Fe3++
Fe3++ ______
______(3)已知:
生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
根据表中数据解释步骤Ⅱ的目的:.
(4)已知:一定条件下,MnO
 可与Mn2+反应生成MnO2,
可与Mn2+反应生成MnO2,①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是
②Ⅳ中加入MnSO4的目的是:
您最近一年使用:0次
2019-01-30更新
|
1889次组卷
|
4卷引用:吉林省长春外国语学校2020-2021学年高一下学期期初考试化学试题
吉林省长春外国语学校2020-2021学年高一下学期期初考试化学试题2013年全国普通高等学校招生统一考试理科综合能力测试化学(北京卷)(已下线)2014届高考化学二轮复习四川配套训练 第10讲金属元素化合物练习卷河南省范县第一中学2021-2022学年高一上学期第三次月考检测化学试题
名校
6 . 食盐是人类生活中不可缺少的物质,海水中含有大量食盐。某地出产的粗盐中,所含杂质是CaCl2,通过下面的实验可制得纯净的NaCl。
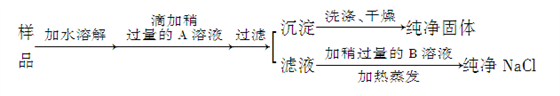
请回答:
(1)加入的A是__________ ,检验A已过量的方法是___________ 。
(2)加入的B是__________ ,加入稍过量B的目的是__________ 。
(3)为检验沉淀是否洗净,最好在最后几滴洗出液中加入_________________ 溶液。

请回答:
(1)加入的A是
(2)加入的B是
(3)为检验沉淀是否洗净,最好在最后几滴洗出液中加入
您最近一年使用:0次
2017-09-13更新
|
853次组卷
|
7卷引用:吉林省公主岭市范家屯镇第一中学2019-2020学年高一上学期期末考试化学试题
吉林省公主岭市范家屯镇第一中学2019-2020学年高一上学期期末考试化学试题河南省周口市中英文学校2018届高三上学期开学摸底考试化学试题江西省南昌市第十中学2019-2020学年高一上学期期中考试化学试题人教版2019必修第二册 第五章 第一节 第2课时 硫酸 硫酸根离子的检验山西省晋中市寿阳县第一中学2019—2020学年高一上学期第二次月考化学试题内蒙古包头市一机一中2021-2022学年高一上学期10月月考化学试题(已下线)第03讲 硫酸根离子的检验 含硫物质的转化(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)
7 . 海水是一种丰富的资源,工业上可从海水中提取多种物质,广泛应用于生活、生产、科技等方面。下图是某工厂对海水资源进行综合利用的示意图。

回答下列问题:
(1)流程图中操作a的名称为________ 。(填序号)
A、蒸发结晶 B、降温结晶
(2)生产生石灰的方程式__________________________ 。从离子反应的角度思考,往海水中加入石灰乳的作用是____________________ 。
(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是_____________ 。
②操作b是在________ 氛围中进行,若在空气中加热,则会生成Mg(OH)2,
写出有关反应的化学方程式:________________________________________ 。
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为__________ ,从考虑成本和废物循环利用的角度,副产物氯气可以用于_______________ 。

回答下列问题:
(1)流程图中操作a的名称为
A、蒸发结晶 B、降温结晶
(2)生产生石灰的方程式
(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是
②操作b是在
写出有关反应的化学方程式:
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为
您最近一年使用:0次
2019-01-19更新
|
465次组卷
|
2卷引用:【全国百强校】吉林省长春市外国语学校2018-2019学年高二上学期期末考试化学试题
9-10高一下·海南·期末
名校
8 . 有下列物质的转化或分离方法:
A.溶解 B.裂解 C.分馏 D.裂化 E.干馏 F.蒸馏 G.电解 H.过滤 I.萃取
请将所选方法的字母代号填在横线上(每一项只填写一种最主要的方法)。
(1)把煤转化为焦炉气、煤焦油和焦炭等___________________ 。
(2)从原油中分离出汽油、煤油、柴油等___________________ 。
(3)将海水淡化________________________________________ 。
(4)除去粗盐溶液中的泥沙______________________________ 。
(5)从海水得到的无水MgCl2中提取金属镁_________________ 。
(6)从海水提溴获得的溴水中提取溴单质__________________ 。
A.溶解 B.裂解 C.分馏 D.裂化 E.干馏 F.蒸馏 G.电解 H.过滤 I.萃取
请将所选方法的字母代号填在横线上(每一项只填写一种最主要的方法)。
(1)把煤转化为焦炉气、煤焦油和焦炭等
(2)从原油中分离出汽油、煤油、柴油等
(3)将海水淡化
(4)除去粗盐溶液中的泥沙
(5)从海水得到的无水MgCl2中提取金属镁
(6)从海水提溴获得的溴水中提取溴单质
您最近一年使用:0次
2016-12-08更新
|
1355次组卷
|
15卷引用:吉林省延边朝鲜族自治州汪清县第四中学2019-2020学年高二上学期第一次阶段考试化学试题
吉林省延边朝鲜族自治州汪清县第四中学2019-2020学年高二上学期第一次阶段考试化学试题(已下线)09—10年海南嘉积中学高一下学期期末考试化学卷(理科)(已下线)2011-2012学年陕西省宝鸡中学高一下学期期中考试化学试卷(已下线)2011-2012学年辽宁省实验中学分校高一下学期期末考试化学试卷陕西省西安市碑林区西安建筑科技大学附属中学2016-2017学年高一下学期期末考试化学试题2017-2018学年高中化学人教版必修2:第四章检测题(已下线)2018年5月26日 周末培优——《每日一题》2017-2018学年高一化学人教必修2甘肃省临泽县第一中学2017-2018学年高一下学期6月月考化学试题高一化学暑假作业:作业十八 阶段检测(四)甘肃省临泽一中2018-2019学年高一下学期期末模拟化学试题河南省周口中英文学校2018-2019学年高一下学期期末考试化学试题云南省楚雄市楚雄实验中学2019-2020学年高二上学期期末考试化学试题新疆乌鲁木齐市第四中学2020-2021学年高二上学期期末考试化学试题(人教版2019)必修第二册 第八章 化学与可持续发展 章末综合检测卷山西省太原市英才学校高中部2021-2022学年高一下学期6月考化学试题
名校
9 . 将粗盐溶于水,为了除去粗盐中的CaCl2,MgCl2,Na2SO4杂质得到纯净氯化钠。需要加入一些试剂。
(1)除去CaCl2需要加入试剂_________________________ ,写出发生反应化学方程式______________________________________________
(2)除去MgCl2需要加入试剂_________________________ ,写出发生反应化学方程式______________________________________________
(3)除去Na2SO4需要加入试剂_________________________ ,写出发生反应化学方程式______________________________________________
(1)除去CaCl2需要加入试剂
(2)除去MgCl2需要加入试剂
(3)除去Na2SO4需要加入试剂
您最近一年使用:0次
2018-10-26更新
|
457次组卷
|
3卷引用:吉林省油田第十一中学2019-2020学年高一上学期第一次月考化学试题
10 . 从海水中可以获得淡水、食盐,并可提取镁和溴等物质。
(1)从海水中提取镁的流程如图所示:
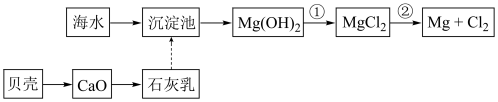
反应①的离子方程式为__ ;
反应②的化学方程式为__ ;
(2)海水提取溴流程:
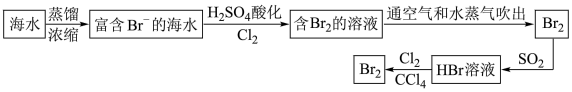
①该流程中涉及发生反应的离子方程式:__ ; ___ ;
②该流程中溴元素被氧化又被还原又被氧化的目的是:___ ;
③从最终溴的四氯化碳溶液中得到液溴,应采取的操作是__ 。
(1)从海水中提取镁的流程如图所示:

反应①的离子方程式为
反应②的化学方程式为
(2)海水提取溴流程:
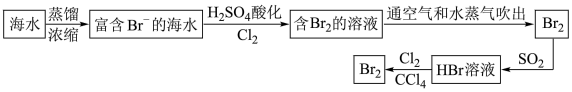
①该流程中涉及发生反应的离子方程式:
②该流程中溴元素被氧化又被还原又被氧化的目的是:
③从最终溴的四氯化碳溶液中得到液溴,应采取的操作是
您最近一年使用:0次
2019-12-12更新
|
286次组卷
|
2卷引用:吉林省延边朝鲜族自治州汪清县第四中学2019-2020学年高二上学期第一次阶段考试化学试题



