名校
解题方法
1 . 下列实验操作规范且能达到实验目的的是


| A.图甲装置可除去Cl2中含有的少量HCl |
| B.图乙装置可探究钠与Cl2反应 |
| C.图丙装置可制备Fe(OH)3胶体 |
| D.图丁装置可用于比较碳酸钠和碳酸氢钠的热稳定性 |
您最近一年使用:0次
2023-04-26更新
|
971次组卷
|
3卷引用: 山东省德州市第一中学2022-2023学年高一上学期1月份阶段性测试化学试题
山东省德州市第一中学2022-2023学年高一上学期1月份阶段性测试化学试题山东省东营市河口区第一高级中学2023-2024学年高一上学期10月月考(贯通班)化学试题(已下线)考点巩固卷03 金属及其化合物(4大考点48题)-2024年高考化学一轮复习考点通关卷(新高考通用)
名校
2 . 某化学兴趣小组以含钴废渣(主要成分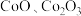 ,还含有
,还含有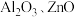 等杂质)为原料制备
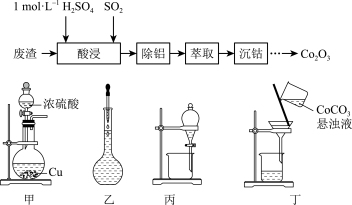
等杂质)为原料制备 的一种实验流程如下。下列与流程相关的原理、装置和操作能达到实验目的的是
的一种实验流程如下。下列与流程相关的原理、装置和操作能达到实验目的的是
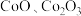 ,还含有
,还含有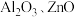 等杂质)为原料制备
等杂质)为原料制备 的一种实验流程如下。下列与流程相关的原理、装置和操作能达到实验目的的是
的一种实验流程如下。下列与流程相关的原理、装置和操作能达到实验目的的是
A.将 固体放入蒸发血中灼烧制 固体放入蒸发血中灼烧制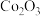 |
B.“酸浸”所需的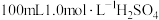 溶液用装置乙配制 溶液用装置乙配制 |
C.“萃取”的目的是除去 ,用装置丙,振荡时分液漏斗下口应倾斜向上 ,用装置丙,振荡时分液漏斗下口应倾斜向上 |
D.用装置甲制备“酸浸”所需的 ,“酸浸”时 ,“酸浸”时 为还原剂 为还原剂 |
您最近一年使用:0次
2023-12-18更新
|
304次组卷
|
3卷引用:江西省宜春市宜丰中学2023-2024学年高一上学期1月期末化学试题
名校
3 . 海水晒盐后精制得到 ;氯碱工业电解饱和
;氯碱工业电解饱和 溶液得到
溶液得到 和
和 ;向海水晒盐得到的卤水中通
;向海水晒盐得到的卤水中通 可制溴;从海水中还能提取镁;海洋中许多藻类植物具有富集碘的能力,从海带中可以提取碘。下列有关从海带中提取碘的实验原理和装置能达到实验目的的是
可制溴;从海水中还能提取镁;海洋中许多藻类植物具有富集碘的能力,从海带中可以提取碘。下列有关从海带中提取碘的实验原理和装置能达到实验目的的是

 ;氯碱工业电解饱和
;氯碱工业电解饱和 溶液得到
溶液得到 和
和 ;向海水晒盐得到的卤水中通
;向海水晒盐得到的卤水中通 可制溴;从海水中还能提取镁;海洋中许多藻类植物具有富集碘的能力,从海带中可以提取碘。下列有关从海带中提取碘的实验原理和装置能达到实验目的的是
可制溴;从海水中还能提取镁;海洋中许多藻类植物具有富集碘的能力,从海带中可以提取碘。下列有关从海带中提取碘的实验原理和装置能达到实验目的的是
| A.用装置甲灼烧碎海带 | B.用装置乙过滤海带灰的浸泡液 |
C.用装置丙制备用于氧化浸泡液中 的 的 | D.用装置丁吸收氧化浸泡液中 后的 后的 尾气 尾气 |
您最近一年使用:0次
2023-02-16更新
|
233次组卷
|
2卷引用:江苏省苏州市木渎高级中学2022-2023学年高一下学期期初调研化学试题
解题方法
4 . 亚铁盐由于具有较强的还原性,久置于空气中容易氧化变质,日常实验中常以复盐硫酸亚铁铵晶体 代替绿矾(
代替绿矾( )等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:
)等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:
(1)①在制备硫酸亚铁铵晶体时,为了防止被氧化,需除去溶解氧,所配制 溶液、
溶液、 溶液等都必须预先经过
溶液等都必须预先经过___________ (操作)处理后再使用。向 溶液中加入饱和
溶液中加入饱和 溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。
溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。
②在上述洗涤操作步骤中,下列蒸馏水最适合作为洗涤剂的是___________ (填字母)。
A.沸水 B.冰水 C.温水 D.常温
(2)取少量制得晶体按下图进行实验,
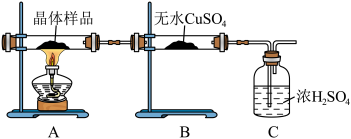
①若B装置中无水 变蓝证明含有结晶水,C装置的作用是
变蓝证明含有结晶水,C装置的作用是___________ 。
②另取少量晶体于试管中,加水溶解,___________ (填操作与现象),证明晶体中有 ,用相关的离子方程式说明产生该现象的原理:
,用相关的离子方程式说明产生该现象的原理:___________ 。
 代替绿矾(
代替绿矾( )等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:
)等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:| 溶剂 | 蒸馏水 | ||||
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 9.8 | 22.0 | 28.2 | 35.7 | 45.2 |
(1)①在制备硫酸亚铁铵晶体时,为了防止被氧化,需除去溶解氧,所配制
 溶液、
溶液、 溶液等都必须预先经过
溶液等都必须预先经过 溶液中加入饱和
溶液中加入饱和 溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。
溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。②在上述洗涤操作步骤中,下列蒸馏水最适合作为洗涤剂的是
A.沸水 B.冰水 C.温水 D.常温
(2)取少量制得晶体按下图进行实验,

①若B装置中无水
 变蓝证明含有结晶水,C装置的作用是
变蓝证明含有结晶水,C装置的作用是②另取少量晶体于试管中,加水溶解,
 ,用相关的离子方程式说明产生该现象的原理:
,用相关的离子方程式说明产生该现象的原理:
您最近一年使用:0次
5 . Ⅰ.二氧化氯(ClO2)是一种高效消毒剂,易溶于水,沸点为11.0℃,极易爆炸。在干燥空气稀释条件下,用干燥的氯气与固体亚氯酸钠制备二氧化氯,装置如图:
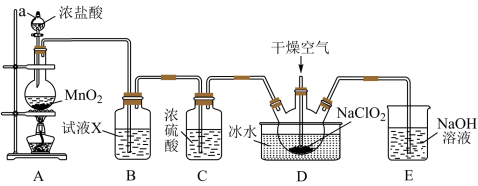
(1)装置A中反应的化学方程式为___________ 。
(2)试剂X是___________ 。
(3)装置D中冰水的主要作用是_______ ,装置D内发生反应的化学方程式为________ 。
(4)工业上对氯气的需求量很大。常利用电解饱和食盐水的方法来制取氯气,该反应的化学方程式为___________ 。
(5)工业上,用双氧水与NaClO3在稀硫酸酸化下反应制备ClO2,则反应的化学方程式为___________ 。
(6)已知NaClO2饱和溶液在不同温度时析出的晶体情况如表。
利用NaClO2溶液制得NaClO2晶体的操作步骤:_______ 、38~60℃的温水洗涤、低于60℃干燥。
Ⅱ.某同学研究84消毒液的漂白性,实验如下。
资料:84消毒液中含氯微粒主要有ClO-、Cl-、HClO:相同浓度时,HClO的氧化性强于ClO-;ORP是反映水溶液中所有物质表现出来的氧化-还原性,ORP值越大,氧化性越强。
①向2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
②向2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
③测得84消毒液在不同温度时ORP随时间的变化曲线如下。
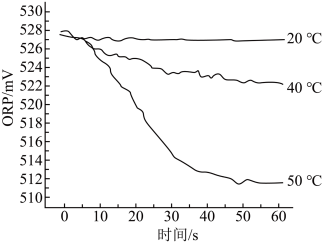
(7)①已知白醋显酸性,不具有漂白性。实验①②现象不同的原因是___________ 。
②实验表明,向84消毒液中加入较多稀盐酸时会产生氯气,生成氯气的方程式是___________ 。
③由实验③可得不同温度下ORP值不同的原因可能是___________ 。
(8)针对不同物品的消毒,84消毒液需要稀释到不同的浓度来使用。取含次氯酸钠14.9g/L的84消毒液1mL,加水稀释至100mL,则稀释后的溶液中次氯酸钠的物质的量浓度为___________ mol/L。

(1)装置A中反应的化学方程式为
(2)试剂X是
(3)装置D中冰水的主要作用是
(4)工业上对氯气的需求量很大。常利用电解饱和食盐水的方法来制取氯气,该反应的化学方程式为
(5)工业上,用双氧水与NaClO3在稀硫酸酸化下反应制备ClO2,则反应的化学方程式为
(6)已知NaClO2饱和溶液在不同温度时析出的晶体情况如表。
| 温度 | <38℃ | 38℃~60℃ | >60℃ |
| 析出晶体 | NaClO2·3H2O | NaClO2 | 分解成NaClO3和NaCl |
Ⅱ.某同学研究84消毒液的漂白性,实验如下。
资料:84消毒液中含氯微粒主要有ClO-、Cl-、HClO:相同浓度时,HClO的氧化性强于ClO-;ORP是反映水溶液中所有物质表现出来的氧化-还原性,ORP值越大,氧化性越强。
①向2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
②向2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
③测得84消毒液在不同温度时ORP随时间的变化曲线如下。

(7)①已知白醋显酸性,不具有漂白性。实验①②现象不同的原因是
②实验表明,向84消毒液中加入较多稀盐酸时会产生氯气,生成氯气的方程式是
③由实验③可得不同温度下ORP值不同的原因可能是
(8)针对不同物品的消毒,84消毒液需要稀释到不同的浓度来使用。取含次氯酸钠14.9g/L的84消毒液1mL,加水稀释至100mL,则稀释后的溶液中次氯酸钠的物质的量浓度为
您最近一年使用:0次
名校
6 . 铁及其化合物,有着不同的重要用途。请完成下面的问题:
Ⅰ.某化学兴趣小组以菱铁矿(主要成分为FeCO3,含有SiO2、Al2O3等少量杂质)为原料制备氯化铁晶体(FeCl3·6H2O)的实验过程如下:

已知:①SiO2不溶于酸和水; ②Al3++4OH-= AlO +2H2O。
+2H2O。
(1)写出酸溶时发生反应的离子方程式___________ 、Al2O3+6H+=2Al3++3H2O。
(2)操作Ⅰ名称是___________ 。
(3)在氧化过程中,发生反应的离子方程式为___________ 。如何检验铁元素全部以Fe3+形式存在:___________ 。
(4)加入过量NaOH溶液的目的是___________ 。
(5)请补充完整由过滤后得到的固体制备FeCl3·6H2O的实验方案:向过滤后所得固体加___________ 使固体完全溶解,然后___________ ,过滤,用水洗涤固体2-3次,低温干燥,得到FeCl3·6H2O。
Ⅱ.碳酸亚铁(FeCO3)是白色固体,难溶于水,是生产补血剂的重要原料。下图装置利用FeCl2溶液制取FeCO3:
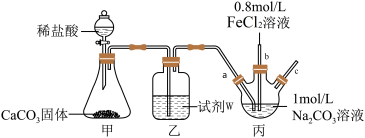
装置丙中操作步骤与现象:①将导管a移出液面,通入一段时间气体,②将导管a插入液面以下,向Na2CO3溶液(碱性)通入一段时间CO2至其呈中性,③通过导管b向丙中滴加一定量FeCl2溶液产生白色沉淀和无色气体,④取丙中混合物,过滤、洗涤、干燥,得到FeCO3固体。
请回答:
(6)试剂w是___________ 。向Na2CO3溶液通入CO2的目的是___________ 。丙装置中制取FeCO3的离子方程式为___________ 。
(7)100mL 0.8mol/L FeCl2 溶液完全反应,最终得到5克FeCO3固体,则产率为___________ (结果保留2位小数)。
Ⅰ.某化学兴趣小组以菱铁矿(主要成分为FeCO3,含有SiO2、Al2O3等少量杂质)为原料制备氯化铁晶体(FeCl3·6H2O)的实验过程如下:

已知:①SiO2不溶于酸和水; ②Al3++4OH-= AlO
 +2H2O。
+2H2O。(1)写出酸溶时发生反应的离子方程式
(2)操作Ⅰ名称是
(3)在氧化过程中,发生反应的离子方程式为
(4)加入过量NaOH溶液的目的是
(5)请补充完整由过滤后得到的固体制备FeCl3·6H2O的实验方案:向过滤后所得固体加
Ⅱ.碳酸亚铁(FeCO3)是白色固体,难溶于水,是生产补血剂的重要原料。下图装置利用FeCl2溶液制取FeCO3:

装置丙中操作步骤与现象:①将导管a移出液面,通入一段时间气体,②将导管a插入液面以下,向Na2CO3溶液(碱性)通入一段时间CO2至其呈中性,③通过导管b向丙中滴加一定量FeCl2溶液产生白色沉淀和无色气体,④取丙中混合物,过滤、洗涤、干燥,得到FeCO3固体。
请回答:
(6)试剂w是
(7)100mL 0.8mol/L FeCl2 溶液完全反应,最终得到5克FeCO3固体,则产率为
您最近一年使用:0次
名校
解题方法
7 . 将少量饱和 溶液分别滴加到下列物质中,得到三种不同的分散系,回答下列问题。
溶液分别滴加到下列物质中,得到三种不同的分散系,回答下列问题。
甲:将饱和 溶液滴加到冷水中。
溶液滴加到冷水中。
乙:将饱和 溶液滴加到NaOH溶液中。
溶液滴加到NaOH溶液中。
丙:将饱和 溶液滴加到沸水中。
溶液滴加到沸水中。
(1)甲属于_______ (填“溶液”或“胶体”或“浊液”),其颜色是_______ 。
(2)乙中分散质粒子直径范围是_______ 。
(3)将乙分散系过滤,向滤渣中加入盐酸,反应的离子方程式为_______ 。
(4)将丙继续加热煮沸得到红褐色透明液体,反应的离子方程式为_______ 。可以用简单的方法判断丙中是否成功制备胶体,该方法是_______ 。
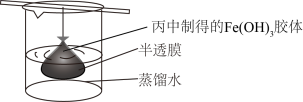
(5)可用如图所示的装置除去 胶体中的杂质离子来提纯
胶体中的杂质离子来提纯 胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入
胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入 溶液,若
溶液,若_______ (填实验现象),则说明该 胶体中的杂质离子已经完全除去。
胶体中的杂质离子已经完全除去。
 溶液分别滴加到下列物质中,得到三种不同的分散系,回答下列问题。
溶液分别滴加到下列物质中,得到三种不同的分散系,回答下列问题。甲:将饱和
 溶液滴加到冷水中。
溶液滴加到冷水中。乙:将饱和
 溶液滴加到NaOH溶液中。
溶液滴加到NaOH溶液中。丙:将饱和
 溶液滴加到沸水中。
溶液滴加到沸水中。(1)甲属于
(2)乙中分散质粒子直径范围是
(3)将乙分散系过滤,向滤渣中加入盐酸,反应的离子方程式为
(4)将丙继续加热煮沸得到红褐色透明液体,反应的离子方程式为
(5)可用如图所示的装置除去
 胶体中的杂质离子来提纯
胶体中的杂质离子来提纯 胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入
胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入 溶液,若
溶液,若 胶体中的杂质离子已经完全除去。
胶体中的杂质离子已经完全除去。
您最近一年使用:0次
名校
8 . 二氧化氯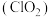 是一种新型的消毒杀剂,常用于饮用水的消毒,其消市效果优于传统的液氯消毒,除此之外,二氧化氯还具有漂白性,常用干纸浆和纸、纤维、小麦面粉、淀粉的漂白。常温常压下
是一种新型的消毒杀剂,常用于饮用水的消毒,其消市效果优于传统的液氯消毒,除此之外,二氧化氯还具有漂白性,常用干纸浆和纸、纤维、小麦面粉、淀粉的漂白。常温常压下 是一种带有辛辣气味的黄绿色气体,易溶于水和四氯化碳。工业上常用综合法制备
是一种带有辛辣气味的黄绿色气体,易溶于水和四氯化碳。工业上常用综合法制备 ,其工序包括制备氯酸钠,盐酸合成和
,其工序包括制备氯酸钠,盐酸合成和 制取,主要工艺流程如图所示。
制取,主要工艺流程如图所示。
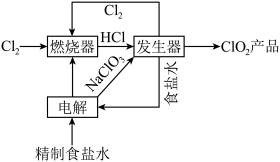
回答下列问题:
(1)工艺流程图涉及到的物质化学式或物质名称,其中能导电的是___________ ,属于电解质的是___________ 。
(2)实验室模拟“燃烧器”中发生的反应,观察到的现象有___________ 。
(3)“发生器”中发生反应的离子方程式为___________ ,若整个过程制得 ,则理论上分别向装置中补充
,则理论上分别向装置中补充___________ (填质量和物质名称)恢复至起始状态。
(4)粗盐中常常含有泥沙、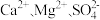 等杂质,粗盐提纯的步骤中加入稍过量的
等杂质,粗盐提纯的步骤中加入稍过量的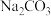 的目的是
的目的是___________ ,经一系列操作可得制食盐水,电解精制食盐水制得 同时还会获取轻质燃料氢气,则离子方程式为
同时还会获取轻质燃料氢气,则离子方程式为___________ 。
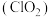 是一种新型的消毒杀剂,常用于饮用水的消毒,其消市效果优于传统的液氯消毒,除此之外,二氧化氯还具有漂白性,常用干纸浆和纸、纤维、小麦面粉、淀粉的漂白。常温常压下
是一种新型的消毒杀剂,常用于饮用水的消毒,其消市效果优于传统的液氯消毒,除此之外,二氧化氯还具有漂白性,常用干纸浆和纸、纤维、小麦面粉、淀粉的漂白。常温常压下 是一种带有辛辣气味的黄绿色气体,易溶于水和四氯化碳。工业上常用综合法制备
是一种带有辛辣气味的黄绿色气体,易溶于水和四氯化碳。工业上常用综合法制备 ,其工序包括制备氯酸钠,盐酸合成和
,其工序包括制备氯酸钠,盐酸合成和 制取,主要工艺流程如图所示。
制取,主要工艺流程如图所示。
回答下列问题:
(1)工艺流程图涉及到的物质化学式或物质名称,其中能导电的是
(2)实验室模拟“燃烧器”中发生的反应,观察到的现象有
(3)“发生器”中发生反应的离子方程式为
 ,则理论上分别向装置中补充
,则理论上分别向装置中补充(4)粗盐中常常含有泥沙、
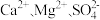 等杂质,粗盐提纯的步骤中加入稍过量的
等杂质,粗盐提纯的步骤中加入稍过量的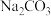 的目的是
的目的是 同时还会获取轻质燃料氢气,则离子方程式为
同时还会获取轻质燃料氢气,则离子方程式为
您最近一年使用:0次
名校
9 . FeCl3是实验室常见的药品,将少量FeCl3饱和溶液分别滴加到下列物质中,可得到三种分散系。

回答下列问题:
(1)可判断丙中成功制备胶体的是_________
(2)关于分散系的下列说法中,正确的是_________
(3)用括号中注明的方法分离下列各组混合物,其中正确的是_________
(4)丙中溶液液体呈透明的红褐色,发生反应的化学方程式为___________ 。
(5)现有另一胶体丁,向丁中插入电极通电,胶体粒子移向电源正极相连的一极,说明该胶体粒子带___________ 电荷;将丁与丙混合,可观察到___________ 现象。
(6)用如图所示的装置来提纯丙中制得的胶体,实验过程中需不断更换烧杯中的蒸馏水。证明胶体中杂质离子已经完全除去的方法是___________ 。

(7)四氯化碳也是一种重要的含氯化合物,其沸点约为76℃。碘单质沸点为184℃。若要从含碘的四氯化碳中提取碘和回收四氯化碳,还需要经过蒸馏,装置如图(加热和夹持装置已略去)。冷凝水应从___________ (填a或b)口通入,该装置使用水浴加热的优点是___________ ,最后晶态碘在___________ 里聚集(填仪器名称)。


回答下列问题:
(1)可判断丙中成功制备胶体的是_________
| A.布朗运动 | B.丁达尔现象 |
| C.形成分散系 | D.形成澄清透明的液体 |
(2)关于分散系的下列说法中,正确的是_________
| A.分散系一定是混合物 | B.分散剂一定是液体 |
| C.一种分散系里只能有一种分散质 | D.胆矾、空气、有色玻璃都是分散系 |
(3)用括号中注明的方法分离下列各组混合物,其中正确的是_________
| A.溴的四氯化碳溶液(分液) |
| B.淀粉和水(过滤) |
| C.KCl和MnO2(溶解过滤,再蒸发结晶) |
| D.碘和蒸馏水(萃取) |
(4)丙中溶液液体呈透明的红褐色,发生反应的化学方程式为
(5)现有另一胶体丁,向丁中插入电极通电,胶体粒子移向电源正极相连的一极,说明该胶体粒子带
(6)用如图所示的装置来提纯丙中制得的胶体,实验过程中需不断更换烧杯中的蒸馏水。证明胶体中杂质离子已经完全除去的方法是

(7)四氯化碳也是一种重要的含氯化合物,其沸点约为76℃。碘单质沸点为184℃。若要从含碘的四氯化碳中提取碘和回收四氯化碳,还需要经过蒸馏,装置如图(加热和夹持装置已略去)。冷凝水应从

您最近一年使用:0次
10 . 某探究学习小组在实验室中模拟并改进侯氏制碱法制备 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如下图:
,实验流程如下图:

回答下列问题:
(1)实验室中用下图所示装置制备 ,正确的连接顺序是
,正确的连接顺序是___________ (按气流方向,用小写字母表示),装置C的作用是___________ 。
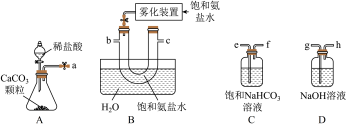
(2)B中使用雾化装置的优点是___________ 。
(3)生成 总反应的化学方程式为
总反应的化学方程式为___________ 。
(4)检验“母液”中大量存在的阳离子的实验方法是___________ (说明实验操作及现象)。
 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如下图:
,实验流程如下图:
回答下列问题:
(1)实验室中用下图所示装置制备
 ,正确的连接顺序是
,正确的连接顺序是
(2)B中使用雾化装置的优点是
(3)生成
 总反应的化学方程式为
总反应的化学方程式为(4)检验“母液”中大量存在的阳离子的实验方法是
您最近一年使用:0次



