1 . 化学小组同学在课外读物中看到:“通常 CO2可作灭火剂,但有些物质(如 Na) 着火,不能用 CO2熄灭。”他们决定探究 CO2与Na 反应的产物。
【提出猜想】CO2与Na 反应可能生成 4 种物质:C、CO、Na2O 和Na2CO3。
【查阅资料】
① Na 是非常活泼的金属,常温下与 O2、H2O 等物质反应。
②向氯化钯(PdCl2)溶液中通入 CO,产生黑色沉淀。
③Na2CO3是白色固体,易溶于水,能与 CaCl2溶液发生反应,化学方程式为:Na2CO3+CaCl2 =CaCO3↓+2NaCl
④Na2O 是白色固体,与H2O 反应生成NaOH。
⑤CaCl2、NaCl、Na2CO3、NaOH 四种溶液分别与无色酚酞溶液作用比较:
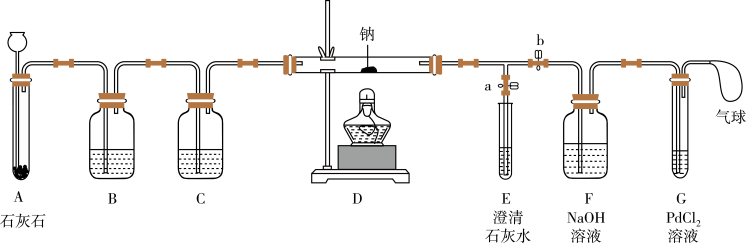
【实验过程】同学们在老师的指导下设计了如图所示装置(部分夹持仪器已略去)。
(1)实验记录
(2)实验反思
① 实验记录②中,E 中出现浑浊再点燃酒精灯的目的是______ 。
② 装置 B、C 的作用是_______ 。
③ 检验第 4 种物质是否存在的实验方案:取 D 中白色固体于试管中,_____ 。
【提出猜想】CO2与Na 反应可能生成 4 种物质:C、CO、Na2O 和Na2CO3。
【查阅资料】
① Na 是非常活泼的金属,常温下与 O2、H2O 等物质反应。
②向氯化钯(PdCl2)溶液中通入 CO,产生黑色沉淀。
③Na2CO3是白色固体,易溶于水,能与 CaCl2溶液发生反应,化学方程式为:Na2CO3+CaCl2 =CaCO3↓+2NaCl
④Na2O 是白色固体,与H2O 反应生成NaOH。
⑤CaCl2、NaCl、Na2CO3、NaOH 四种溶液分别与无色酚酞溶液作用比较:
| 分别向右侧溶液中加入无色酚酞溶液 | CaCl2 | NaCl | Na2CO3 | NaOH |
| 主要实验现象 | 无色 | 无色 | 由无色变为红色 | 由无色变为红色 |
【实验过程】同学们在老师的指导下设计了如图所示装置(部分夹持仪器已略去)。

(1)实验记录
| 序号 | 实验操作 | 主要实验现象 | 实验结论及解释 |
| ① | 打开 a,关闭 b,由长颈漏斗注入稀盐酸 | A 中产生大量气泡 E 中出现浑浊 | E 中反应的化学方程式为 |
| ② | 当 E 中出现浑浊时,打开b, 关闭 a,点燃酒精灯 | D 中 Na 剧烈燃烧,产生白烟,内壁附着黑色、白色固体,G 中产生黑色沉淀 | 反应产物一定有 |
| ③ | 取D 中白色固体于试管中,加水溶解,再加入几滴CaCl2 溶液 | 产生白色沉淀 | 反应产物还有 |
(2)实验反思
① 实验记录②中,E 中出现浑浊再点燃酒精灯的目的是
② 装置 B、C 的作用是
③ 检验第 4 种物质是否存在的实验方案:取 D 中白色固体于试管中,
您最近一年使用:0次
2 . 某学习小组在通过反应Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O研究反应速率的影响因素后,对Na2S2O3产生了兴趣,查资料知Na2S2O3的名称为硫代硫酸钠,可视为一个S原子取代了Na2SO4中的一个O原子。该实验小组运用类比学习的思想预测了Na2S2O3的某些性质,并通过实验探究了自己的预测。
【提出假设】
(1)部分学生认为Na2S2O3与Na2SO4结构相似,化学性质也相似,因此推测室温时Na2S2O3溶液的pH____ 7(填“>”、“=”或“<”)。
(2)部分学生从S元素化合价推测Na2S2O3与Na2SO3性质相似,推测具有较强的______________ 。
【实验探究】取适量Na2S2O3晶体,溶于水中制成Na2S2O3溶液,进行如下探究(填写表中空格)。
【实验结论】
(5)从探究①、②的结论:_________________________________________________________ 。
【问题讨论】
(6)甲同学向“探究②”反应后的溶液中滴加AgNO3溶液,观察到有白色沉淀产生,并据此认为氯水可将Na2S2O3氧化。你认为该方案是否正确并说明理由______________________________ 。
(7)请你重新设计一个实验方案,证明Na2S2O3被氯水氧化,你的方案是______________________________ 。
【提出假设】
(1)部分学生认为Na2S2O3与Na2SO4结构相似,化学性质也相似,因此推测室温时Na2S2O3溶液的pH
(2)部分学生从S元素化合价推测Na2S2O3与Na2SO3性质相似,推测具有较强的
【实验探究】取适量Na2S2O3晶体,溶于水中制成Na2S2O3溶液,进行如下探究(填写表中空格)。
| 实验操作 | 实验现象 | 现象解释(用离子方程式表示) | |
| 探究① | 用玻璃棒蘸取Na2S2O3溶液点在pH试纸中部,将试纸颜色与标准比色卡对照 | 溶液pH=8 | (3) |
| 探究② | 向新制氯水(pH<2)中滴加少量Na2S2O3溶液 | 氯水颜色变浅 | (4) |
(5)从探究①、②的结论:
【问题讨论】
(6)甲同学向“探究②”反应后的溶液中滴加AgNO3溶液,观察到有白色沉淀产生,并据此认为氯水可将Na2S2O3氧化。你认为该方案是否正确并说明理由
(7)请你重新设计一个实验方案,证明Na2S2O3被氯水氧化,你的方案是
您最近一年使用:0次
3 . Ⅰ:某学习小组为了探究硝酸铁的热稳定性,设计如下实验:
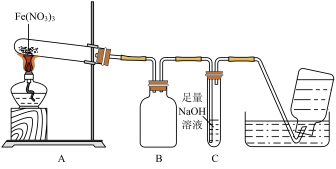
利用如图所示装置进行实验。加热A中Fe(NO3)3固体,装置B中均能看到红棕色气体,装置A中试管内剩余红棕色粉末状固体。
(1)装置B的作用是______ ;
(2)甲同学认为装置A中试管内剩余的红棕色粉末固体为Fe2O3。乙同学为了验证甲的观点,设计了下列实验
①取该固体少量于洁净试管内加入盐酸,固体溶解成棕黄色溶液,该反应的离子方程式为:______ 。
②向该棕黄色溶液中滴入__________ (填化学式)溶液,溶液变为血红色。
(3)经过检验发现C装置中生成了NaNO3和NaNO2。请写出生成这两种盐的化学反应方程式______ ,最后用排水法收集到少量无色气体,关于该无色气体,下列说法正确的是_______ (选填编号)
A.该气体是NO B.主要是O2,还有少量N2 C.NO和O2
(4)通过以上实验,写出Fe(NO3)3受热分解的化学反应方程式____________________ 。
Ⅱ:CH4燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由CH4、空气(氧气)、KOH(电解质溶液)构成。其中负极的电极方程式为:______ 。则电池放电时通入空气的电极为______ (填“正极”或“负极”);电解质溶液的pH______ (填“变大”或“变小”);每转移0.8mol电子消耗______ gCH4。

利用如图所示装置进行实验。加热A中Fe(NO3)3固体,装置B中均能看到红棕色气体,装置A中试管内剩余红棕色粉末状固体。
(1)装置B的作用是
(2)甲同学认为装置A中试管内剩余的红棕色粉末固体为Fe2O3。乙同学为了验证甲的观点,设计了下列实验
①取该固体少量于洁净试管内加入盐酸,固体溶解成棕黄色溶液,该反应的离子方程式为:
②向该棕黄色溶液中滴入
(3)经过检验发现C装置中生成了NaNO3和NaNO2。请写出生成这两种盐的化学反应方程式
A.该气体是NO B.主要是O2,还有少量N2 C.NO和O2
(4)通过以上实验,写出Fe(NO3)3受热分解的化学反应方程式
Ⅱ:CH4燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由CH4、空气(氧气)、KOH(电解质溶液)构成。其中负极的电极方程式为:
您最近一年使用:0次
名校
4 . 卤素单质在碱性溶液中容易发生歧化反应,歧化的产物依反应温度的不同而不同。
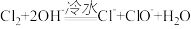 、
、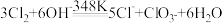
下图为制取氯气、氯酸钾、次氯酸钠和检验氯气性质的微型实验装置:
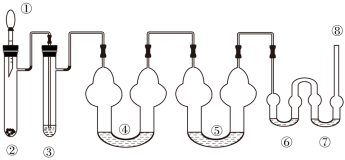
装置中盛装的药品如下:
①胶头滴管中装有 5 mL 浓盐酸;②微型具支试管中装有 1.5 g KMnO4;③微型具支试管中装有 2~3 mL 浓硫酸;④U 形反应管中装有 30% KOH 溶液;⑤U 形反应管中装有 2 mol·L-1 NaOH 溶液;⑥、⑦双 U 形反应管中分别装有 0.1 mol·L-1 KI-淀粉溶液和 KBr 溶液;⑧尾气出口用浸有 0.5 mol·L-1 Na2S2O3 溶液的棉花轻轻覆盖住
(1)检查整套装置气密性的方法是_________ 。
(2)为了使装置④⑤中的反应顺利完成,应该控制的反应条件分别为_______ 、_______ 。
(3)装置⑥⑦中能够观察到的实验现象分别是_________ , _______ 。
(4)如果把装置⑥⑦中的试剂互换位置,则______ (填“能”或“不能”)证明氧化性 Cl2>I2,理由是________ 。
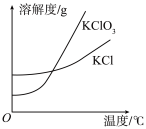
(5)已知氯酸钾和氯化钾的溶解度曲线如图所示,反应结束后,从装置④所得溶液中提取氯酸钾晶体的实验操作是________ 。
(6)尾气处理时 Cl2 发生反应的离子方程式为_________ 。
(7)选择微型实验装置的优点有____________ (任答两点)。
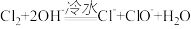 、
、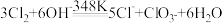
下图为制取氯气、氯酸钾、次氯酸钠和检验氯气性质的微型实验装置:

装置中盛装的药品如下:
①胶头滴管中装有 5 mL 浓盐酸;②微型具支试管中装有 1.5 g KMnO4;③微型具支试管中装有 2~3 mL 浓硫酸;④U 形反应管中装有 30% KOH 溶液;⑤U 形反应管中装有 2 mol·L-1 NaOH 溶液;⑥、⑦双 U 形反应管中分别装有 0.1 mol·L-1 KI-淀粉溶液和 KBr 溶液;⑧尾气出口用浸有 0.5 mol·L-1 Na2S2O3 溶液的棉花轻轻覆盖住
(1)检查整套装置气密性的方法是
(2)为了使装置④⑤中的反应顺利完成,应该控制的反应条件分别为
(3)装置⑥⑦中能够观察到的实验现象分别是
(4)如果把装置⑥⑦中的试剂互换位置,则
(5)已知氯酸钾和氯化钾的溶解度曲线如图所示,反应结束后,从装置④所得溶液中提取氯酸钾晶体的实验操作是

(6)尾气处理时 Cl2 发生反应的离子方程式为
(7)选择微型实验装置的优点有
您最近一年使用:0次
2020-05-03更新
|
328次组卷
|
3卷引用:四川省绵阳东辰国际学校2020届高三下期第二次月考理科综合化学试题
四川省绵阳东辰国际学校2020届高三下期第二次月考理科综合化学试题安徽省宿州市2020年高三年级理综模拟卷(五)化学试题(已下线)专题02 卤素元素拓展之实验大题-【微专题·大素养】备战2022年高考化学核心突破(元素拓展综合题)
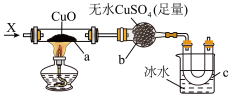
5 . 按照下图装置持续通入气体 ,可以看到
,可以看到 处有红色物质生成,
处有红色物质生成, 处变蓝,
处变蓝, 处得到液体,则
处得到液体,则 可能是(假设每个反应均完全)( )。
可能是(假设每个反应均完全)( )。
 ,可以看到
,可以看到 处有红色物质生成,
处有红色物质生成, 处变蓝,
处变蓝, 处得到液体,则
处得到液体,则 可能是(假设每个反应均完全)( )。
可能是(假设每个反应均完全)( )。
A. | B. 或 或 | C. | D. |
您最近一年使用:0次
2020-04-10更新
|
459次组卷
|
9卷引用:四川省绵阳市第一中学2021届高三开学考试化学试题
四川省绵阳市第一中学2021届高三开学考试化学试题(已下线)2014年甘肃省天水一中第二学期第二学段段中考试化学(理科)试卷(已下线)2019年5月1日 《每日一题》必修2-乙醇的氧化反应7.3.1 乙醇——2020年春高一新人教版第二册化学一课一练第三节 生活中两种常见的有机物 易错疑难集训(二)——A学习区 夯实基础(人教版必修2)2020年春高一化学新人教版第二册课后同步:7.3.1 乙醇必修第二册RJ第7章易错疑难集训(二)(苏教版2019)必修第二册专题8 有机化合物的获得与应用 易错疑难集训(二)云南省普洱市镇沅彝族哈尼族拉祜族自治县第一中学2021-2022学年高一下学期4月份考试化学试题
13-14高一上·广东深圳·期末
名校
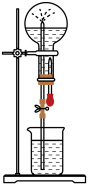
6 . 如图是化学教材中常用的喷泉实验装置(夹持仪器已略去),在烧瓶中充满干燥气体,而胶头滴管及烧杯中分别盛有液体。下列气体和液体的组合中不可能形成喷泉的是( )

| A.氯化氢和水 |
| B.氧气和水 |
| C.氨气和水 |
| D.二氧化碳和氢氧化钠溶液 |
您最近一年使用:0次
2020-02-15更新
|
338次组卷
|
17卷引用:四川省三台中学实验学校2020-2021学年高一3月月考化学试题
四川省三台中学实验学校2020-2021学年高一3月月考化学试题(已下线)2012-2013学年广东省深圳科学高中高一第一学期期末考试化学试卷A(已下线)4.4.1 氨高中化学人教版 必修1 第四章 非金属及其化合物 4.氨 硫酸 硝酸 氨(已下线)【走进新高考】(人教版必修一)4.4.1氨、硝酸、硫酸——氨 同步练习02广东省汕头市金山中学2018-2019学年高一下学期第一次月考化学试题福建省三明第一中学2019-2020学年高一上学期第二次月考化学试题人教版高中化学必修1第四章《非金属及其化合物》测试卷2云南省永善县第二中学2019—2020学年高一上学期期末考试化学试题贵州省独山县第四中学2019-2020学年高一上学期期末考试化学试题(已下线)专题4.4 氮及其化合物(练)——2020年高考化学一轮复习讲练测辽宁省抚顺县高级中学2019-2020学年高一下学期期中网课学习质量检测化学试题山西省大同市浑源县第七中学2020-2021学年高一下学期第一次月考化学试题四川省南充市白塔中学2021-2022学年高一下学期3月月考化学试题黑龙江省伊春市伊美区第二中学2021-2022学年高一下学期期中考试(会考)化学试题海南省三亚华侨学校南新校区2021-2022学年高一下学期期中考试化学试题吉林省白城市第十四中学2022届高三上学期期中考试化学试题
7 . 某学习小组通过下列装置探究MnO2与FeCl3·6H2O能否反应产生Cl2,FeCl3的升华温度为315℃。
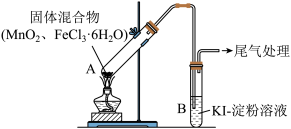
实验操作和现象:
(1)现象ⅰ中的白雾是___ 。
(2)分析现象ⅱ,该小组探究黄色气体的成分,实验如下:
a.加热FeCl3·6H2O,产生白雾和黄色气体。
b.用KSCN溶液检验现象ⅱ和a中的黄色气体,溶液均变红。通过该实验说明现象ⅱ中黄色气体含有___ 。
(3)除了氯气可使B中溶液变蓝外,推测还可能的原因是:
①实验b检出的气体使之变蓝,反应的离子方程式是___ 。经实验证实推测成立。
②溶液变蓝的另外一种原因是:在酸性条件下,装置中的空气使之变蓝。通过进一步实验确认了这种可能性,其实验方案是___ 。
(4)为进一步确认黄色气体是否含有Cl2,小组提出两种方案,均证实了Cl2的存在。
方案1:在A、B间增加盛有某种试剂的洗气瓶C。
方案2:将B中KI淀粉溶液替换为NaBr溶液;检验Fe2+。
现象如下:
①方案1的C中盛放的试剂是___ (填字母)。
A.NaCl饱和溶液 B.NaOH溶液 C.NaClO溶液
②方案2中检验Fe2+的原因是___ 。
③综合方案1、2的现象,说明选择NaBr溶液的依据是___ 。
(5)将A中的产物分离得到Fe2O3和MnCl2,A中产生Cl2的化学方程式是:___ 。

实验操作和现象:
| 操作 | 现象 |
| 点燃酒精灯,加热 | ⅰ.A中部分固体溶解,上方出现白雾 ⅱ.稍后,产生黄色气体,管壁附着黄色液滴 ⅲ.B中溶液变蓝 |
(2)分析现象ⅱ,该小组探究黄色气体的成分,实验如下:
a.加热FeCl3·6H2O,产生白雾和黄色气体。
b.用KSCN溶液检验现象ⅱ和a中的黄色气体,溶液均变红。通过该实验说明现象ⅱ中黄色气体含有
(3)除了氯气可使B中溶液变蓝外,推测还可能的原因是:
①实验b检出的气体使之变蓝,反应的离子方程式是
②溶液变蓝的另外一种原因是:在酸性条件下,装置中的空气使之变蓝。通过进一步实验确认了这种可能性,其实验方案是
(4)为进一步确认黄色气体是否含有Cl2,小组提出两种方案,均证实了Cl2的存在。
方案1:在A、B间增加盛有某种试剂的洗气瓶C。
方案2:将B中KI淀粉溶液替换为NaBr溶液;检验Fe2+。
现象如下:
| 方案1 | B中溶液变为蓝色 |
| 方案2 | B中溶液呈浅橙红色,未检出Fe2+ |
A.NaCl饱和溶液 B.NaOH溶液 C.NaClO溶液
②方案2中检验Fe2+的原因是
③综合方案1、2的现象,说明选择NaBr溶液的依据是
(5)将A中的产物分离得到Fe2O3和MnCl2,A中产生Cl2的化学方程式是:
您最近一年使用:0次
2020-02-02更新
|
153次组卷
|
3卷引用:四川省绵阳南山中学实验学校2020届高三下学期5月月考化学试题
名校
解题方法
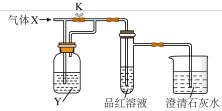
8 . 下图是一检验气体性质的实验装置。向装置中缓慢通入气体X,若关闭活塞K,则品红溶液无变化,而澄清石灰水变浑浊;若打开活塞K,则品红溶液褪色。据此判断气体X和洗气瓶内液体Y(足量)可能是( )

| 选项 | A | B | C | D |
| X | CO | SO2 | CO2 | Cl2 |
| Y | 浓H2SO4 | NaHCO3饱和溶液 | Na2SO3溶液 | NaHSO3饱和溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-01-10更新
|
309次组卷
|
3卷引用:四川绵阳南山中学2019-2020学年高一12月化学考试题
四川绵阳南山中学2019-2020学年高一12月化学考试题宁夏银川市第二中学2019-2020学年高一上学期期末考试化学试题(已下线)5.1.1 硫与二氧化硫(练好题)(能力提升)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)
9 . 实验室用浓盐酸和MnO2制Cl2,并以干燥的Cl2为原料进行实验,装置如下图所示。
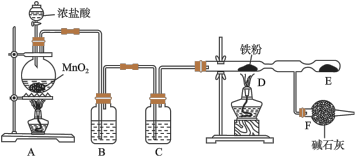
(1)写出A中反应的化学方程式:_______________________________________ 。
(2)装置B、C中应盛放的试剂名称分别为_____________ 、_____________ ;
(3)实验时,先点燃______________ 处的酒精灯, F装置所起的作用是:__________ (答两点)。
(4)用石灰乳吸收氯气可制得漂白粉,写出工业制漂白粉的化学方程式:______________ ,长期露置于空气中的漂白粉,加稀盐酸后产生的气体是______ (用字母代号填)。
A.O2 B.Cl2 C.CO2 D.HClO

(1)写出A中反应的化学方程式:
(2)装置B、C中应盛放的试剂名称分别为
(3)实验时,先点燃
(4)用石灰乳吸收氯气可制得漂白粉,写出工业制漂白粉的化学方程式:
A.O2 B.Cl2 C.CO2 D.HClO
您最近一年使用:0次
10 . Co(CH3COO)2(乙酸钴)可用作酯交换反应的催化剂并可用于制备高质量锂电池电极。在氮气氛围中,乙酸钴受热分解生成CO、CO2和C2H6等产物。某研究小组利用下列装置检验乙酸钴热分解的部分产物。
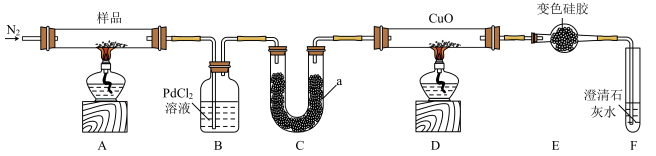
已知:①CO+PdCl2+H2O==CO2+Pd↓(黑色)+2HCl;
②变色硅胶为深蓝色,吸水后变为粉红色。
回答下列问题:
(1)B装置的作用是____ ,要检验乙酸钴分解产物中的CO2,对以上装置的改进方案是______ 。
(2)仪器a中的试剂是_______ ,其作用是_______ 。
(3)能证明乙酸钴的分解产物含有C2H6的实验现象是______ 。
(4)装置D中C2H6被CuO完全氧化的化学方程式是________ 。
(5)另取一定量乙酸钴结晶水合物样品[Co(CH3COO)2·nH2O]在空气中加热,样品的固体残留率(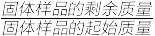 ×100%)随温度的变化如图所示(样品在200 ℃时已完全失去结晶水,350 ℃以上残留固体为金属氧化物)。根据以上实验数据列出残留氧化物CoxOy中x∶y的计算式:
×100%)随温度的变化如图所示(样品在200 ℃时已完全失去结晶水,350 ℃以上残留固体为金属氧化物)。根据以上实验数据列出残留氧化物CoxOy中x∶y的计算式:_____ 。

已知:①CO+PdCl2+H2O==CO2+Pd↓(黑色)+2HCl;
②变色硅胶为深蓝色,吸水后变为粉红色。
回答下列问题:
(1)B装置的作用是
(2)仪器a中的试剂是
(3)能证明乙酸钴的分解产物含有C2H6的实验现象是
(4)装置D中C2H6被CuO完全氧化的化学方程式是
(5)另取一定量乙酸钴结晶水合物样品[Co(CH3COO)2·nH2O]在空气中加热,样品的固体残留率(
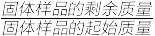 ×100%)随温度的变化如图所示(样品在200 ℃时已完全失去结晶水,350 ℃以上残留固体为金属氧化物)。根据以上实验数据列出残留氧化物CoxOy中x∶y的计算式:
×100%)随温度的变化如图所示(样品在200 ℃时已完全失去结晶水,350 ℃以上残留固体为金属氧化物)。根据以上实验数据列出残留氧化物CoxOy中x∶y的计算式: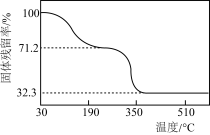
您最近一年使用:0次



