名校
解题方法
1 . 1810年,英国化学家戴维以大量事实为依据,确认一种黄绿色气体是一种新元素组成的单质——氯气。某化学兴趣小组同学利用以下装置制备干燥的氯气并对氯气的性质进行探究。
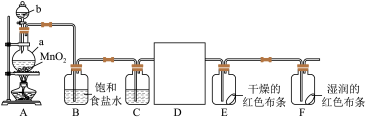
(1)仪器b的名称为___________ 。某同学认为该实验装置存在一处明显的不足,其改进措施为___________ 。
(2)仪器a中发生反应的化学方程式为___________ 。根据氯气的性质D中的收集装置可以选择___________ (填序号)。
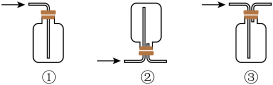
(3)下列有关该实验的说法中不正确 的是___________(填字母)。
(4)实验室还可用等物质的量的 与
与 的水溶液反应制取
的水溶液反应制取 ,同时生成
,同时生成 和NaCl,反应的化学方程式为
和NaCl,反应的化学方程式为___________ 。

(1)仪器b的名称为
(2)仪器a中发生反应的化学方程式为

(3)下列有关该实验的说法中
| A.将b中溶液换为稀盐酸,同样可以产生氯气 |
| B.C中试剂是浓硫酸,目的是干燥氯气 |
| C.F中红色布条褪色,证明氯气具有漂白性 |
| D.可用湿润的淀粉碘化钾试纸检验氯气是否收集满 |
(4)实验室还可用等物质的量的
 与
与 的水溶液反应制取
的水溶液反应制取 ,同时生成
,同时生成 和NaCl,反应的化学方程式为
和NaCl,反应的化学方程式为
您最近一年使用:0次
2023-11-22更新
|
211次组卷
|
2卷引用:浙江省温州市新力量联盟2023-2024学年高一上学期11月期中联考化学试题
名校
2 . 为探究物质的氧化性,某实验小组设计如图实验,在实验过程中,观察到氯化亚铁溶液变黄,四氯化碳溶液变为紫红色。下列说法错误的是(已知:碘单质易溶于四氯化碳,可得到紫红色溶液)


A.烧瓶中的反应为: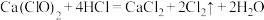 |
B.浸有 溶液的棉花起吸收尾气的作用 溶液的棉花起吸收尾气的作用 |
C. 可用淀粉溶液替换 可用淀粉溶液替换 |
D.试管下层出现紫红色,可证明氧化性: |
您最近一年使用:0次
2023-11-15更新
|
980次组卷
|
7卷引用:辽宁省鞍山市第一中学2023-2024学年高一上学期期中考试化学试题
3 . 完成下列问题。
(1)在氯碱工业中,常用电解饱和食盐水的方法制备氯气。其使用的电解饱和食盐水的装置原理如图所示。电解饱和食盐水的化学方程式为___________ 。电解时,铁电极上生成的气体为___________ 。
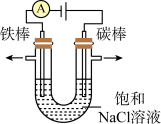
(2)天原化工厂是我国最早的民族氯碱化工企业之一、下列物质中,不是该厂产品的是______。
(3)氯碱工业的衍生产品——二氧化氯( )被世界卫生组织(WHO)列为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有着广泛应用。以下关于二氧化氯的说法正确的是______。
)被世界卫生组织(WHO)列为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有着广泛应用。以下关于二氧化氯的说法正确的是______。
(4)实验室用二氧化锰与浓盐酸在加热条件下制取氯气,写出该反应的化学方程式:___________ 。
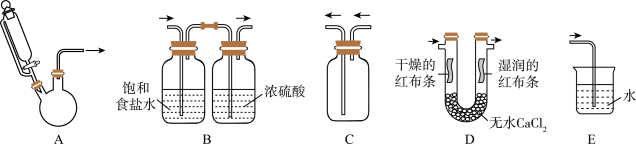
(5)实验室按照制备、净化、收集、性质检验及尾气处理的顺序进行实验。下列装置(“→”表示气流方向)能达到实验目的的是________ 。
(6)将氯气持续通入紫色石蕊试液中,溶液颜色呈如图变化:

关于溶液中导致变色的微粒Ⅰ、Ⅱ、Ⅲ的判断正确的是___________。
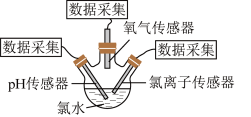
(7)验证氯水中HClO光照分解的产物。将新制的氯水加入三颈烧瓶内,将pH传感器、氯离子传感器、氧气传感器分别插入三颈瓶中(如图),用强光照射氯水,进行实验并采集数据,获得相关变化曲线。(溶液中, 越大,pH越小,溶液酸性越强)
越大,pH越小,溶液酸性越强)
若能够证明氯水中HClO在光照下发生了分解反应,则如图中纵坐标不能表示的物理量是______ 。
A.氧气的体积分数 B.氯离子的浓度 C.氯水的pH

(8)某化工厂用氯气与石灰乳生产漂白粉。产品出厂说明书如图:

①从物质类别看,漂白粉属于________ 。
②制备漂白粉的化学方程式是________ 。
③漂白粉需“避光保存于阴凉处”是因为漂白粉的有效成分与空气中的 、
、 反应生成不稳定的次氯酸而易失效。生成次氯酸的化学方程式为
反应生成不稳定的次氯酸而易失效。生成次氯酸的化学方程式为________ 。
④使用漂白粉时最好“随用随配”。某次使用时,取漂白粉2.54g溶解于1000g水中,所得溶液中次氯酸钙的物质的量浓度为________ 。(假设漂白粉中只含有次氯酸钙和氯化钙,不含其它杂质,且所得溶液的体积为1L)
(1)在氯碱工业中,常用电解饱和食盐水的方法制备氯气。其使用的电解饱和食盐水的装置原理如图所示。电解饱和食盐水的化学方程式为

(2)天原化工厂是我国最早的民族氯碱化工企业之一、下列物质中,不是该厂产品的是______。
| A.纯碱 | B.盐酸 | C.食盐 | D.漂白粉 |
(3)氯碱工业的衍生产品——二氧化氯(
 )被世界卫生组织(WHO)列为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有着广泛应用。以下关于二氧化氯的说法正确的是______。
)被世界卫生组织(WHO)列为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有着广泛应用。以下关于二氧化氯的说法正确的是______。| A.是强还原剂 | B.其中氯元素的化合价为+4价 |
| C.是强氧化剂 | D.相对分子质量为67.5g/mol |
(4)实验室用二氧化锰与浓盐酸在加热条件下制取氯气,写出该反应的化学方程式:
(5)实验室按照制备、净化、收集、性质检验及尾气处理的顺序进行实验。下列装置(“→”表示气流方向)能达到实验目的的是

(6)将氯气持续通入紫色石蕊试液中,溶液颜色呈如图变化:

关于溶液中导致变色的微粒Ⅰ、Ⅱ、Ⅲ的判断正确的是___________。
A. 、HClO、 、HClO、 | B. 、 、 、 、 |
C.HCl、 、 、 | D.HCl、HClO、 |
(7)验证氯水中HClO光照分解的产物。将新制的氯水加入三颈烧瓶内,将pH传感器、氯离子传感器、氧气传感器分别插入三颈瓶中(如图),用强光照射氯水,进行实验并采集数据,获得相关变化曲线。(溶液中,
 越大,pH越小,溶液酸性越强)
越大,pH越小,溶液酸性越强)
若能够证明氯水中HClO在光照下发生了分解反应,则如图中纵坐标不能表示的物理量是
A.氧气的体积分数 B.氯离子的浓度 C.氯水的pH

(8)某化工厂用氯气与石灰乳生产漂白粉。产品出厂说明书如图:

①从物质类别看,漂白粉属于
②制备漂白粉的化学方程式是
③漂白粉需“避光保存于阴凉处”是因为漂白粉的有效成分与空气中的
 、
、 反应生成不稳定的次氯酸而易失效。生成次氯酸的化学方程式为
反应生成不稳定的次氯酸而易失效。生成次氯酸的化学方程式为④使用漂白粉时最好“随用随配”。某次使用时,取漂白粉2.54g溶解于1000g水中,所得溶液中次氯酸钙的物质的量浓度为
您最近一年使用:0次
名校
解题方法
4 . 某实验小组为了证明过氧化钠可在呼吸面具和潜水艇中做供氧剂,设计了如图实验装置进行实验,则下列说法不正确的是
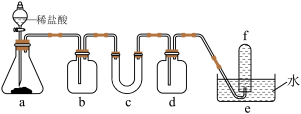
A.c中盛放的是 ,装置中会发生2个反应 ,装置中会发生2个反应 |
B.b中盛放的是浓硫酸,作用是干燥 |
| C.c中会观察到固体颜色逐渐变白,伴有发热的现象 |
D.d中盛放的是NaOH溶液,作用是吸收多余的 |
您最近一年使用:0次
2023-12-06更新
|
127次组卷
|
3卷引用:广东省东莞市东莞中学2023-2024学年高一上学期期中考试化学试卷
名校
解题方法
5 . 为检验某加碘食盐中是否含有 ,取相同食盐样品进行下表所示实验:
,取相同食盐样品进行下表所示实验:
已知:
下列说法中正确的是
 ,取相同食盐样品进行下表所示实验:
,取相同食盐样品进行下表所示实验:已知:

| 实验① | 实验② | 实验③ |
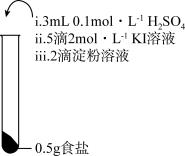 | 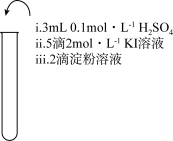 | 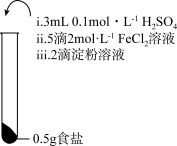 |
| 振荡,溶液迅速变为蓝色 | 振荡,一段时间后溶液变为浅蓝色 | 振荡,溶液变为浅黄色 |
A.仅由实验①就能证明食盐样品中存在 |
B.以上实验说明离子的还原性: |
C.实验③能证明食盐样品中不存在 |
D.实验②中发生反应的离子方程式为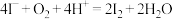 |
您最近一年使用:0次
2023-11-04更新
|
288次组卷
|
2卷引用:北京交通大学附属中学2023-2024学年高一上学期期中考试化学试题
解题方法
6 . 实验小组研究 与
与 的反应,装置、步骤和现象如下:
的反应,装置、步骤和现象如下:
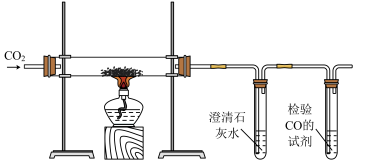
实验步骤和现象:
i.先向硬质玻璃管中加一定量钠,再迅速通入 至澄清石灰水浑浊,然后点燃酒精灯。
至澄清石灰水浑浊,然后点燃酒精灯。
ii.一段时间后,硬质玻璃管中有白色物质产生,管壁上有黑色物质出现。检验 的试剂未见明显变化。
的试剂未见明显变化。
iii.将硬质玻璃管中的固体溶于水,未见气泡产生;过滤,向滤液中加入过量 溶液,产生白色沉淀:再次过滤,滤液呈碱性;取白色沉淀加入盐酸,产生气体。
溶液,产生白色沉淀:再次过滤,滤液呈碱性;取白色沉淀加入盐酸,产生气体。
iv.将管壁上的黑色物质与浓硫酸混合加热,生成能使品红溶液褪色的气体。
下列说法不正确的是
 与
与 的反应,装置、步骤和现象如下:
的反应,装置、步骤和现象如下:
实验步骤和现象:
i.先向硬质玻璃管中加一定量钠,再迅速通入
 至澄清石灰水浑浊,然后点燃酒精灯。
至澄清石灰水浑浊,然后点燃酒精灯。ii.一段时间后,硬质玻璃管中有白色物质产生,管壁上有黑色物质出现。检验
 的试剂未见明显变化。
的试剂未见明显变化。iii.将硬质玻璃管中的固体溶于水,未见气泡产生;过滤,向滤液中加入过量
 溶液,产生白色沉淀:再次过滤,滤液呈碱性;取白色沉淀加入盐酸,产生气体。
溶液,产生白色沉淀:再次过滤,滤液呈碱性;取白色沉淀加入盐酸,产生气体。iv.将管壁上的黑色物质与浓硫酸混合加热,生成能使品红溶液褪色的气体。
下列说法不正确的是
A.实验证明 与 与 的反应的氧化产物为 的反应的氧化产物为 ,还原产物为C ,还原产物为C |
B.步骤iii证明 与 与 也可以发生类似于 也可以发生类似于 与 与 的反应 的反应 |
C.步骤iv发生反应的化学方程式为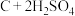 (浓) (浓)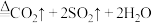 |
D.根据以上实验推测: 与金属K也可以发生反应并被还原 与金属K也可以发生反应并被还原 |
您最近一年使用:0次
7 . 为比较碳酸钠与碳酸氢钠的热稳定性,某兴趣小组设计了如下套管实验。
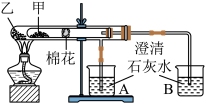
下列说法或做法中不科学的是

下列说法或做法中不科学的是
| A.甲为小苏打,乙为纯碱 |
| B.要证明碳酸氢钠受热能产生水,可在小试管内塞上沾有无水硫酸铜粉末的棉花球 |
| C.加热不久就能看到A烧杯中的澄清石灰水变浑浊 |
| D.实验过程中没有发现B烧杯中的澄清石灰水变浑浊 |
您最近一年使用:0次
解题方法
8 . T℃时,在体积为2L的密闭容器内,与同一个化学反应有关的A、B、C、D四种物质(D为固体,其余均为气体)的物质的量随反应时间变化的曲线如图所示,回答下列问题。
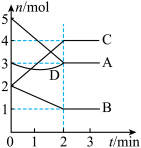
(1)该反应的化学方程式为_______ 。
(2)物质D在反应中的作用是______ 。
(3)若在上述反应中A是SO2、B是O2、C是SO3。下列说法能表示反应达到平衡状态的是______ (填字母);在0~2min内用O2表示的反应速率v(O2)=______ 。
A.容器内的气体压强保持不变 B.物质的量浓度:c(SO2)=2c(O2)
C.混合气的平均相对分子质量保持不变 D.化学反应速率:v(SO2)=v(SO3)
(4)某兴趣小组同学拟在实验室中制取SO2,并探究SO2使品红溶液褪色的原因。
①用Cu和浓硫酸反应制取SO2,化学反应方程式是_______ 。
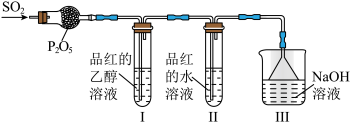
②兴趣小组同学利用如图装置探究SO2的漂白性,观察到I中品红溶液不褪色,II中品红溶液褪色。
查阅资料:SO2通入水中存在如下反应:SO2+xH2O SO2•xH2O
SO2•xH2O H++HSO
H++HSO +(x-1)H2O;HSO
+(x-1)H2O;HSO
 SO
SO +H+。
+H+。
通过分析上述现象,猜测使品红水溶液褪色的微粒可能是i.H2SO3;ii.______ ;iii.______ 。
③为了证明上述猜测ii和iii,进行表中实验1和2,记录现象。
该实验说明,两种粒子中,______ 使品红水溶液褪色程度更大。
④取实验1所得溶液直接加热接近沸腾,溶液不恢复红色,在热溶液中滴加稀硫酸则恢复红色;说明______ ;取实验2所得溶液直接加热,则慢慢恢复浅红色,说明NaHSO3与品红生成的物质不稳定。

(1)该反应的化学方程式为
(2)物质D在反应中的作用是
(3)若在上述反应中A是SO2、B是O2、C是SO3。下列说法能表示反应达到平衡状态的是
A.容器内的气体压强保持不变 B.物质的量浓度:c(SO2)=2c(O2)
C.混合气的平均相对分子质量保持不变 D.化学反应速率:v(SO2)=v(SO3)
(4)某兴趣小组同学拟在实验室中制取SO2,并探究SO2使品红溶液褪色的原因。
①用Cu和浓硫酸反应制取SO2,化学反应方程式是
②兴趣小组同学利用如图装置探究SO2的漂白性,观察到I中品红溶液不褪色,II中品红溶液褪色。

查阅资料:SO2通入水中存在如下反应:SO2+xH2O
 SO2•xH2O
SO2•xH2O H++HSO
H++HSO +(x-1)H2O;HSO
+(x-1)H2O;HSO
 SO
SO +H+。
+H+。通过分析上述现象,猜测使品红水溶液褪色的微粒可能是i.H2SO3;ii.
③为了证明上述猜测ii和iii,进行表中实验1和2,记录现象。
| 实验序号 | 实验1 | 实验2 |
| 实验操作 |  2mL0.20mol•L-1Na2SO3溶液 | 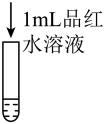 2mL0.20mol•L-1NaHSO3溶液 |
| 实验现象 | 迅速褪色 | 褪色较慢 |
④取实验1所得溶液直接加热接近沸腾,溶液不恢复红色,在热溶液中滴加稀硫酸则恢复红色;说明
您最近一年使用:0次
2023-04-28更新
|
380次组卷
|
3卷引用:江西省南昌市等5地2022-2023学年高一下学期4月期中考试化学试题
解题方法
9 .  溶液与KI溶液混合时,按照复分解反应原理分析,可得到AgI黄色沉淀。查阅资料可知:①
溶液与KI溶液混合时,按照复分解反应原理分析,可得到AgI黄色沉淀。查阅资料可知:① 溶液呈酸性;②
溶液呈酸性;② 具有较强的氧化性;③单质碘遇淀粉溶液会变蓝。根据所得信息,甲学生对
具有较强的氧化性;③单质碘遇淀粉溶液会变蓝。根据所得信息,甲学生对 溶液与KI溶液混合时发生的反应做出了如下猜测:
溶液与KI溶液混合时发生的反应做出了如下猜测:
猜测1:发生复分解反应。
猜测2: 与
与 发生氧化还原反应。
发生氧化还原反应。
(1)①如果猜测2成立,则发生反应的化学方程式为_______ ;为了验证该猜测,甲同学往反应后的溶液中加入淀粉,观察到溶液变蓝,证明猜测2成立。
②乙同学认为甲同学的实验方案不能证明猜测2成立,原因是 溶液中的
溶液中的 在酸性条件下具有较强的氧化性,也可能氧化
在酸性条件下具有较强的氧化性,也可能氧化 ,反应的离子方程式为
,反应的离子方程式为_______ ;该反应中的氧化剂和还原剂的物质的量之比为_______ 。
(2)乙同学利用原电池原理来验证以上猜测,设计了如图所示实验装置(盐桥中的离子可以自由移动,两烧杯中电解质溶液足量),一段时间后,电流计指针发生偏转, 溶液无气泡产生,石墨2表面有银白色金属析出。
溶液无气泡产生,石墨2表面有银白色金属析出。
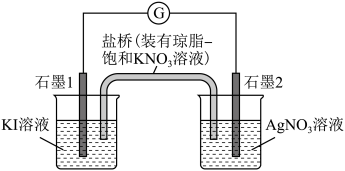
①该装置的负极为石墨_______ (填“1”或“2”)。
②若石墨2增重5.4g(不考虑其他反应),则电路中转移电子数为_______  。
。
③根据实验现象,证明猜测2成立。若将盐桥中的 溶液换成
溶液换成 溶液,一段时间后,电流计指针不发生偏转,可能原因是
溶液,一段时间后,电流计指针不发生偏转,可能原因是_______ 。
(3)原电池在生产生活和学习中有着广泛的应用,下列关于原电池的说法正确的是_______(填标号)。
 溶液与KI溶液混合时,按照复分解反应原理分析,可得到AgI黄色沉淀。查阅资料可知:①
溶液与KI溶液混合时,按照复分解反应原理分析,可得到AgI黄色沉淀。查阅资料可知:① 溶液呈酸性;②
溶液呈酸性;② 具有较强的氧化性;③单质碘遇淀粉溶液会变蓝。根据所得信息,甲学生对
具有较强的氧化性;③单质碘遇淀粉溶液会变蓝。根据所得信息,甲学生对 溶液与KI溶液混合时发生的反应做出了如下猜测:
溶液与KI溶液混合时发生的反应做出了如下猜测:猜测1:发生复分解反应。
猜测2:
 与
与 发生氧化还原反应。
发生氧化还原反应。(1)①如果猜测2成立,则发生反应的化学方程式为
②乙同学认为甲同学的实验方案不能证明猜测2成立,原因是
 溶液中的
溶液中的 在酸性条件下具有较强的氧化性,也可能氧化
在酸性条件下具有较强的氧化性,也可能氧化 ,反应的离子方程式为
,反应的离子方程式为(2)乙同学利用原电池原理来验证以上猜测,设计了如图所示实验装置(盐桥中的离子可以自由移动,两烧杯中电解质溶液足量),一段时间后,电流计指针发生偏转,
 溶液无气泡产生,石墨2表面有银白色金属析出。
溶液无气泡产生,石墨2表面有银白色金属析出。
①该装置的负极为石墨
②若石墨2增重5.4g(不考虑其他反应),则电路中转移电子数为
 。
。③根据实验现象,证明猜测2成立。若将盐桥中的
 溶液换成
溶液换成 溶液,一段时间后,电流计指针不发生偏转,可能原因是
溶液,一段时间后,电流计指针不发生偏转,可能原因是(3)原电池在生产生活和学习中有着广泛的应用,下列关于原电池的说法正确的是_______(填标号)。
| A.原电池是化学能转化为电能的装置 | B.原电池内发生的反应为氧化还原反应 |
| C.所有的化学反应均可设计成原电池 | D.电子从负极流出,经电解质溶液流入正极 |
您最近一年使用:0次
2023-05-20更新
|
196次组卷
|
2卷引用:辽宁省抚顺市重点高中六校协作体2022-2023学年高一下学期期中考试化学试题
10 . 某同学用下列装置进行有关 的实验。下列说法
的实验。下列说法不正确 的是
 的实验。下列说法
的实验。下列说法| A | B | C | D |
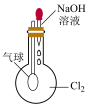 |  | 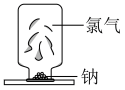 | 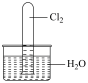 |
若气球变瘪,证明 可与 可与 溶液反应 溶液反应 | 证明氯气无漂白作用,氯水有漂白作用 | 剧烈燃烧,产生大量白烟 | 证明 可溶于水 可溶于水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-05更新
|
439次组卷
|
3卷引用:北京市第一○一中学2023-2024学年高一上学期期中考试化学试题



